

Đào Hạnh Thảo
Giới thiệu về bản thân



































Gọi số mol C3H8 và C4H10 trong bình gas 12 kg lần lượt là x và y, ta có:
(1) x : y = 3 : 7 ⇒ 7x - 3y = 0
(2) 44x + 58y = 12000
⇒ x = 66,61 mol; y = 156,13 mol
Nhiệt lượng tỏa ra khi đốt cháy 1 bình gas 12 kg:
66,61.2220 + 156,13.2874 = 596591,82 (kJ)
Hộ gia đình sử dụng được bình gas trong:
596591,82 : 6000 ≃ 99 (ngày).
a) Quan sát đồ thị, ta thấy nồng độ của chất nghiên cứu tăng dần theo thời gian nên đồ thị mô tả sự thay đổi nồng độ của chất sản phẩm.
⇒ Đồ thị mô tả sự thay đổi nồng độ của HBr.
b) Tốc độ trung bình của phản ứng:
\(\overset{\overline}{\upsilon} = \frac{\Delta C_{H B r}}{2. \Delta t}\)
\[\]
- Phản ứng đốt than:
C + O2 → CO2
- Phản ứng quang hợp:
6CO2 + 6H2O → C6H12O6 + O2
- Phản ứng đốt than:
C + O2 → CO2
- Phản ứng quang hợp:
6CO2 + 6H2O → C6H12O6 + O2
mglucose=100%mdd.C%=100%V.D.C%=100%500.1,1.5%=27,5(g)
⇒ \(n_{g l u c o s e} = \frac{27 , 5}{180} = \frac{11}{72} \left(\right. m o l \left.\right)\)
⇒ Năng lượng tối đa một người bệnh nhận được khi truyền một chai 500 mL dung dịch glucose 5% là
\(2803 , 0. \frac{11}{72} = 428 , 24 \left(\right. k J \left.\right)\).
a)
- Chất khử: HCl.
- Chất oxi hóa: MnO2.
b)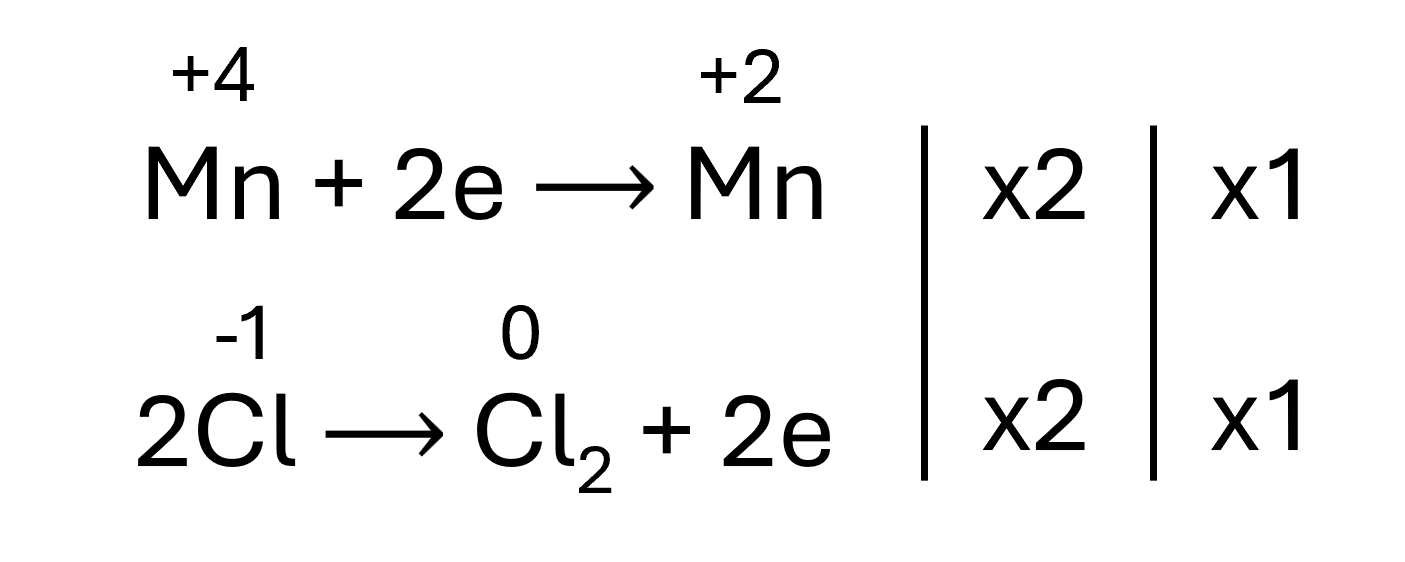
⇒ MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
- Phản ứng tỏa nhiệt:
+ Phản ứng đốt than.
+ Phản ứng phân hủy glucose trong cơ thể.
- Phản ứng thu nhiệt:
+ Phản ứng nhiệt phân KMnO4.
+ Phản ứng C sủi tan trong nước.
Bước 1: Tính số mol SO₂
Ở đktc:
\(n_{S O_{2}} = \frac{5 , 6}{22 , 4} = 0 , 25 \&\text{nbsp};\text{mol}\)
- Bước 2: Viết quá trình oxi hóa – khử
Kim loại bị oxi hóa
\(Z n \rightarrow Z n^{2 +} + 2 e\) \(A l \rightarrow A l^{3 +} + 3 e\)
Lưu huỳnh bị khử
Trong H₂SO₄ đặc:
\(S^{+6}\rightarrow S^{+4}\left(\right.\text{trongSO}_2\left.\right)\) \(S^{+ 6} + 2 e \rightarrow S^{+ 4}\)
→ 1 mol SO₂ nhận 2 mol e
- Bước 3: Bảo toàn electron
Tổng mol electron nhận:
\(0 , 25 \times 2 = 0 , 5 \&\text{nbsp};\text{mol}\)
Gọi:
\(n_{Z n} = x\) \(n_{A l} = y\)
Electron kim loại nhường:
\(2 x + 3 y = 0 , 5\)
- Bước 4: Bảo toàn khối lượng
\(65 x + 27 y = 9 , 2\)
- Bước 5: Giải hệ phương trình
\(2 x + 3 y = 0 , 5 65 x + 27 y = 9 , 2\)
Nhân phương trình (1) với 27:
\(54 x + 81 y = 13 , 5\)
Nhân phương trình (2) với 2:
\(130 x + 54 y = 18 , 4\)
Trừ hai phương trình:
\(76 x - 27 y = 4 , 9\)
Giải cùng với:
\(2 x + 3 y = 0 , 5\)
→ Giải ra:
\(x = 0 , 1 \&\text{nbsp};\text{mol}\) \(y=0,1\text{mol}\)
- Bước 6: Tính khối lượng Al
\(m_{Al}=0,1\times27=2,7\text{gam}\)
- Kết luận
\(\boxed{m_{Al}=2,7\text{gam}}\)
Ta xét phản ứng đốt cháy:
\(\textbf{C}_{3} \textbf{H}_{8} \left(\right. g \left.\right) + 5 \textbf{O}_{2} \left(\right. g \left.\right) \rightarrow 3 \textbf{CO}_{2} \left(\right. g \left.\right) + 4 \textbf{H}_{2} \textbf{O} \left(\right. g \left.\right)\)
a) Tính ΔH° phản ứng
- Dựa vào nhiệt tạo thành chuẩn
Công thức:
\(\Delta H^{\circ} = \sum \Delta H_{f}^{\circ} \left(\right. s p \left.\right) - \sum \Delta H_{f}^{\circ} \left(\right. t p \left.\right)\)
Dữ liệu (kJ/mol):
- ΔH°f(C₃H₈) = –105,00
- ΔH°f(CO₂) = –393,50
- ΔH°f(H₂O(g)) = –241,82
- ΔH°f(O₂) = 0
Tính toán
Tổng sản phẩm:
\(3 \left(\right. - 393 , 50 \left.\right) + 4 \left(\right. - 241 , 82 \left.\right)\) \(= - 1180 , 50 - 967 , 28\) \(=-2147,78\text{kJ}\)
Tổng chất tham gia:
\(- 105 , 00\)
Vậy:
\(\Delta H^{\circ} = - 2147 , 78 - \left(\right. - 105 , 00 \left.\right)\) \(=-2042,78\text{kJ}\)
- Kết quả theo nhiệt tạo thành:
\(\boxed{\Delta H^{\circ} = - 2042 , 78 \& \text{nbsp} ; \text{kJ}}\)
a) 8FeS + 30HNO₃ → 8Fe(NO₃)₃ + 9N₂O + 8H₂SO₄ + 7H₂O
b) 2NaCrO₂ + 3Br₂ + 8NaOH → 2Na₂CrO₄ + 6NaBr + 4H₂O
c) 3Fe₃O₄ + 28HNO₃ → 9Fe(NO₃)₃ + NO + 14H₂O
d) 4Mg + 10HNO₃ → 4Mg(NO₃)₂ + NH₄NO₃ + 3H₂O