

Lê Thị Hiền
Giới thiệu về bản thân



































\(ΔfH298°=ΣΔfH298°(sp)−ΣΔfH298°(cđ)\)= 2.(-393,5) + 3.(-285,84) - (-84,7) = -1559,82 kJ.
Áp dụng công thức \(v‾=ΔCΔt=0,22−0,14=0,03(Ms)v=ΔtΔC=40,22−0,1=0,03(sM)\)
a. PTHH
2KMnO4 + 16HClđặc ----> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Chất khử: HCl
Chất oxi hóa: KMnO4
Quá trình oxi hóa: 2Cl- ---> Cl20 + 2e |x5
Quá trình khử: Mn+7 + 5e ---> Mn+2 |x2
b, nNaI = 0,2.0,1 = 0,02 (mol)
PTHH: 2NaI + Cl2 ---> 2NaCl + I2
mol: 0,02 --> 0,01
=> PTHH: 2KMnO4 + 16HClđặc ----> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
mol: 0,004 <--- 0,01
=> mKMnO4 = n.M = 0,004.158 = 0,632(g)
a)
![]()
- Chất khử: HCl.
- Chất oxi hóa: MnO2.
b)
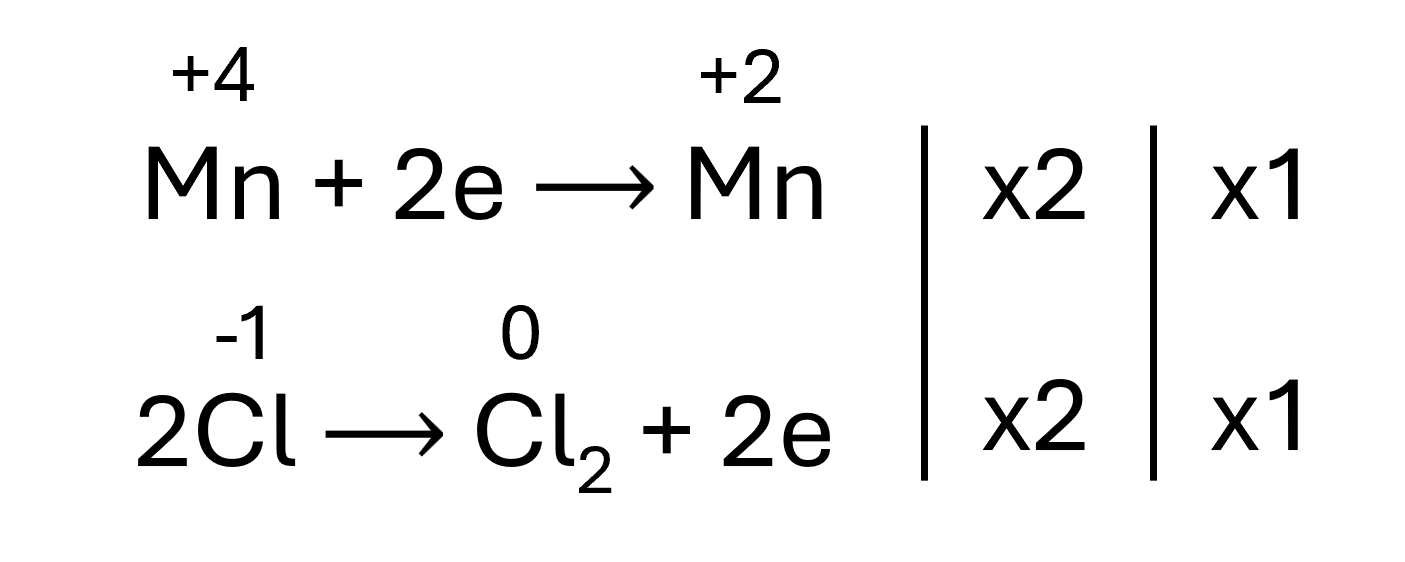
⇒ MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
- Phản ứng tỏa nhiệt:
+ Phản ứng đốt than.
+ Phản ứng phân hủy glucose trong cơ thể.
- Phản ứng thu nhiệt:
+ Phản ứng nhiệt phân KMnO4.
+ Phản ứng C sủi tan trong nước.
a) Tính biến thiên enthalpy chuẩn của phản ứng
Công thức: \(\Delta H_{p ư}^{o} = \sum E_{l k \textrm{ } b ị p h \overset{ˊ}{a} v ỡ} - \sum E_{l k \textrm{ } h \overset{ˋ}{\imath} n h t h \overset{ˋ}{a} n h}\)
- Phân tử C\(_{3}\)H\(_{8}\): 2 liên kết C–C, 8 liên kết C–H
- Phân tử O\(_{2}\): 5 liên kết O=O
- Phân tử CO\(_{2}\): 3 × 2 = 6 liên kết C=O
- Phân tử H\(_{2}\)O: 4 × 2 = 8 liên kết O–H
Năng lượng liên kết:
\(E_{C - C} = 346\), \(E_{C - H} = 418\), \(E_{O = O} = 494\), \(E_{C = O} = 732\), \(E_{O - H} = 459 \textrm{ } \left(\right. \text{kJ}/\text{mol} \left.\right)\)
Tổng năng lượng liên kết bị phá vỡ:
\(2 \times 346 + 8 \times 418 + 5 \times 494 = 692 + 3344 + 2470 = 6506 \textrm{ } \text{kJ}\)
Tổng năng lượng liên kết hình thành:
\(6 \times 732 + 8 \times 459 = 4392 + 3672 = 8064 \textrm{ } \text{kJ}\)\(\Delta H^{o} = 6506 - 8064 = - 1558 \textrm{ } \text{kJ}/\text{mol}\)
b) So sánh và giải thích
- Giá trị tính theo nhiệt tạo thành: \(- 2042 , 78 \textrm{ } \text{kJ}/\text{mol}\)
- Giá trị tính theo năng lượng liên kết: \(- 1558 \textrm{ } \text{kJ}/\text{mol}\)
Sự khác biệt đáng kể (khoảng \(484 , 78 \textrm{ } \text{kJ}/\text{mol}\)) là do:
- Năng lượng liên kết sử dụng là giá trị trung bình từ nhiều hợp chất, không đặc trưng cho từng phân tử cụ thể. Ví dụ, liên kết C=O trong CO\(_{2}\) có năng lượng cao hơn giá trị trung bình của liên kết đôi C=O trong các hợp chất carbonyl do cấu trúc cộng hưởng.
- Nhiệt tạo thành được xác định bằng thực nghiệm, phản ánh chính xác năng lượng của phản ứng trong điều kiện chuẩn.
- Vì vậy, kết quả từ nhiệt tạo thành đáng tin cậy hơn.
a. \(8 F e S + 42 H N O_{3} \rightarrow 8 F e \left(\right. N O_{3} \left.\right)_{3} + 9 N_{2} O + 8 H_{2} S O_{4} + 13 H_{2} O\)
b. \(2 N a C r O_{2} + 3 B r_{2} + 8 N a O H \rightarrow 2 N a_{2} C r O_{4} + 6 N a B r + 4 H_{2} O\)
c. \(3 F e_{n} O_{m} + \left(\right. 12 n - 2 m \left.\right) H N O_{3} \rightarrow 3 n F e \left(\right. N O_{3} \left.\right)_{3} + \left(\right. 3 n - 2 m \left.\right) N O + \left(\right. 6 n - m \left.\right) H_{2} O\)
d. \(4 M g + 10 H N O_{3} \rightarrow 4 M g \left(\right. N O_{3} \left.\right)_{2} + N H_{4} N O_{3} + 3 H_{2} O\)
a) Cân bằng phương trình phản ứng
5CaC2O4 + 2KMnO4 + 8H2SO4 → 5CaSO4 + K2SO4 + 2MnSO4 + 8H2O + 10CO2
b) Số mol KMnO4 cần dùng để phản ứng hết với calcium oxalate kết tủa từ 1 mL máu là:
2,05.10-3.4,88.10-4 = 10-6 mol
Số mol CaSO4 = 5/2. Số mol KMnO4 = 2,5x10-6 mol
Khối lượng ion calcium (mg) trong 100 mL máu là: 2,5x10-6x40x103x 100 = 10mg/100 mL.
ΔrH2980=∑ΔfH2980(sp)−∑ΔfH2980(cđ)
= -542,83 + (-167,16) - (-795,0)
= 85,01 kJ/mol.
a. Fe0 + HN+5O3 Fe+3(NO3)3 + N+2O + H2O.
Chất khử: Fe
Chất oxi hóa: HNO3
Quá trình oxi hóa: Feo --> Fe+3 +3e
Quá trình khử: N+5 + 3e ---> N+2
1Fe + 4HNO3 1Fe(NO3)3 + 1NO + 2H2O.
b. KMn+7O4 + Fe+2SO4 + H2SO4 Fe2+3(SO4)3 + Mn+2SO4 + K2SO4 + H2O.
Chất khử: FeSO4
Chất oxi hóa: KMnO4
Quá trình oxi hóa: 2Fe+2 ---> Fe2+3 + 1e.2
Quá trình khử: Mn+7 +5e ----> Mn+2
2KMnO4 + 10FeSO4 + 8H2SO4 \(\rightarrow\) 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O.