

Đồng Linh Giang
Giới thiệu về bản thân



































ọi hóa trị của M là n
\(n_{H_{2}} = \frac{0 , 2479}{24 , 79} = 0 , 01 \left(\right. m o l \left.\right) ; n_{M \left(\left(\right. O H \left.\right)\right)_{n}} = 0 , 5.0 , 04 = 0 , 02 \left(\right. m o l \left.\right)\)
PTHH: \(2 M + 2 n H_{2} O \rightarrow 2 M \left(\left(\right. O H \left.\right)\right)_{n} + n H_{2}\)
\(\frac{0 , 02}{n}\)<--------------\(\frac{0 , 02}{n}\)<--------0,01
\(M_{2} O_{n} + n H_{2} O \rightarrow 2 M \left(\left(\right. O H \left.\right)\right)_{n}\)
Theo PTHH: \(n_{M \left(\left(\right. O H \left.\right)\right)_{n}} = 2 n_{M_{2} O_{n}} + n_{M}\)
=> \(n_{M_{2} O_{n}} = \frac{0 , 02 - \frac{0 , 02}{n}}{2} = 0 , 01 - \frac{0 , 01}{n} \left(\right. m o l \left.\right)\)
=> \(\frac{0 , 01}{n} < 0 , 01 \Leftrightarrow n > 1\)
Do M là kim loại tan trong nước nên n = 2
=> \(n_{M} = \frac{0 , 02}{2} = 0 , 01 \left(\right. m o l \left.\right)\)
\(\rightarrow_{}^{\text{BTNT}\&\text{nbsp};\text{M}} n_{M O} = n_{M \left(\left(\right. O H \left.\right)\right)_{2}} - n_{M} = 0 , 02 - 0 , 01 = 0 , 01 \left(\right. m o l \left.\right)\)
=> \(0 , 01. \left(\right. M_{M} + 16 \left.\right) + 0 , 01. M_{M} = 2 , 9\)
=> \(M_{M} = 137 \left(\right. g / m o l \left.\right)\)
=> M là Barium (Ba)
công thức lewis của
CO2: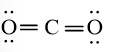
NH3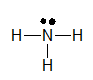
Công thức cấu tạo của CO2 là: O = C = O.
Công thức cấu tạo của NH3 là: \(H - N - H\)
\(\mid\)
H
Hợp chất tan trong nước: CO2 và NH3
Trong CO2 chứa hai liên kết cộng hóa trị phân cực C=O (đều phân cực về phía OO). Tuy nhiên, CO2 có cấu trúc phân tử thẳng (O=C=O) → 2 vectơ mô men cực cùng phương, ngược hướng triệt tiêu nhau → Phân tử CO2 không phân cực nên có tan trong nước song là ít tan
+ NH3 tan tốt trong nước vì NH3 có liên kết cộng hóa trị phân cực trong phân tử
X: 1s2 2s2 2p6 3s1
Y: 1s2 2s2 2p4
=>x là sodium
y là oxy
O+2e->O2-
Na->Na+ +
2Na+ +O2->Na2O