

Trần Trà My
Giới thiệu về bản thân



































Khối lượng của NaCl là 1,17kg
khối lượng của KCl là 0,745kg
b)
Chu kì 3, nhóm IIIA- Aluminium có 3 lớp electron nên thuộc chu kì 3.
- Electron cuối cùng điền vào phân lớp p, có 3 electron hóa trị (2 electron ở phân lớp 3s và 1 electron ở phân lớp 3p) nên thuộc nhóm IIIA.
Kết tủa `AgCl`: \(\frac{4 , 305}{143 , 5} = 0 , 03 \left(\right. m o l \left.\right)\)
Có: \(\left(\right. \overset{\overline}{M} + 35 , 5 \left.\right) . 0 , 03 = 1 , 915 \left(\right. g \left.\right) \Rightarrow \overset{\overline}{M} = 28 , 33\)
=> \(\left{\right. A : N a \\ B : K\)
=> \(\left{\right. x + y = 0 , 1 \\ 58 , 5 x + 74 , 5 y = 1 , 915 \Leftrightarrow \left{\right. x = 0 , 02 \\ y = 0 , 01\)
\(\Rightarrow X : \left{\right. m_{N a C l} = 1 , 17 \left(\right. g \left.\right) \\ m_{K C l} = 0 , 745 \left(\right. g \left.\right)\)
a) Ta có: p = e; p = 13
=> p = e = 13
- Cấu hình electron trong nguyên tử của nguyên tố Aluminium (Al) là:
+) Lớp thứ nhất: 2 electron
+) Lớp thứ hai: 8 electron
+) Lớp thứ ba: 3 3lectron
b) Vị trí của nguyên tố Aluminium trong bảng tuần hoàn các nguyên tố hóa học:
- Ô: 13
- Chu kì: 3
- Nhóm: IIIA
Theo bài ra ta có hệ phương trình:
a. Công thức Lewis của CO2: 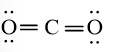
Công thức cấu tạo của CO2 là: O = C = O.
Công thức Lewis của NH3 là: 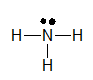
Công thức cấu tạo của NH3 là: \(H - N - H\)
\(\mid\)
H
b. Hợp chất tan trong nước: CO2 và NH3
Trong CO2CO2 chứa hai liên kết cộng hóa trị phân cực C=OC=O (đều phân cực về phía OO). Tuy nhiên, CO2CO2 có cấu trúc phân tử thẳng (O=C=OO=C=O) → 2 vectơ mô men cực cùng phương, ngược hướng triệt tiêu nhau → Phân tử CO2CO2 không phân cực nên có tan trong nước song là ít tan
+ NH3 tan tốt trong nước vì NH3 có liên kết cộng hóa trị phân cực trong phân tử
a, Y có số hiệu nguyên tử là 8 => Y là oxi
=> cấu hình electron là: \(1 s^{2} 2 s^{2} 2 p^{4}\)
X có số hiệu nguyên tử là 11 => X là natri
=> cấu hình electron là: \(1 s^{2} 2 s^{2} 2 p^{6} 3 s^{1}\)
b.O + 2e → O2-
2Na \(\rightarrow\) 2Na\(^{1 +}\)+2e
=> \(2 N a^{1 +} + O^{- 2} \rightarrow N a_{2} O\)