

NGUYỄN THỊ THANH HUYỀN
Giới thiệu về bản thân
Chào mừng bạn đến với trang cá nhân của NGUYỄN THỊ THANH HUYỀN





0





0





0





0





0





0





0
2025-12-28 20:34:33
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.
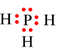
2025-12-08 22:26:26
a) Z = 20 → nguyên tử R có 20 electron. Cấu hình electron (theo lớp):
1s² 2s² 2p⁶ 3s² 3p⁶ 4s².
b) Vị trí trong bảng tuần hoàn:
- Chu kì 4 (vì electron ngoài cùng ở lớp n = 4).
- Nhóm 2 (nhóm kim loại kiềm thổ), khối s.
c) Tính chất hoá học đặc trưng:
- Là kim loại kiềm thổ, có tính kim loại (dẫn điện, bóng, dễ uốn).
- Dễ mất 2 electron để thành ion +2 (M²⁺) — oxi hóa thành R²⁺.
- Phản ứng với O₂ tạo oxit dạng MO (ví dụ Ca + 1/2 O₂ → CaO).
- Phản ứng với nước tạo dung dịch bazơ (nhưng kém phản ứng hơn nhóm kiềm): M + 2H₂O → M(OH)₂ + H₂ (tùy mức hoạt tính).
- Tạo muối ion với halogen (MCl₂, MBr₂…), với axit tạo muối và giải phóng H₂.
(Ứng xử điển hình: ion hóa trị +2, hợp chất ion mạnh.)
d) Dữ kiện: đốt 8,0 g R trong O₂ → thu 11,2 g chất rắn (sản phẩm rắn là oxit của R).
- Khối lượng O kết hợp = 11,2 − 8,0 = 3,2 g.
- Tỉ số khối lượng O : R = 3,2 : 8,0 = 0,4.
Phương trình tổng quát (mỗi mol kim loại M tạo M O): M + ½O₂ → MO, nên trên cơ sở 1 mol M, khối lượng O kết hợp = 16 g (1 nguyên tử O).
Ta có: \dfrac{16}{A_r(M)} = 0{.}4.
Suy ra A_r(M) = \dfrac{16}{0.4} = 40.
Nguyên tố có Z = 20 và khối lượng nguyên tử ≈ 40 là canxi (Ca).
Kết luận: R là canxi (Ca).