S + HCL có pứ ko
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a/ nHCl = nH2SO4 = 0,2 x 0,3 = 0,06 mol
nH2 = 1,8816 : 22,4 = 0,082 mol
Ta có: nH (axit) = 0,06 + 0,06 x 2 = 0,18 mol
nH(H2) = 0,084 x 2 = 0,168 mol < 0,18 => axit còn dư
Vậy hỗn hợp kim loại tan hết
b/ Đặt CT tương đương 2 axit là HX
Gọi x, y, z lần lượt là sô mol của Al, Mg, Zn trong hõn hợp
PTHH 2Al + 6HX ===> 2AlX3 + 3H2
Zn + 2HX ===> ZnX2 + H2
Mg + 2HX ===> MgX2 + H2
Sơ đô: 2Al=>3H2 ; Mg => H2 ; Zn=>H2
x 1,5x y y z z (mol)
Theo đề bài ta có hệ pt\(\begin{cases}27x+24y+65z=2,661\\1,5+y+z=0,084\\27x-24y=0\end{cases}\)
=> x = 0,024(mol)
y =0,027(mol)
z=0,021(mol)
=> mZn = 0,021 x 65 = 1,365 gam
=>%mZn = 1,365 / 2,661 = 51,3%

a) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
_____0,1-->0,2----->0,1----->0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
b) \(V_{ddHCl}=\dfrac{0,2}{0,5}=0,4\left(l\right)\)
c) \(C_{M\left(ZnCl_2\right)}=\dfrac{0,1}{0,5}=0,2M\)

Nếu phản ứng xảy ra hoàn toàn thì khối lượng hỗn hợp phải là 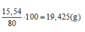
![]()

Cho Zn pứ hết với HCl thu 4,48l H2
a)Tính mHCl pứ
PTHH : \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PTHH :
\(n_{HCl}=2.n_{H_2}=2.0,2=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=n.M=0,4.36,5=14,6\left(g\right)\)
b)Cho lượng HCl trên pứ hết với Zn .Tính số phân tử H2 tạo ra
Số phân tử H2 = \(n.6.10^{23}=0,2.6.10^{23}=1,2.10^{23}\) (phân tử )

a) $Mg + 2HCl \to MgCl_2 + H_2$
$n_{MgCl_2} = \dfrac{4,75}{95} = 0,05(mol)$
$n_{HCl} = 2n_{MgCl_2} = 0,1(mol)$
$m_{dd\ HCl} = \dfrac{0,1.36,5}{14,6\%} = 25(gam)$
$\Rightarrow V_{dd\ HCl} = \dfrac{25}{1,12} = 22,32(ml)$
b) $n_{Mg} = n_{H_2} = n_{MgCl_2} = 0,05(mol)$
$\Rightarrow m_{dd\ sau\ pư} = 0,05.24 + 25 - 0,05.2 = 26,1(gam)$
$C\%_{HCl} = \dfrac{4,75}{26,1}.100\% = 18,2\%$

a)Zn+2HCl--->ZnCl2+H2
b) n\(_{Zn}=\frac{9,75}{65}=0,15\left(mol\right)\)
Theo pthh
n\(_{H2}=n_{Zn}=0,15\left(mol\right)\)
V\(_{H2}=0,15.22,4=3,36\left(l\right)\)
b) n\(_{HCl}=\frac{14,6}{36,5}=0,4\left(mol\right)\)
Theo pthh
n\(_{HCl}=2n_{Zn}=0,3\left(mol\right)\)
m\(_{HCl}dư=\left(0,4-0,3\right)36,5=3,65\left(g\right)\)
c) m\(_{HCl}=1,2.100=120\left(g\right)\)
C%=\(\frac{0,15.136}{120+9,75-0,3}.100\%=1,13\%\)


pứ ?
???