Thí nghiêm 4: Phản ứng Cu với dung dịch H2SO4 đặc nóng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn C
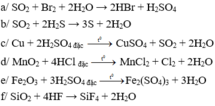
→ Các phản ứng a, b, c và d thuộc phản ứng oxi hóa – khử

Gọi $n_{Mg} = a ; n_{Al} = b ; n_{Cu} = c$
$\Rightarrow 24a + 27b + 64c = 16,6(1)$
Thí nghiệm 1 :
$Mg + H_2SO_4 \to MgSO_4 + H_2$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$\Rightarrow n_{H_2} = a + 1,5b = \dfrac{11,2}{22,4} = 0,5(2)$
Thí nghiệm 2 : $n_{SO_2} = \dfrac{13,44}{22,4} = 0,6(mol)$
Bảo toàn electron :
$2a + 3b + 2c = 0,6.2(3)$
Từ (1)(2)(3) suy ra a = 0,2 ; b = 0,2 ; c = 0,1
$m_{Mg} = 0,2.24 = 4,8(gam)$
$m_{Al} = 0,2.27 = 5,4(gam)$
$m_{Cu} = 0,1.64 = 6,4(gam)$

Chọn D.
(1) Cu + Fe2(SO4)3 ® CuSO4 + 2FeSO4
(2) 2CO2 + Ca(OH)2 ® Ca(HCO3)2
(3) 4NO2 + O2 + 2H2O ® 4HNO3
(4) MnO2 + 4HCl → t ∘ MnCl2 + Cl2 + 2H2O
(5) 2FeO + 4H2SO4 ® Fe2(SO4)3 + SO2 + 4H2O
(6) Fe3O4 + 8HCl ® FeCl2 + 2FeCl3 + 4H2O

Đáp án D
(a) Cho dung dịch AgNO3 vào dung dịch HBr.
(d) Cho Ba(OH)2 vào dung dịch NaHCO3.

Đáp án D
(a) AgNO3 + HCl → AgCl ↓ + HNO3
(b) Al2O3 + 2NaOH → 2NaAlO2 + H2O
(c) Cu + 2H2SO4 (đặc, nóng) → CuSO4 + SO2 ↑ + 2H2O
(d) Ba(OH)2 + 2NaHCO3 → BaCO3 ↓ + Na2CO3 + 2H2O
=> Vậy có (a) và (d) tạo kết tủa
- Tiến hành TN
+ Cho 1-2 mảnh đồng vào ống nghiệm chứa 2-3 ml dd H2SO4 đặc, đun nóng
+ Nhỏ vài giọt dd NaOH vào dd vừa thu được, quan sát.
- Hiện tượng
+ Có bọt khí không màu thoát ra, có mùi hắc.
+ Dung dịch trong ống nghiệm chuyển màu xanh.
+ Khi nhỏ thêm dd NaOH thấy xuất hiện kết tủa màu xanh và phản ứng chậm lại
- Giải thích
Cu phản ứng với H2SO4 sinh ra khí SO2 (mùi hắc) và dd Cu2+ màu xanh.
Khi nhỏ thêm dd NaOH thấy xuất hiện kết tủa màu xanh là Cu(OH)2 và phản ứng chậm lại do nồng độ H2SO4 giảm
PTHH: Cu + 2H2SO4 → CuSO4 + SO2 ↑ (mùi hắc) + 2H2O
CuSO4 + 2NaOH → Cu(OH)2 ↓ xanh + Na2SO4
NaOH + H2SO4 → Na2SO4 + H2O (phản ứng làm giảm nồng độ axit ⇒ làm phản ứng xảy ra chậm)