tính pH dung dịch x gồm hcl 0,01m và h2so4 0,02m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H^+}=0,2.\left(0,02+0,01.2\right)=0,008\left(mol\right)\)
\(n_{OH^-}=0,3.2.0,04=0,024\left(mol\right)\)
\(n_{OH^-dư}=0,3.2.0,04=0,016\left(mol\right)\)
\(\Rightarrow\left[OH^-_{dư}\right]=\dfrac{0,016}{0,5}=0,032M\)
\(\Rightarrow\left[H^+\right]=3,125.10^{-13}M\)
\(\Rightarrow pH\approx12,5\)

Ta có:
$ V_{HCl} = 100,ml = 0{,}1,L,\quad C_{HCl} = 0{,}02,M $
$ V_{H_2SO_4} = 100,ml = 0{,}1,L,\quad C_{H_2SO_4} = 0{,}01,M $
Số mol axit:
$ n_{HCl} = 0{,}1 \times 0{,}02 = 0{,}002\ \text{mol} $
$ n_{H_2SO_4} = 0{,}1 \times 0{,}01 = 0{,}001\ \text{mol} $
Do $H_2SO_4$ là axit mạnh 2 nấc nên:
$ n_{H^+ \text{ từ } H_2SO_4} = 2 \times 0{,}001 = 0{,}002\ \text{mol} $
Tổng số mol $H^+$:
$ n_{H^+} = 0{,}002 + 0{,}002 = 0{,}004\ \text{mol} $
Thể tích dung dịch sau khi trộn:
$ V = 0{,}1 + 0{,}1 = 0{,}2,L $
Nồng độ ion $H^+$:
$ [H^+] = \dfrac{0{,}004}{0{,}2} = 0{,}02,M $
Giá trị pH:
$ pH = -\log [H^+] = -\log(0{,}02) \approx 1{,}7 $
Vậy $ pH \approx 1{,}7 $
Dung dịch có môi trường axit.

Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 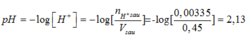


Ta có: \(\left[H^+\right]=0,01+0,02\cdot2=0,05\left(M\right)\) \(\Rightarrow pH=-log\left(0,05\right)\approx1,3\)