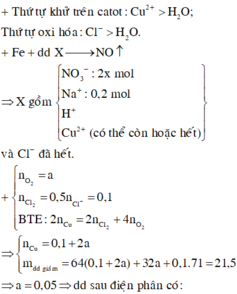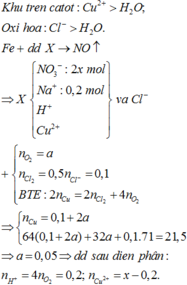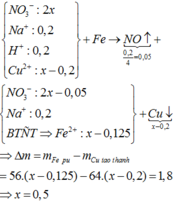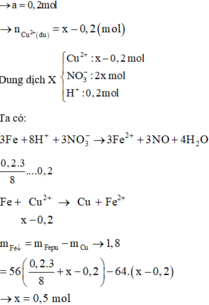Cho m g Cu vào đ Fe(NO3)3. Sau phản ứng thấy Cu giảm 0.8g. Tính lượg muối thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Do sau phản ứng vẫn còn chất rắn nên Fe và Cu hoặc cả Fe và Cu đều còn. Khi Fe hoặc Cu còn thì Fe3+ đã chuyển hoàn toàn thành Fe2+.

Đáp án D
Khi nhúng thanh sắt vào X thì tạo khí NO → có H+
Ta có dung dịch X thu được có màu xanh → Cu2+ dư → catot chưa điện phân nước
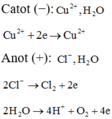
Gọi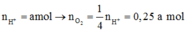
Bảo toàn e
![]()
![]()
![]()
![]()
![]()
Dung dịch X
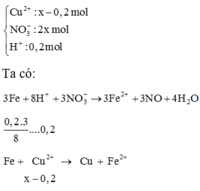
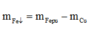
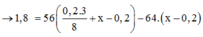
![]()

Đáp án D
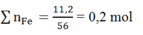
Khi ngâm m gam vào dung dịch Cu(NO3)2 thì chỉ có Fe phản ứng:
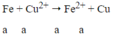
Δm = 64a - 56a = 8a → nFe = 0,4/8 = 0,05 mol
Fe3O4 → 3Fe
b 3b
Ta có: 0,05 + 2b = 0,2 → b = 0,05 mol
m = 0,05.56 + 0,05.232 = 14,4g

Cho hỗn hợp X tác dụng với H2SO4 loãng dư thì chỉ có Fe và Mg phản ứng; nên khối lượng CU là 1,28 gam
\(\text{ -> nCu=0,02 mol}\)
\(\text{Fe + H2SO4 -> FeSO4 + H2; Mg + H2SO4 -> MgSO4 + H2}\)
Gọi số mol Fe và Mg lần lượt là x, y -> nH2=x+y =1,456/22,4=0,065 mol
Cho X tác dụng với H2SO4 đặc nóng dư
\(\text{2Fe + 6 H2SO4 -> Fe2(SO4)3 + 3SO2 + 6H2O}\)
\(\text{Mg + 2H2SO4 -> MgSO4 + SO2 + H2O }\)
\(\text{Cu + 2H2SO4 -> CuSO4 + SO2 + H2O }\)
Theo ptpu: nSO2=3/2nFe+nMg+nCu=1,5x+y+0,02=0,105
\(\text{Giải được x=0,06; y=0,005}\)
\(\text{-> a=mFe+mCu +mMg=4,76 gam }\)
\(\Rightarrow\left\{{}\begin{matrix}\text{%Fe=70,59%}\\\text{ %Cu=26,89%}\\\text{%Mg=2,52%}\end{matrix}\right.\)