mọi người giúp với mai nộp rồi ạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





Bài 3:
Gọi O là trung điểm của AH
Vì \(\hat{AEH}=\hat{ADH}=90^0\)
nên A,D,H,E cùng thuộc đường tròn đường kính AH
=>A,D,H,E cùng thuộc (O)
=>O là tâm đường tròn ngoại tiếp ΔADE
Gọi K là giao điểm của AH và BC
Xét ΔABC có
BD,CE là các đường cao
BD cắt CE tại H
Do đó: H là trực tâm của ΔABC
=>AH⊥BC tại K
OE=OH
=>ΔOEH cân tại O
=>\(\hat{OEH}=\hat{OHE}\)
mà \(\hat{OHE}=\hat{AHE}=\hat{ABC}\left(=90^0-\hat{BAH}\right)\)
nên \(\hat{OEH}=\hat{ABC}\)
ΔEBC vuông tại E
mà EI là đường trung tuyến
nên IE=IC
=>ΔIEC cân tại I
=>\(\hat{IEC}=\hat{ICE}\)
\(\hat{OEI}=\hat{OEC}+\hat{IEC}\)
\(=\hat{EBC}+\hat{ECB}=90^0\)
=>IE là tiếp tuyến tại E của (O)
ΔDBC vuông tại D
mà DI là đường trung tuyến
nên DI=IB=IC
Xét ΔIEO và ΔIDO có
IE=ID
EO=DO
IO chung
Do đó: ΔIEO=ΔIDO
=>\(\hat{IEO}=\hat{IDO}\)
=>\(\hat{IDO}=90^0\)
=>DI là tiếp tuyến tại D của (O)


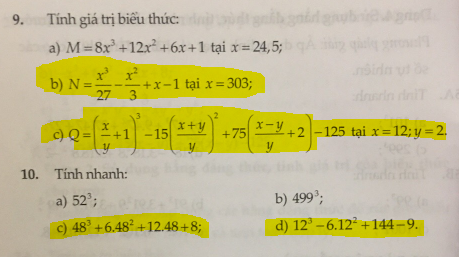 Mọi người ơi giúp em với ạ. Mai em phải nộp rồi. Mấy phần em đánh dấu đó mọi người.
Mọi người ơi giúp em với ạ. Mai em phải nộp rồi. Mấy phần em đánh dấu đó mọi người. 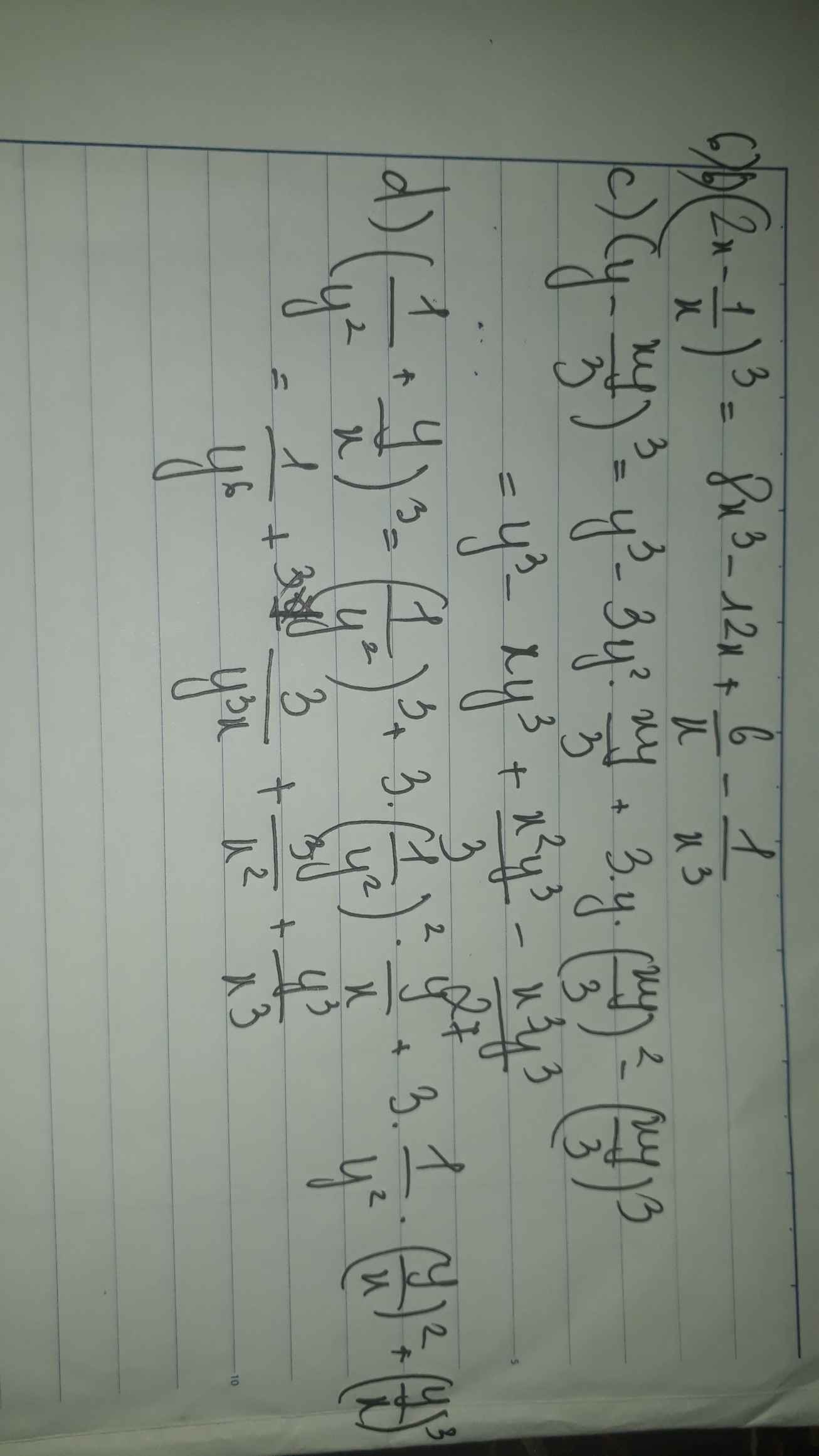













Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O (1)
x<----------8x<-----------2x<--------x
2FeCl3 + Cu → 2FeCl2 + CuCl2 (2)
2x---------->x------->2x
\(Fe^{2+}+2OH^-\rightarrow Fe\left(OH\right)_2\)
3x-------->6x------------->3x
\(Cu^{2+}+2OH^-\rightarrow Cu\left(OH\right)_2\)
x---------->2x-------------->x
\(H^++OH^-\rightarrow H_2O\)
\(n_{OH^-}=0,5.1+0,5.1=1\left(mol\right)\)
\(m_{KLkhongtan}=m_{Cu}\)
Dung dịch Y : FeCl2, FeCl3, HCl dư
Theo PT (1) \(n_{FeCl_2}=x\left(mol\right);n_{FeCl_3}=2x\left(mol\right)\)
Theo PT (2) \(n_{CuCl_2}=x\left(mol\right);n_{FeCl_2}=2x\left(mol\right)\)
Theo PT (2) : \(\Sigma n_{FeCl_2}=3x\left(mol\right)\)
Sau phản ứng => 36,8 gam kết tủa
\(m_{kt}=m_{Cu\left(OH\right)_2}+m_{Fe\left(OH\right)_2}=x.98+3x.90=36,8\)
=> x=0,1(mol)
\(m=m_{Cu\left(pứ\right)}+m_{Cu\left(dư\right)}+m_{Fe_3O_4}=0,1.64+1,6+0,1.232=31,2\left(g\right)\)
\(n_{HCl\left(dư\right)}=1-\left(2x+6x\right)=0,2\left(mol\right)\)
\(n_{HCl\left(pứ\right)}=8x=0,8\left(mol\right)\)
=> \(n_{HCl\left(bđ\right)}=0,8+0,2=1\left(mol\right)\)