Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. Lập công thức khi biết hóa trị
Giả sử hợp chất gồm 2 nguyên tố A và B, có hóa trị lần lượt là \(x\) và \(y\).
- Quy tắc: Tích chéo hóa trị → chỉ số nguyên tử.
\(A_{x} B_{y} \rightarrow A_{y} B_{x}\)
📌 Ví dụ: Lập công thức của hợp chất giữa Al (III) và O (II):
\(A l^{3 +} , \&\text{nbsp}; O^{2 -} \Rightarrow A l_{2} O_{3}\)
2. Lập công thức khi biết thành phần phần trăm khối lượng các nguyên tố
Quy trình:
Bước 1: Giả sử có 100 g hợp chất
→ số gam mỗi nguyên tố chính bằng phần trăm của nó.
Bước 2: Tính số mol từng nguyên tố
\(n = \frac{\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{l}ượ\text{ng}}{\text{nguy} \hat{\text{e}} \text{n}\&\text{nbsp};\text{t}ử\&\text{nbsp};\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}}\)
Bước 3: Chia số mol cho giá trị nhỏ nhất
→ được tỉ lệ số nguyên tử gần đúng.
Bước 4: Rút gọn thành số nguyên tối giản
→ đó là công thức đơn giản nhất (công thức nguyên).
Bước 5 (nếu đề cho M – khối lượng mol của hợp chất):
Tính hệ số \(k = \frac{M_{t h ự c}}{M_{đo n g i ả n}}\).
Nhân toàn bộ chỉ số trong công thức đơn giản với \(k\) để ra công thức phân tử.
📌 Ví dụ: Hợp chất X có 40% C, 6,7% H, 53,3% O. Xác định công thức.
- Giả sử 100 g chất → C: 40 g, H: 6,7 g, O: 53,3 g.
- Số mol:
\(n_{C} = \frac{40}{12} \approx 3.33 , n_{H} = \frac{6.7}{1} \approx 6.7 , n_{O} = \frac{53.3}{16} \approx 3.33\) - Chia cho số nhỏ nhất (3.33):
\(C : 1 , \&\text{nbsp}; H : 2 , \&\text{nbsp}; O : 1\)
→ Công thức đơn giản nhất: CH₂O.
- Nếu khối lượng mol thực tế cho là 60 g/mol → khối lượng mol CH₂O = 30 → \(k = 2\).
→ Công thức phân tử: C₂H₄O₂.

Công thức hóa học của ethanol là
C2H6Obold cap C sub 2 bold cap H sub 6 bold cap O𝐂𝟐𝐇𝟔𝐎(hoặc
C2H5OHbold cap C sub 2 bold cap H sub 5 bold cap O bold cap H𝐂𝟐𝐇𝟓𝐎𝐇).

Câu trả lời là Có. Nguyên tắc sắp xếp các nguyên tố hóa học để dễ nhận ra tính chất của chúng được thể hiện rõ nhất trong Bảng tuần hoàn các nguyên tố hóa học (thường được gọi tắt là Bảng tuần hoàn).

a) khối lượng phân tử của hợp chất là: 64*3,625=232
b) khối lượng nguyên tử của X là :
3*M(X) + 4*M(O) = 232
3*M(X) = 232-4*M(O)
3*M(X) = 232 - 4*16
3*M(X) = 168
M(X) = 56
Vậy nguyên tố X là iron, kí hiệu hóa học là Fe

- Nguyên tố có số hiệu nguyên tử 1 là Hiđro (H).
- Nguyên tố có mặt nhiều nhất trong vỏ Trái Đất là Oxi (O).
- Nguyên tố kim loại nhẹ nhất là Liti (Li).
- Kí hiệu hóa học của nguyên tố Sắt là Fe.
- Kí hiệu hóa học của nguyên tố Đồng là Cu.
- BTVN tự làm đê !

Tóm tắt lại cho dễ nhớ:
- Nguyên tử có cùng số proton → thuộc cùng một nguyên tố hóa học → Ví dụ: mọi nguyên tử có 1 proton đều là nguyên tử Hidro (H)
- Kí hiệu nguyên tố hóa học:
- Gồm 1 hoặc 2 chữ cái
- Chữ cái đầu viết hoa, chữ sau (nếu có) viết thường
- Ví dụ:
- O: Oxi
- Na: Natri
- Fe: Sắt
- Cl: Clo
Mẹo học nhanh:
- Số proton = số hiệu nguyên tử trong bảng tuần hoàn
- Kí hiệu hóa học thường lấy từ tên tiếng Latin hoặc tiếng Anh của nguyên tố

Câu 1. vì nguyên tố iron có khả năng tạo nhiều hợp chất bền và tham gia cấu trúc của hemoglobin, là chất vận chuyển oxy trong máu, nhờ đó quyết định màu đỏ đặc trưng của hồng cầu nên trở thành thành phần quan trọng nhất trong hồng cầu
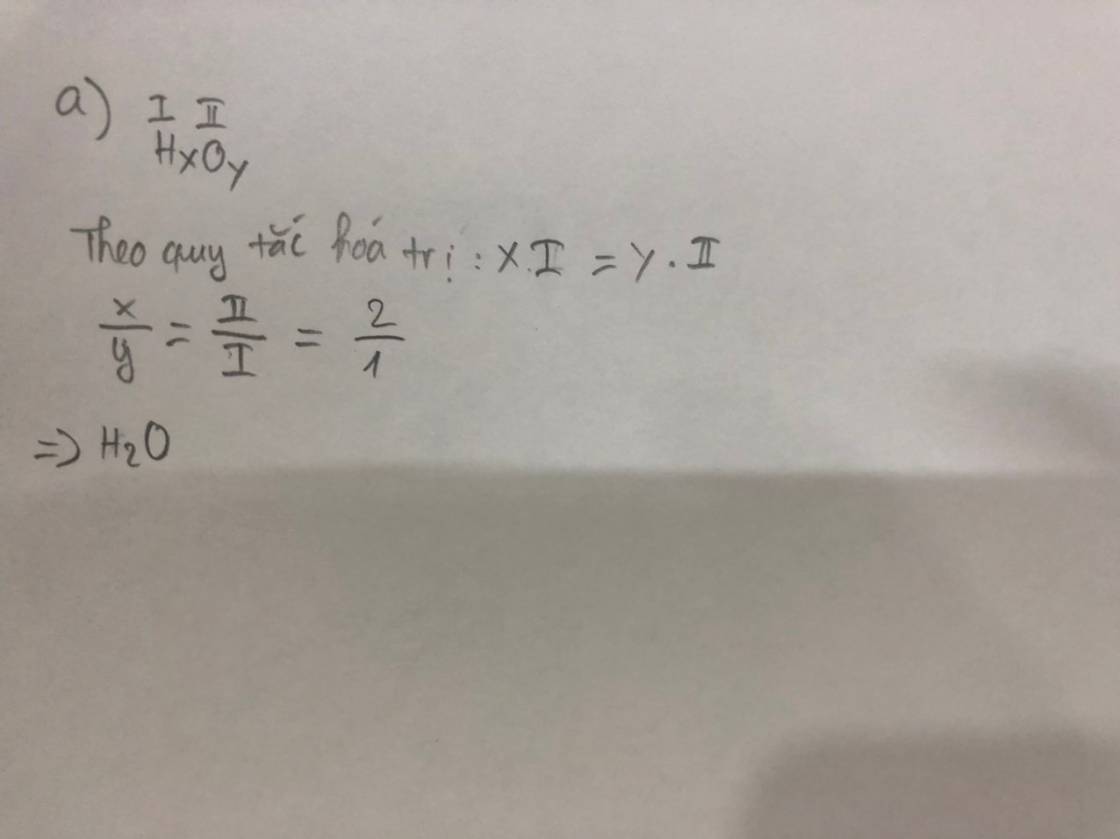
1. Công thức tính % khối lượng Oxygen ($O$):
$$\%m_O = \frac{y \cdot M_O}{M_{hợp\ chất}} \cdot 100\%$$Trong đó:
2. Ví dụ minh họa cho dễ hiểu:
Bài toán: Tính % khối lượng của $O$ trong phân tử nước ($H_2O$).
=(Khối lượng mol của hợp chất : Khối lượng mol của oxygen)×100%
Công thức tính % khối lượng Oxygen (O):
Với hợp chất có công thức tổng quát AxOy:
%mO=Mhợp cha^ˊty×16×100%Trong đó: