Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.

Quặng này chứa 10% tạp chất trơ tức
FeS2 chiếm 90%.
Vậy khối lượng quặng pirit sắt cần:
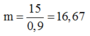

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.


mFeS2=1,6.10^6.60%=960000g
=>nFeS2=960000/120=8000 mol
Sơ đồ cả quá trình tạo H2SO4
FeS2 =>2SO2 =>2SO3 =>2H2SO4
8000 mol =>16000 mol
Theo sơ đồ bảo toàn ngtố S ta có nH2SO4=8000.2.80%=12800 mol
=>mH2SO4=12800.98=1254400g=1,2544 tấn

Fe + 2H+ → Fe2+ + H2↑
Fe2O3 + 6H+ → 2Fe3+ + 3H2O
25ml dd phản ứng với 12,5ml dd KMnO4 0,096M
→ 500ml dd phản ứng với
\(\frac{500.12,5}{25}\) = 250ml dd KMnO4 0,096M
nKMnO4 phản ứng với 500ml dd = 0,096 . 0,25 = 0,024 mol
Fe+2 → Fe+3 + 1e M+7 + 5e → Mn+2
0,12 ← 0,12 0,12←0,024
(Bảo toàn e)
nFe = nFe2+ = 0,12 mol
\(\%m_{Fe}=\frac{0,12.56}{7,81}.100\%=93,59\%\)
Chọn A
