Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

b,\(n_{HCl}=0,2.2=0,4\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2
Mol: 0,2 0,4
\(\Rightarrow m_{CuO}=0,2.80=16\left(g\right)\)
c,\(n_{ZnO}=\dfrac{16,2}{81}=0,2\left(mol\right)\)
PTHH: ZnO + H2SO4 → ZnSO4 + H2
Mol: 0,2 0,2
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{0,2}{2}=0,1\left(l\right)\)
d,\(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
PTHH: H2SO4 + 2KOH → K2SO4 + 2H2O
Mol: 0,2 0,4
\(\Rightarrow V_{ddKOH}=\dfrac{0,4}{1}=0,4\left(l\right)\)

Gọi \(\left\{{}\begin{matrix}C_{M\left(A\right)}=aM\\C_{M\left(B\right)}=bM\end{matrix}\right.\)
Giả sử trộn 50ml dd A với 50ml dd B để thu được 100ml dd C
=> \(\left\{{}\begin{matrix}n_{NaOH}=0,05a\left(mol\right)\\n_{Ba\left(OH\right)_2}=0,05b\left(mol\right)\end{matrix}\right.\)
\(n_{BaSO_4}=\dfrac{9,32}{233}=0,04\left(mol\right)\)
nH2SO4 = 0,035.2 = 0,07 (mol)
PTHH: Ba(OH)2 + H2SO4 --> BaSO4 + 2H2O
0,04<----0,04<-------0,04
2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,06<----0,03
=> \(\left\{{}\begin{matrix}0,05a=0,06\\0,05b=0,04\end{matrix}\right.\)
=> a = 1,2; b = 0,8
20 ml dd A chứa nNaOH = 0,02.1,2 = 0,024 (mol)
\(n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
PTHH: 2NaOH + Al2O3 --> 2NaAlO2 + H2O
0,024-->0,012
Ba(OH)2 + Al2O3 --> Ba(AlO2)2 + H2O
0,188<---0,188
=> \(V_{dd.B}=\dfrac{0,188}{0,8}=0,235\left(l\right)=235\left(ml\right)\)

bạn thử làm như sau nhé
TN1 : 2HCl + Ba(OH)2 = BaCI2 + 2H2O
Gọi a là nồng độ mol/llít của ddA, b là nồng độ mol/lít của dd B, thí nghiệm 1 cho thấy dd thiếu là ddB (Ba(OH)2 ) từ đó kéo số mol dd Ba(OH)2 wa là 0,05b ra số mol dd A phản ứng là 0,1b mol.
HCl + NaOH = NaCl + H2O
từ số mol NaOH đề cho phản ứng với HCl dư là 0,1x0,05= 0,005 mol ta suy ra số mol HCl dư là 0,005 mol.
Như vậy tổng số mol HCl tham gia phản ứng trong TN 1 là 0,1b + 0,005 mol, ta có phương trình 0,1b + 0,005 = 0,05a
TN2 tương tự như vậy nhưng ở đây dd Ba(OH)2 là dd còn dư sau phản ứng,số mol dư là 0,07 mol ( kéo từ số mol HNO3 tham gia phản ứng ) ,như vậy tổng số mol Ba(OH)2 tham gia là 0,05a + 0,07 mol, ta có phương trình 0,05a + 0,07 = 0,15b giải hệ phương trình sẽ ra lần lượt a và b .

n HCl = \(0,796.2\) =1,592 (mol)
n H2 = \(\dfrac{4,368}{22,4}\)=0,195 (mol)
Bảo toàn nguyên tố H
=> n H2O =\(\dfrac{1,592-0,195.2}{2}\) = 0,601 (mol)
=> m H2O = 10,818 g
Áp dụng định luật bảo toàn khối lượng :
m muối khan = m hỗn hợp + m axit - m H2O - mH2
=> 26,43 + 1,592.36,5 - 10,818 - 0,195.2
= 73,33 g

$n_{NaOH}=0,2.0,5=0,1mol \\PTHH : \\NaOH+HCl\to NaCl+H_2O \\NaOH+HNO_3\to NaNO_3+H_2O \\Gọi\ n_{HCl}=x;n_{HNO_3}=y(x,y>0) \\Ta\ có : \\n_{NaOH}=x+y=0,1mol \\m_{muối}=58,5x+85y=6,38g$
$\text{Ta có hpt :}$
$\left\{\begin{matrix} x+y=0,1 & \\ 58,5x+85y=6,38 & \end{matrix}\right.⇔\left\{\begin{matrix} x=0,08 & \\ y=0,02 & \end{matrix}\right. \\⇒C\%_{HNO_3}=\dfrac{63.0,02}{100}.100\%=1,26\% \\C\%_{HCl}=\dfrac{36,5.0,08}{400}.100\%=0,73\%$

\(n_{NaOH}=0,2.1=0,2\left(mol\right)\\ n_{H_2SO_4}=0,3.1,5=0,45\left(mol\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,2------->0,1--------->0,1
Xét \(\dfrac{0,2}{2}< \dfrac{0,45}{1}\Rightarrow\) \(H_2SO_4\)dư
Trong dung dịch D có:
\(\left\{{}\begin{matrix}n_{H_2SO_4}=0,45-0,1=0,35\left(mol\right)\\n_{Na_2SO_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}CM_{H_2SO_4}=\dfrac{0,35}{0,5}=0,7M\\CM_{Na_2SO_4}=\dfrac{0,1}{0,5}=0,2M\end{matrix}\right.\)
b
\(Ca\left(OH\right)_2+H_2SO_4\rightarrow CaSO_4+2H_2O\)
0,35<---------0,35
\(V_{Ca\left(OH\right)_2}=\dfrac{0,35.74}{1,2}=\dfrac{259}{12}\approx21,58\left(ml\right)\\ \Rightarrow V_{dd.Ca\left(OH\right)_2}=\dfrac{\dfrac{259}{12}.100\%}{10\%}=\dfrac{1295}{6}\approx215,83\left(ml\right)\)

Câu 1
Ta có \(n_{NaOH}=0,06\left(mol\right)\)
\(n_{H_3PO_4}=0,05\left(mol\right)\)
PT \(NaOH+H_3PO_4\rightarrow NaH_2PO_4+H_2O\) (1)
Ta thấy \(n_{NaOH}>n_{H_3PO_4}\Rightarrow n_{NaOH\left(pu\right)}=n_{H_3PO_4}=0,05\left(mol\right)\)
\(\Rightarrow n_{NaOH\left(du\right)}=0,06-0,05=0,01\left(mol\right)\)
\(NaOH_{\left(du\right)}+NaH_2PO_4\rightarrow Na_2HPO_4+H_2O\) (2)
Ta có chất sau phản ứng gồm \(NaH_2PO_4;Na_2HPO_4\)
Theo (1) \(n_{NaH_2PO_4}=n_{H_3PO_4}=0,05\left(mol\right)\)
Theo (2) \(n_{NaH_2PO_4\left(pu\right)}=n_{NaOH\left(du\right)}=0,01\left(mol\right)\)
\(\Rightarrow n_{NaH_2PO_4\left(du\right)}=0,05-0,01=0,04\left(mol\right)\)
\(n_{Na_2HPO_4}=0,01\left(mol\right)\)
Thể tích dd sau phản ứng là
\(V_{dd}=200+250=450\left(ml\right)=0,45\left(l\right)\)
\(C_M\left(NaH_2PO_4\right)=\dfrac{4}{45}M\)
\(C_M\left(Na_2HPO_4\right)=\dfrac{1}{45}M\)
Câu 2
Ta có \(m_{KOH}=33,6\left(g\right)\Rightarrow n_{KOH}=0,6\left(mol\right)\)
\(m_{H_2SO_4}=49\left(g\right)\Rightarrow n_{H_2SO_4}=0,5\left(mol\right)\)
\(KOH+H_2SO_4\rightarrow KHSO_4+H_2O\) (1)
\(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\) (2)
Ta thấy ở (2) \(n_{KOH}< n_{H_2SO_4}=\dfrac{0,6}{2}< \dfrac{0,5}{1}\)

Đặt nồng độ HCl trong dung dịch A là x
Đặt nồng độ Ba(OH)2 trong dung dịch B là y
- Khi trộn 50ml dung dịch A với 50ml dung dịch B thì HCl dư, ta có:
2HCl + Ba(OH)2 → BaCl2 + 2H2O (1)
0,1y← 0,05y mol
HCl + NaOH → NaCl + H2O (2)
0,005←0,005 mol
Ta có: 2.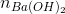 + nNaOH = nHCl
+ nNaOH = nHCl
0,1y + 0,005 = 0,05x
x– 2y = 0,1 (*)
- Khi trộn 50 ml dung dịch A với 150ml thì Ba(OH)2 dư, ta có:
2HCl + Ba(OH)2 → BaCl2 + 2H2O (3)
0,05x→0,025x mol
2HNO3 + Ba(OH)2 → Ba(NO3)2 + H2O (4)
0,035→ 0,0175 mol
Ta có: 2.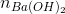 = (nHCl +
= (nHCl + 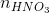 )
)
0,15y = 0,025x + 0,0175
x– 6y = - 0,7 (**)
Giải hệ pt:
x– 6y = -0,7
x– 2y = 0,1
=>x = 0,5; y= 0,2
=>CM của HCl = 0,5M
CM của Ba(OH)2 = 0,2M