Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Lâu lắm rồi mới ngoi lên lại với cuộc thi và tiêu chí mới, trong kì thi lần này không biết là các bạn có muốn lồng ghép thêm 1 chút kiến thức Sinh học vào không ta?
Mng ơi, các bạn có thể đóng góp cho mình về các hình thức thi cũng như đề hay nha :3

Quy đổi hh thành Fe và O
Đặt nFe=a(mol);nO=b(mol); nSo2=c(mol).
=> \(56a+16b=69.6\)(1)
Bảo toàn e => \(3a-2b-2c=0\)(2)
Kết tủa Fe(OH)3: \(n_{Fe\left(OH\right)_3}=0.7\left(mol\right)\)
=> \(n_{H^+_{\left(du\right)}}=1,55.2-0,7.3=1\left(mol\right)\)
=> \(n_{H_2SO_4\left(pu\right)}=2-0,5=1,5\left(mol\right)\)
=> \(b+2c=1,5\) (3)
Từ (1)(2) (3)
=> \(\left\{{}\begin{matrix}a=0,9\left(mol\right)\\b=1,2\left(mol\right)\\c=0,15\left(mol\right)\end{matrix}\right.\)=> \(V=3,36\left(l\right)\)
Quy đổi hỗn hợp ban đầu về a mol Fe; b mol O.
\(\Rightarrow56a+16b=69,6\left(1\right)\)
TN1: Cho hỗn hợp td H2SO4
\(n_{H_2SO_4}=2\left(mol\right)\)
QT nhường e: Fe -----> Fe+3 + 3e
____________a\(_{\rightarrow}\)______________3a
QT nhận e: O + 2e ------> O-2
__________b\(_{\rightarrow}\)__2b
S+6 + 2e -----> S+4
______3a+2b____\(_{\leftarrow}\frac{3a+2b}{2}\)
TN2: Cho Y td NaOH
Sau pứ ta có Fe(OH)3 ; Fe2(SO4)3(dư); Na2SO4
\(n_{NaOH}=3,1\left(mol\right);n_{Fe\left(OH\right)_3}=0,7\left(mol\right)\\ BTNT.Na\Rightarrow n_{Na_2SO_4}=\frac{1}{2}n_{NaOH}=1,55\left(mol\right)\\ BTNT.Fe\Rightarrow n_{Fe}=2n_{Fe_2\left(SO_4\right)_3\left(du\right)}+n_{Fe\left(OH\right)_3}\\ \Rightarrow n_{Fe_2\left(SO_4\right)_3\left(du\right)}=\frac{a-0,7}{2}\left(mol\right)\\ \\ BTNT.S\Rightarrow n_{H_2SO_4}=3n_{Fe_2\left(SO_4\right)_3\left(du\right)}+n_{SO_2}+n_{Na_2SO_4}\\ \Rightarrow2=1,5\left(a-0,7\right)+\frac{3a-2b}{2}+1,55\left(2\right)\)
(1) và (2) => \(\left\{{}\begin{matrix}a=0,9\\b=1,2\end{matrix}\right.\)
\(\Rightarrow n_{SO_2}=0,15\left(mol\right)\Rightarrow V=3,36\left(l\right)\)

Theo anh thì 1,3,4 co tác dụng với nhau nên k cùng tồn tại trong 1 dung dịch nhưng không có đáp án đó.

Hai lí do chính :
Trong lòng biển và đại dương tồn tại cân bằng hoá học :
![]()
Theo nguyên lí chuyển dịch cân bằng, khi nồng độ cacbon đioxit tăng thì cân bằng hoá học chuyển theo chiều thuận, do đó làm giảm nồng độ của cacbon đioxit.
- Sự quang hợp của cây xanh trên lục địa và của tảo ở biển và các đại dương :
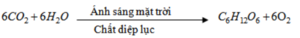
Dù cho có những quá trình tự điều tiết, khống chế sự tăng cacbon đioxit, nhưng con người đang thải lượng cacbon đioxit ngày càng nhiều hơn, vượt quá khả năng tự điều chỉnh của thiên nhiên.

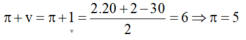
Các bạn chú ý bảng của mình ở mục nhận xét chấm thi của vòng 1 nhé!
Lên rồi nhé :))
Okla :3
:3
Thiệt sự là nhìn cách giải bài 5 k hiểu gì :))
Anh ơi sao mấy cuộc thi khác có chỗ xem bài làm mà công thêm nhận xét nữa?
Vì mấy cuộc thi đó đã kết thúc nên xem được bải làm
Còn nhận xét thi khi nào em xem được bài làm rồi, cũng sẽ xem được nhận xét trong bài làm đó nhé
Nguyễn Nhật Minh ok anh
Ơ hơ hơ... mới vào thấy cái thông báo này. Bị loại từ vòng 1 thật luôn rồi kìa :((
Cái chỗ cuối là sao anh Toshiro Kiyoshi, như vậy hả a?
\(Q\rightarrow F+I\rightarrow K\underrightarrow{+Q}L\)
Vầy làm thử đề chung vòng 2 đi ''anh'' eyyy =))
\(F+I-->K+Q\)
Hạ điểm đề chung xuống 15 điểm
Mở rộng thời gian thi tới 0h00 ngày 6/4
Ai biểu onl muộn
Còn Q thì ra F + I?
Toshiro Kiyoshi
Hùng Nguyễn Phản ứng thuận nghịch
Gần 9h rồi mà vẫn chưa ai nạp nhỉ???
@Nguyễn Thị Ngọc Thơ nói vậy thôi chứ biết gì đâu mà làm
Tiếp tục mở vòng thi đến 0h00 ngày 9/4
Cứ khiêm tốn anh eyyy :))
ui
=)) Tao biết ngay mà.
Toshiro Kiyoshi hết mai?
Hùng Nguyễn Ủa chưa lộp à?
17/4/2020 be like =_=
À t phát hiện m sai thời gian nha, 2019 gì cha -.-
Bỏ đề thi chung mở vòng thi đến 0h00 ngày 12/04/2019