Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nFe = \(\frac{5,6}{56}\) = 0,1 mol
nCu =\(\frac{3,2}{64}\) = 0,05 mol
nHNO3 = 0,5 . 0,2 = 0,1 mol
nHCl = 0,5 . 0,8 = 0,4 mol
nH+ = nHNO3 + nHCl = 0,5 mol
nCl- = nHCl = 0,4 mol
\(Fe,Cu\underrightarrow{+H^+,NO3^-,Cl^-}Fe^{2+},Cu^{2+},H^+Cl^-\underrightarrow{+Ag^+,NO3^-}\left\{{}\begin{matrix}Fe^{3+},Cu^{2+}\\Ag,AgCl\end{matrix}\right.\)
Fe0 → Fe+3 + 3e.....................4H+ + NO3- + 3e → NO + H2O
0,1________0,3......................0,5__________0,375
Cu0 → Cu+2 + 2e......................................Ag+ + 1e → Ag
0,05_________0,1..............................................x___x
BT e: 0,3 + 0,1 = 0,375 + x
→ x = 0,025
Ag+ + Cl- → AgCl
______0,4____0,4
m↓ = mAg + mAgCl
= 0,025 . 108 + 0,4 . 143,5
= 60,1 (g)

Xét 100g phân bón có 40g P O
Bảo toàn P:\(\frac{nP}{Ca\left(H2PO4\right)2}\) = \(\frac{nP}{P2O5}\)
⇒ mCa(H2PO4)2 = 65, 92 g ⇒ %mCa(H2PO4)2 = 65, 92

- Xét phản ứng giữa OH- và H+:
pH = 13 > 7 → Bazo còn dư
→ pOH = 14 - 13 = 1 → [OH-] = 0,1 M
→ nOH- dư = 0,1.0,5 = 0,05 mol
nH+ = nHCl + nHNO3 = 0,04 + 0,06 = 0,1 mol
PT ion: H+ + OH- → H2O
Bđ:___0,1___x
Pư:___0,1___0,1
Sau:___0___x-0,1
→ nOH- dư = x - 0,1 = 0,05 → x = 0,15 mol
- Xét phản ứng của X với H2O dư:
2X + 2nH2O → 2X(OH)n + nH2 → nOH- = 2nH2
X2On + nH2O → 2X(OH)n → nOH- = 2nO
Vậy nOH- = 2nH2 + 2nO → 0,15 = 2.0,015 + 2.nO
→ nO = 0,06
→ mO = 0,06.16 = 0,96 gam
Do O chiếm 10% hỗn hợp → m = 9,6 gam

hai cách làm tăng hiệu suất:
- dùng dư axit acetic: làm phản ứng về phía tạo sản phẩm nhiều hơn theo nguyên tắc chuyển dịch cân bằng của le chatelier.
- liên tục tách nước sinh ra: nước là sản phẩm, nếu loại bỏ nước ngay khi phản ứng xảy ra, cân bằng dịch chuyển về phía tạo isoamyl acetate, tăng hiệu suất.

nNaHCO3= 0,2 mol⇒ nHCO3= 0,2 mol
nK2CO3= 0,2 mol⇒ nCO3= 0,2 mol
nH2SO4= 0,1 mol
nHCl= 0,1 mol
⇒∑nH+= 0,1.2+0,1=0,3 mol
PT:\(CO3^{2-}+H^+\rightarrow HCO3^-\)
____0,2____0,2______0,2
\(HCO3^-+H^+\rightarrow CO2+H2O\)
0,1______________0,1__0,1
⇒nHCO3= 0,2+0,2- 0,1= 0,3 mol
Cho Ba(OH)2 dư:
\(HCO3^-+OH^-\rightarrow CO3^{2-}+H2O\)
0,3____________________0,3
⇒m kết tuả= mBaCO3= 0, 3.197=59,1 g
VCO2 = 0,1.22,4= 2,24 l

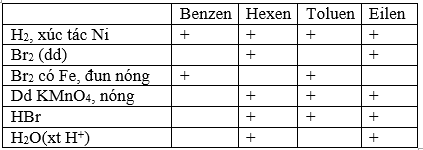
- Phản ứng thế là phản ứng trong đó nguyên tử hoặc nhóm nguyên tử trong phân tử chất hữu cơ bị thay thế bởi một nguyên tử hoặc nhóm nguyên tử khác
Ví dụ: CH4 + Cl2 –ánh sáng–> CH3Cl + HCl
- Phản ứng cộng là phản ứng trong đó phân tử chất hữu cơ kết hợp với phân tử khác tạo thành phân tử hợp chất mới
Ví dụ: C2H4 + Br2 –> C2H4Br2
- Phản ứng tách là phản ứng trong đó hai hay nhiều nguyên tử bị tách ra khỏi phân tử hợp chất hữu cơ
Ví dụ: C2H6 —xt-tº→ C2H4 + H2
- Phản ứng thế là phản ứng trong đó nguyên tử hoặc nhóm nguyên tử trong phân tử chất hữu cơ bị thay thế bởi một nguyên tử hoặc nhóm nguyên tử khác
Ví dụ: CH4 + Cl2 –ánh sáng–> CH3Cl + HCl
- Phản ứng cộng là phản ứng trong đó phân tử chất hữu cơ kết hợp với phân tử khác tạo thành phân tử hợp chất mới
Ví dụ: C2H4 + Br2 –> C2H4Br2
- Phản ứng tách là phản ứng trong đó hai hay nhiều nguyên tử bị tách ra khỏi phân tử hợp chất hữu cơ
Ví dụ: C2H6 —xt-tº\(\rightarrow\) C2H4 + H2
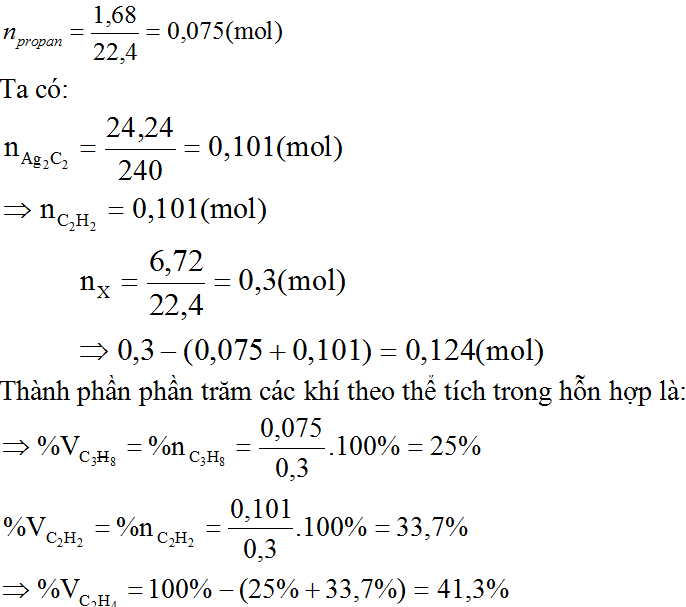

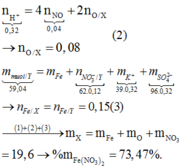
Fe_______________________Fe2+
Fe3O4______NaHSO4 0,32 \(\rightarrow\)Fe3+_______+NO 0,04 +H2O
Fe(NO3)2 ________________Na+ 0,32
_________________________SO42- 0,32
_________________________NO3-
_________________________53,92g
Theo bảo toàn H: nNaHSO4=2nH2O=0,32
\(\rightarrow\)nH2O=0,16
Theo bảo toàn khối lượng
m+mNaHSO4=m muối+mNO+mH2O
\(\rightarrow\)m+0,32.120=53,92+0,04.30+0,16.18
\(\rightarrow\)m=19,6