Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Lực đẩy của nước tác dụng vào hai thỏi tính bằng công thức:
F1 = d.V1; F2 = d.V2 (trong đó d là trọng lượng riêng của nước, V1 là thể tích của thỏi nhôm, V2 là thể tích của thỏi đồng)
Vì hai thỏi có trọng lượng như nhau: P1 = P2 và trọng lượng riêng của đồng lớn hơn của nhôm d1 < d2 nên V1 > V2, do đó F1 > F2.
Vậy cân sẽ không cân bằng nữa khi nhúng ngập cả hai thỏi đồng thời vào hai bình đựng nước.
F1 = d.V1; F2 = d.V2 (trong đó d là trọng lượng riêng của nước, V1 là thể tích của thỏi nhôm, V2 là thể tích của thỏi đồng)
Vì hai thỏi có trọng lượng như nhau: P1 = P2 và trọng lượng riêng của đồng lớn hơn của nhôm d1 < d2 nên V1 > V2, do đó F1 > F2.
Vậy cân sẽ không cân bằng nữa khi nhúng ngập cả hai thỏi đồng thời vào hai bình đựng nước.

CuO: copper(II) oxide K₂O: potassium oxide P₂O₅: diphosphorus pentoxide NO: nitrogen monoxide
CuO: copper(II) oxide. K2O: potassium oxide. P2O5: diphosphorus pentoxide. NO: nitrogen monoxide.

P=> 1→1 P2O5 2→2 + H3PO4
H3PO4 3→
=> Na3PO4 4→
+ Ca3(PO4)2
(1) 4P + 5O2 ��→to 2P2O5
(2) P2O5 + 3H2O → 2H3PO4
(3) H3PO4 + NaOH → Na3PO4 + H2O
(4) 2Na3PO4 + 3CaCl2 → 6NaCl + Ca3(PO4)2

1. Đồng hydroxit
2 . Nitrous Oxide
3 . Barium Sulfate
4. Hydro Sulfide

nO2=a;nN2=4a��2=�;��2=4�
PTHH: 2SO2+O2V2O5⟷2SO32��2+�2⟷�2�52��3
Bđ: a� a�
Pư: 2x2� x� 2x2�
Sau: a−2x�−2� a−x�−� 2x2�
Bảo toàn khối lượng: mA=mB⇒nA.
Không khí: 5a mol → O₂ = a mol, N₂ = 4a mol.
PTHH: 2SO₂ + O₂ → 2SO₃.
Gọi x mol SO₂ phản ứng.
Số mol:
- Hỗn hợp A: 6a
- Hỗn hợp B: 6a − x/2
Khối lượng không đổi: m = 208a.
dA/dB = MA/MB
= (208a/6a) / (208a/(6a − x/2))
= (6a − x/2) / 6a
= 0,93
⇒ x = 0,84a
Hiệu suất:
H = x/a × 100% = 84%

Phương trình: \text{Zn} + \text{H}_{2}\text{SO}_{4} \rightarrow \text{ZnSO}_{4} + \text{H}_{2} \uparrow. Số mol các chất: n_{\text{Zn}} = \frac{19,5}{65} = 0,3 \text{ mol}. m_{\text{H}_{2}\text{SO}_{4}} = \frac{200 \cdot 24,5\%}{100\%} = 49 \text{ g} \Rightarrow n_{\text{H}_{2}\text{SO}_{4}} = \frac{49}{98} = 0,5 \text{ mol}. Biện luận: Vì 0,3 < 0,5 nên \text{Zn} hết, \text{H}_{2}\text{SO}_{4} dư. Tính toán sau phản ứng: n_{\text{H}_{2}\text{SO}_{4} \text{ pư}} = n_{\text{ZnSO}_{4}} = n_{\text{H}_{2}} = 0,3 \text{ mol}. m_{\text{H}_{2}\text{SO}_{4} \text{ dư}} = 49 - (0,3 \cdot 98) = 19,6 \text{ g}. m_{\text{ZnSO}_{4}} = 0,3 \cdot 161 = 48,3 \text{ g}. Khối lượng dung dịch sau phản ứng: m_{\text{dd}} = m_{\text{Zn}} + m_{\text{dd } \text{H}_{2}\text{SO}_{4}} - m_{\text{H}_{2}} = 19,5 + 200 - (0,3 \cdot 2) = 218,9 \text{ g}. Nồng độ phần trăm (C\%): C\%_{\text{ZnSO}_{4}} = \frac{48,3}{218,9} \cdot 100\% \approx 22,06\%. C\%_{\text{H}_{2}\text{SO}_{4} \text{ dư}} = \frac{19,6}{218,9} \cdot 100\% \approx 8,95\%.
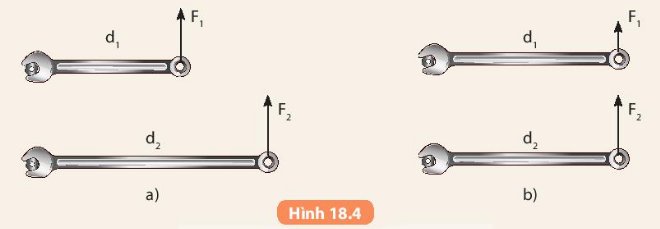


- Ở hình 18.4 a moment của lực F2 lớn hơn moment của lực F1
Do F1 = F2 nhưng giá của lực F2 cách xa trục quay hơn lực F1 nên tác dụng làm quay của lực F2 lớn hơn.
- Ở hình 18.4 b moment của lực F2 lớn hơn moment của lực F1
Do giá của lực F2 cách trục quay bằng giá của lực F1 cách trục quay nhưng F2 > F1 nên tác dụng làm quay của lực F2 lớn hơn.