Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : C
Vì ngâm lá sắt vào dung dịch sau điện phân thấy khối lượng tăng => chứng tỏ Cu2+ còn dư
Catot : Cu2+ + 2e -> Cu
Anot : 2H2O -> 4H+ + O2 + 4e
,nO2 = 0,05 mol
=> 4nO2 = 2nCu2+ đp => nCu2+ đp = 0,1 mol
Fe + 2H+ -> Fe2+ + H2
0,1 <- 0,2 mol
Fe + Cu2+ -> Fe2+ + Cu
,x -> x -> x
=> mtăng = 64x – 56(x + 0,1) = 0,8g
=> x = 0,8 mol
=> nCuSO4 bđ = 0,1 + 0,8 = 0,9 mol
=> CM(CuSO4) = 1,8M

Đáp án B
Fe + Cu2+ → Fe2+ + Cu
Mol x → x
=> DmThanh KL(tăng) = mCu – mFe pứ = 64x – 56x = 1,6
=> x = 0,2 mol => nCuSO4 = nCu = 0,2 mol
=> CM(CuSO4) = 0,2 : 0,1 = 2M

Chọn đáp án A.
Dung dịch sau điện phân + Al. 0,075 mol H2
=> Chứng tỏ có phản ứng điện phân nước.
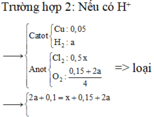
· Trường hợp 1: Dung dịch sau điện phân chứa H+.
n H + = 2 n H 2 = 0 , 15 m o l
Phương trình điện phân:
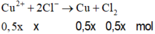

=> Loại (vì n C u = 0 , 05 < 0 , 075 + 0 , 5 x )
· Trường hợp 2: Dung dịch sau điện phân chứa OH-.
n O H - = 2 3 n H 2 = 0 , 05 m o l
Phương trình điện phân:


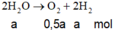
⇒ a = 0 , 025
=> Thời gian điện phân:
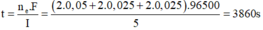

Đáp án B
Ở anot thu được hỗn hợp khí gồm Cl2 và O2, dựa vào tỉ khối ta có tỉ lệ số mol 2 khí này là 6:1.
Gọi số mol O2 là x mol suy ra số mol Cl2 là 6x.
Ở catot thu được Cu 8x mol.
Khối lượng dung dịch giảm là do O2, Cu, Cl2 thoát ra → 32x+64.8x+71.6x = 29,1
Giải được: x=0,03
→ b = 6x.2 = 0,36
Khối lượng kim loại Cu bàm vào catot là 158,36 gam.
Cho Ba(OH)2 dư vào dung dịch sau điện phân kết tủa thu được gồm a mol BaSO4 và a-0,24 mol Cu(OH)2.
→ 233a + (a - 0,24).98 = 135,36
Giải được a=0,48.
Khối lượng chất tan trong X là 97,86 gam.
4,68 gam hỗn hợp Al và Mg có tỉ lệ số mol 2:1 gồm có 0,12 mol Al và 0,06 mol Mg.
Ta có: 0,12.3+0,06.2 = 0,18.2+0,03.4 nên lượng khí oxi hóa vừa đủ.
Điện phân X trong 20072 giây tức số mol e là 1,04 mol.
Ở catot thu được Cu 0,48 mol và H2 0,04 mol.
Ở anot thu được Cl2 0,18 mol và O2 0,17 mol.
Tổng số mol khí thoát ra là 0,39 mol


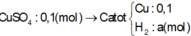
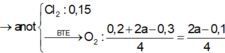
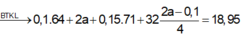






Đáp án của em như thế là hoàn toàn đúng