Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các yếu tố ảnh hưởng đến tốc độ phản ứng trong mỗi trường hợp đã cho là : Giảm nồng độ chất tham gia phản ứng (khí oxi) làm giảm tốc độ phản ứng.

Các yếu tố ảnh hưởng đến tốc độ phản ứng trong mỗi trường hợp đã cho là : Giảm kích thước hạt để tăng tốc độ phản ứng.

Các yếu tố ảnh hưởng đến tốc độ phản ứng trong mỗi trường hợp đã cho là : V 2 O 5 là chất xúc tác, làm tăng tốc độ phản ứng.

Các yếu tố ảnh hưởng đến tốc độ phản ứng trong mỗi trường hợp đã cho là : Tăng nồng độ chất tham gia phản ứng (khí oxi) làm tăng tốc độ phản ứng.

Chọn đáp án C
Na2S2O3 (l) + H2SO4 (l) → Na2SO4 (l) + SO2 (k) +S (r)+H2O (l).
V=k[ Na 2 S 2 O 3 ][ H 2 SO 4 ]
Khi thay đổi một trong các yếu tố (giữ nguyên các yếu tố khác):
(1) Tăng nhiệt độ. Làm tăng tốc độ phản ứng
(2) Tăng nồng độ Na2S2O3. Làm tăng tốc độ phản ứng
(3) Giảm nồng độ H2SO4. Làm giảm tốc độ phản ứng
(4) Giảm nồng độ Na2SO4. Không ảnh hưởng tới tốc độ phản ứng
(5) Giảm áp suất của SO2. Không ảnh hưởng tới tốc độ phản ứng

A. Bất cứ phản ứng nào cũng chỉ vận dụng được một trong các yếu tố ảnh hưởng đến tóc độ phản ứng để tăng tốc độ phản ứng.
B. Bất cứ phản ứng nào cũng phải vận dụng đủ các yếu tố ảnh hưởng đến tốc độ phản ứng mới tăng được tốc độ phản ứng.
C. Tùy theo phản ứng mà vận dụng một, một số hay tất cả các yêu tố ảnh hưởng đến tốc độ phản ứng để tăng tốc độ phản ứng.
D. Bất cứ phản ứng nào cũng cần chất xúc tác để tăng tốc độ phản ứng.

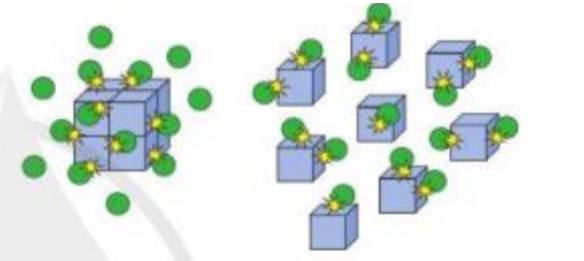
- Hình thứ nhất mô tả: chất tham gia ở dạng khối lớn
- Hình thứ hai mô tả: chất tham gia được chia nhỏ ra
=> Tăng diện tích tiếp xúc bề mặt giữa các chất tham gia
=> Hình ảnh mô tả ảnh hưởng của diện tích bề mặt đến tốc độ phản ứng
1. Nồng độ
Ảnh hưởng: Khi tăng nồng độ chất phản ứng, tốc độ phản ứng thường tăng.
Giải thích: Nồng độ cao làm tăng số lượng phân tử trong một đơn vị thể tích, dẫn đến tần suất va chạm có hiệu quả giữa các hạt tăng lên, từ đó làm tăng tốc độ phản ứng.
2. Nhiệt độ
Ảnh hưởng: Khi tăng nhiệt độ, tốc độ phản ứng tăng.
Giải thích: Nhiệt độ cao cung cấp năng lượng cho các phân tử, làm chúng chuyển động nhanh hơn. Điều này không chỉ tăng tần suất va chạm mà quan trọng hơn là làm tăng số phân tử có đủ năng lượng hoạt hóa để phản ứng xảy ra.
3. Áp suất (đối với chất khí)
Ảnh hưởng: Khi tăng áp suất của hệ có chất khí tham gia, tốc độ phản ứng tăng.
Giải thích: Tăng áp suất thực chất là làm thu hẹp khoảng cách giữa các phân tử khí (tương đương với việc tăng nồng độ), làm tăng mật độ hạt và số va chạm có hiệu quả.
4. Diện tích bề mặt tiếp xúc (đối với chất rắn)
Ảnh hưởng: Khi tăng diện tích bề mặt tiếp xúc (chia nhỏ, nghiền mịn chất rắn), tốc độ phản ứng tăng
Giải thích: Bề mặt tiếp xúc càng lớn thì số lượng phân tử ở lớp bề mặt có khả năng va chạm với các phân tử của chất khác càng nhiều, dẫn đến số va chạm hiệu quả tăng.
5. Chất xúc tác
Ảnh hưởng: Chất xúc tác làm tăng tốc độ phản ứng nhưng không bị tiêu hao sau phản ứng.
Giải thích: Chất xúc tác hoạt động bằng cách tạo ra một lộ trình phản ứng mới có năng lượng hoạt hóa thấp hơn, giúp nhiều phân tử có thể vượt qua rào cản năng lượng để phản ứng dễ dàng hơn.
1. Nồng độ chất phản ứng Ảnh hưởng: Nồng độ tăng → tốc độ phản ứng tăng Nồng độ giảm → tốc độ phản ứng giảm Giải thích: Khi nồng độ cao, số lượng hạt (phân tử, ion) trong một thể tích lớn hơn → va chạm giữa các hạt xảy ra nhiều hơn → phản ứng nhanh hơn. 2. Nhiệt độ Ảnh hưởng: Nhiệt độ tăng → tốc độ phản ứng tăng Nhiệt độ giảm → tốc độ phản ứng giảm Giải thích: Nhiệt độ cao làm các hạt chuyển động nhanh hơn → va chạm mạnh và nhiều hơn → nhiều va chạm đủ năng lượng để xảy ra phản ứng. 3. Diện tích bề mặt (đối với chất rắn) Ảnh hưởng: Diện tích bề mặt tăng → tốc độ phản ứng tăng Giải thích: Chất rắn càng được chia nhỏ (bột mịn) → diện tích tiếp xúc lớn → tăng số lần va chạm với chất khác → phản ứng nhanh hơn. 4. Áp suất (đối với chất khí) Ảnh hưởng: Áp suất tăng → tốc độ phản ứng tăng Giải thích: Áp suất tăng làm các phân tử khí bị nén lại gần nhau hơn → va chạm nhiều hơn → phản ứng nhanh hơn. 5. Chất xúc tác Ảnh hưởng: Làm tăng tốc độ phản ứng (không bị tiêu hao sau phản ứng) Giải thích: Chất xúc tác tạo ra con đường phản ứng mới có năng lượng hoạt hóa thấp hơn → phản ứng xảy ra dễ dàng và nhanh hơn.
1. Nồng độ chất phản ứng - Tăng nồng độ → tốc độ phản ứng tăng: Vì nồng độ tăng làm số hạt vi mô trong một đơn vị thể tích tăng → số va chạm hiệu quả giữa các hạt tăng → tốc độ phản ứng tăng. - VD: Đốt cháy than trong O₂ nguyên chất mãnh liệt hơn trong không khí. *2. Áp suất* - *Tăng áp suất → tốc độ phản ứng tăng*: Chỉ áp dụng với chất khí. Áp suất tăng làm các phân tử khí bị nén lại gần nhau hơn → nồng độ tăng → số va chạm hiệu quả tăng. - VD: Phản ứng tổng hợp NH₃ từ N₂ và H₂ được thực hiện ở áp suất cao. 3. Nhiệt độ - Tăng nhiệt độ → tốc độ phản ứng tăng: Nhiệt độ tăng làm các hạt chuyển động nhanh hơn và số hạt có năng lượng ≥ năng lượng hoạt hóa tăng → số va chạm hiệu quả tăng mạnh. - Quy tắc kinh nghiệm: Tăng 10°C, tốc độ phản ứng tăng 2-4 lần. - VD: Thức ăn để trong tủ lạnh lâu hỏng hơn để ngoài. *4. Diện tích bề mặt tiếp xúc* - *Tăng diện tích tiếp xúc → tốc độ phản ứng tăng*: Áp dụng với chất rắn. Khi nghiền nhỏ, diện tích tiếp xúc với chất phản ứng khác tăng → số va chạm trên bề mặt tăng. - VD: Bột sắt cháy trong O₂, còn đinh sắt thì không. 5. Chất xúc tác - Có xúc tác → tốc độ phản ứng tăng: Chất xúc tác làm giảm năng lượng hoạt hóa của phản ứng → số hạt có đủ năng lượng để phản ứng tăng mạnh mà xúc tác không bị tiêu hao. - VD: MnO₂ xúc tác phản ứng phân hủy H₂O₂. 6. Bản chất của chất phản ứng - Chất phản ứng khác nhau → tốc độ khác nhau: Liên quan đến độ bền liên kết và đặc điểm cấu tạo. Phản ứng ion trong dung dịch thường nhanh, phản ứng cộng hóa trị cần phá vỡ liên kết nên chậm hơn. - VD: Na phản ứng với H₂O nổ mạnh, Mg phản ứng chậm hơn.
Có 5 yếu tố chính ảnh hưởng đến tốc độ phản ứng:
1:Nồng độ: Khi tăng nồng độ chất phản ứng, số va chạm có hiệu quả giữa các phân tử tăng lên \rightarrow Tốc độ phản ứng tăng.
2 Nhiệt độ: Khi tăng nhiệt độ, các phân tử chuyển động nhanh hơn, năng lượng va chạm tăng \rightarrow Tốc độ phản ứng tăng. (Thường tăng 10°C thì tốc độ tăng 2-4 lần).
3 Áp suất (đối với chất khí): Khi tăng áp suất, khoảng cách giữa các phân tử khí giảm lại (tương đương tăng nồng độ) \rightarrow Tốc độ phản ứng tăng.
4Diện tích bề mặt (đối với chất rắn): Khi chia nhỏ chất rắn (nghiền nhỏ, đập vụn), diện tích tiếp xúc giữa các chất phản ứng tăng lên \rightarrow Tốc độ phản ứng tăng.
5Chất xúc tác: Là chất làm giảm năng lượng hoạt hóa của phản ứng nhưng không bị tiêu hao sau phản ứng \rightarrow Tốc độ phản ứng tăng.
Ta có 5 yếu tố ảnh hưởng
1. Nồng độ
Ảnh hưởng: Khi tăng nồng độ chất phản ứng, tốc độ phản ứng thường tăng.
Giải thích: Việc tăng nồng độ làm tăng số lượng hạt (phân tử, ion) trong một đơn vị thể tích, dẫn đến tần suất va chạm có hiệu quả giữa các hạt tăng lên, làm phản ứng xảy ra nhanh hơn.
2. Nhiệt độ
Ảnh hưởng: Khi tăng nhiệt độ, tốc độ phản ứng tăng nhanh.
Giải thích: Ở nhiệt độ cao, các hạt chuyển động nhanh hơn, làm tăng tần suất va chạm. Quan trọng hơn, số lượng hạt có đủ năng lượng hoạt hóa để phản ứng tăng lên đáng kể, giúp phản ứng diễn ra mạnh mẽ hơn.
3. Áp suất
Ảnh hưởng: Khi tăng áp suất của hệ có chất khí tham gia, tốc độ phản ứng tăng.
Giải thích: Tăng áp suất cũng tương đương với việc nén các phân tử khí lại gần nhau hơn , từ đó làm tăng số lượng va chạm có hiệu quả giữa các phân tử.
4. Diện tích bề mặt tiếp xúc
Ảnh hưởng: Khi tăng diện tích bề mặt , tốc độ phản ứng tăng.
Giải thích: Diện tích tiếp xúc càng lớn thì số lượng hạt trên bề mặt có khả năng va chạm với chất phản ứng khác càng nhiều, dẫn đến tốc độ phản ứng tăng lên.
5. Chất xúc tác
Ảnh hưởng: Chất xúc tác làm tăng tốc độ phản ứng nhưng không bị tiêu hao sau phản ứng.
Giải thích: Chất xúc tác hoạt động bằng cách làm giảm năng lượng hoạt hóa cần thiết để phản ứng xảy ra và phản ứng với nhau nhanh hơn.
Tốc độ phản ứng hóa học phụ thuộc vào tần suất va chạm hiệu quả giữa các phân tử chất phản ứng. Dưới đây là 5 yếu tố chính: 1. Nồng độ Giải thích: Khi tăng nồng độ chất phản ứng, số lượng hạt trong một đơn vị thể tích tăng lên, dẫn đến tần suất va chạm giữa các hạt tăng, làm tăng tốc độ phản ứng. 2. Nhiệt độ Giải thích: Khi tăng nhiệt độ, các hạt chuyển động nhanh hơn (động năng tăng) và số lượng hạt có năng lượng đủ lớn để vượt qua rào cản năng lượng hoạt hóa tăng lên. Điều này làm tăng tốc độ phản ứng. 3. Áp suất (Đối với chất khí) Giải thích: Tăng áp suất tương đương với việc nén các phân tử khí lại gần nhau hơn (tăng nồng độ chất khí), làm tăng tần suất va chạm và tăng tốc độ phản ứng. 4. Diện tích bề mặt tiếp xúc (Đối với chất rắn) Giải thích: Khi chia nhỏ chất rắn (nghiền bột, chẻ nhỏ), diện tích bề mặt tiếp xúc giữa các chất phản ứng tăng lên, tạo ra nhiều vị trí va chạm hơn, làm tăng tốc độ phản ứng. 5. Chất xúc tác Giải thích: Chất xúc tác làm giảm năng lượng hoạt hóa của phản ứng, giúp phản ứng xảy ra dễ dàng hơn mà không bị tiêu hao sau phản ứng. Yếu tố này làm tăng tốc độ phản ứng.
Nồng độ: Khi tăng nồng độ chất phản ứng, số lượng phân tử trong một đơn vị thể tích tăng lên, dẫn đến tần số va chạm hiệu quả giữa các phân tử tăng, làm tăng tốc độ phản ứng. Nhiệt độ: Tăng nhiệt độ làm cho các phân tử chuyển động nhanh hơn và có năng lượng cao hơn, dẫn đến tần số va chạm và số lượng va chạm hiệu quả đều tăng, từ đó tăng tốc độ phản ứng. Áp suất: Đối với các phản ứng có chất khí tham gia, tăng áp suất tương đương với việc giảm thể tích, làm tăng nồng độ chất khí, dẫn đến tăng tốc độ phản ứng. Diện tích bề mặt: Khi chia nhỏ chất phản ứng rắn, diện tích bề mặt tiếp xúc tăng lên, giúp các phân tử của các chất khác dễ dàng va chạm với nhau hơn, làm tăng tốc độ phản ứng. Chất xúc tác: Chất xúc tác làm giảm năng lượng hoạt hóa của phản ứng, giúp phản ứng diễn ra nhanh hơn mà không bị tiêu hao sau phản ứng.
1. Nồng độ - Ảnh hưởng: khi tăng nồng độ chất phản ứng tốc độ phản ứng thường tăng - vì nồng độ làm tăng số lượng phân tử trong một đơn vị thế tích dẫn đến tần xuất va chạm có hiệu quả giữa các hạt tăng lên từ đó làm tăng tốc độ phản ứng 2. Nhiệt độ - Ảnh hưởng: khi tăng nhiệt độ tốc độ phản ứng tăng - Vì nhiệt độ cao cung cấp năng lượng cho các phân tử làm chúng chuyến động nhanh hơn điều này không chỉ tăng tần suất va chạm mà quan trọng hơn là làm tăng số phân tử có đủ năng lượng hoạt hóa để phản ứng xảy ra 3. Áp suất - Ảnh hưởng: khi tăng áp suất của hệ có chất khí tham gia tốc độ phản ứng tăng - Vì tăng áp suất thực chất là làm thu hẹp khoảng cách giữa các phân tử khí làm tăng một độ hạt và số va chạm có hiệu quả 4. Diện tích bề mặt tiếp xúc - Ảnh hưởng: khi tăng diện tích bề mặt tiếp xúc tốc độ phản ứng tăng - Vì bề mặt tiếp xúc càng lớn thì số lượng phân tử ở lớp bề mặt có khả năng va chạm với các phân tử của chất khác càng nhiều dẫn đến số va chạm hiệu quả tăng
5. Chất xúc tác - Ảnh hưởng: chất xúc tác làm tăng tốc độ phản ứng nhưng không bị tiêu hao sau phản ứng - Vì chất xúc tác hoạt động bằng cách tạo ra một lộ trình phản ứng có năng năng lượng hoạt hóa thấp hơn giúp nhiều phân tử có thể vượt qua rào cản năng lượng để phản ứng dễ dàng hơn
Nồng độ chất phản ứng
Tăng nồng độ → tốc độ phản ứng tăng. Vì nồng độ cao làm tăng số phân tử chất phản ứng trong 1 đơn vị thể tích, dẫn đến số va chạm hiệu quả giữa các phân tử tăng → phản ứng nhanh hơn.
VD: Than cháy trong oxi nguyên chất mãnh liệt hơn trong không khí.
Nhiệt độ
Tăng nhiệt độ → tốc độ phản ứng tăng. Khi nhiệt độ tăng, các phân tử chuyển động nhanh hơn và có năng lượng lớn hơn. Số phân tử có năng lượng ≥ năng lượng hoạt hóa tăng lên → số va chạm hiệu quả tăng mạnh.
Quy tắc: Cứ tăng 10°C thì tốc độ phản ứng tăng 2-4 lần.
Áp suất - chỉ áp dụng với phản ứng có chất khí
Tăng áp suất → tốc độ phản ứng tăng. Áp suất tăng làm giảm thể tích, tăng mật độ phân tử khí → số va chạm giữa các phân tử khí tăng → phản ứng nhanh hơn.
Diện tích bề mặt tiếp xúc - với phản ứng có chất rắn
Diện tích tiếp xúc càng lớn → tốc độ càng nhanh. Nghiền nhỏ chất rắn làm tăng bề mặt tiếp xúc với chất khác → tăng số va chạm trên bề mặt.
VD: Bột sắt cháy trong oxi nhanh hơn đinh sắt.
Chất xúc tác
Chất xúc tác làm tăng tốc độ phản ứng. Vì xúc tác làm giảm năng lượng hoạt hóa, tạo ra con đường phản ứng mới dễ xảy ra hơn. Xúc tác không bị tiêu hao sau phản ứng.
Chất ức chế thì ngược lại, làm giảm tốc độ.
Bản chất của chất phản ứng
Chất có liên kết kém bền, dễ phá vỡ thì phản ứng nhanh hơn. Phản ứng giữa các ion trong dung dịch xảy ra gần như tức thời, nhanh hơn phản ứng giữa các phân tử cộng hóa trị.
Mẹo nhớ: "Nồng - Nhiệt - Áp - Diện - Xúc - Bản". Cần mình rút gọn lại thành 3-4 dòng cho dễ chép không?