Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(1/\\ Tổng: 2p+n=49(1)\\ \text{Hạt không mang điện bằng 53,125% số hạt mang điện: }\\ n=2.53,125\%p\\ \to -1,0625p-n=0(2)\\ (1)(2)\\ p=e=16\\ n=17\\ A=16+17=33 (S)\\ \)
\(Tổng: 2p+n=36(1)\\ \text{Số hạt mang điện gấp đôi số hạt không mang điện là 36: }\\ 2p=2n\\ \to p-n=0(2)\\ (1)(2)\\ p=e=n=12\\ A=12+12=24(Mg)\)

a) Ta có : \(\left\{{}\begin{matrix}2Z=18\\2Z=2N\end{matrix}\right.\)
=> Z=N=9
Vậy X là Flo (F)
b) Ta có : \(\left\{{}\begin{matrix}2Z+N=156\\2Z-N=32\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}Z=47=P=E\\N=62\end{matrix}\right.\)
A=Z+N=47+62=109

Nguyên tử Y:
\(\left\{{}\begin{matrix}P+N+E=82\\P=E\\\left(P+E\right)-N=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+E=82\\2P-N=22\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=26\\N=30\end{matrix}\right.\)
Kí hiệu: \(^{56}_{26}Fe\)
* Nguyên tử X:
\(\left\{{}\begin{matrix}P+N+E=115\\P=E\\P+E=\dfrac{14}{9}N\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=115\\2P-\dfrac{14}{9}N=0\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=35\\N=45\end{matrix}\right.\)
Kí hiệu: \(^{80}_{35}Br\)
1/ Theo đề ta có:\(S=2Z+N=82\)(1)
\(2Z-N=22\)(2)
từ (1) và(2)\(\Rightarrow Z=26;N=30\)
A=Z+N=26+30=56
Vậy kí hiệu nguyên tử Y là\(^{56}_{26}Fe\)
2/Theo đề ta có:\(S=2Z+N=115\)(1)
\(2Z=\dfrac{14}{9}N\Leftrightarrow2Z-\dfrac{14}{9}N=0\)(2)
Từ (1) và (2)\(\Rightarrow Z=35;N=45\)
A=Z+N=35+45=80
Vậy kí hiệu nguyên tử X là \(^{80}_{35}Br\)

Đáp án B.
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố R là 34:
p + e + n = 34 hay 2p + n = 34 (do p = e) (1)
Số hạt mang điện (p và e) gấp 1,833 lần số hạt không mang điện (n)
p + e = 1,833.n hay 2p=1,833n (do p = e) (2)
Giải (1), (2) ta có p = e = 11; n = 12.

Đáp án A
Một nguyên tử R có tổng số hạt mang điện và không mang điện là 34 → 2p + n = 34
số hạt mang điện gấp 1,833 lần số hạt không mang điện → 2p = 1,883.n
Giải hệ → p =11, n = 12 → R là nguyên tố Na
Cấu hình của R là Na, 1s22s22p63s1.

Đáp án A
Theo đề bài ta có hệ ![]()
Vậy R là Na : 1s2 2s2 2p6 3s1 . Đáp án A.
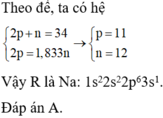
Áp dụng biểu thức điều kiện bền :
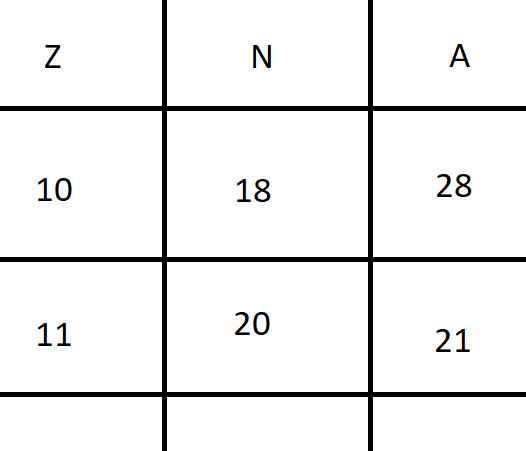
\(\dfrac{S}{3,5}\le Z\le\dfrac{S}{3}\Leftrightarrow\dfrac{34}{3,5}\le Z\le\dfrac{34}{3}\Leftrightarrow9,7\le Z\le11,3\)
\(\Rightarrow Z=10,11\)
\(Z.1,833=N\)
Vậy (1đồng vị) nguyên tử này là Ne , A=21
\(\begin{matrix}21\\10\end{matrix}Ne\)
\(\begin{matrix}21\\11\end{matrix}Na\)

Mình ghi lộn là Ne bạn nha 21Na là 1 đồng vị của Na
biểu thức điều kiện bền ở bài nào vậy bạn
Cái này là gv Hóa mình chỉ mình
hình như bạn làm có gì sai đúng không sao lại có đến 2 cột đáng lẽ chỉ có 1 cột thôi mà
Khi mà nó ra 9,7\(\le\)Z\(\le\)11,3 thì Z có 2 kq nên kẻ bảng loại trừ để lấy 1 kquả
Tùy vào bài mà Z ra nhiều hay ít
của mình ra z = 11 n=12 có 1 kết quả thôi mà bạn xem lại sgk hay gì rùi nói mình đi chứ bạn làm vậy mình không hiểu
của mình ra z = 11 n=12 có 1 kết quả thôi mà bạn xem lại sgk hay gì rùi nói mình đi chứ bạn làm vậy mình không hiểu
của mình ra z = 11 n=12 có 1 kết quả thôi mà bạn xem lại sgk hay gì rùi nói mình đi chứ bạn làm vậy mình không hiểu
của mình ra z = 11 n=12 có 1 kết quả thôi mà bạn xem lại sgk hay gì rùi nói mình đi chứ bạn làm vậy mình không hiểu
bạn có thể làm step by step để nhưng người không học gv hóa của bạn hiểu chứ bạn làm theo cách gv hóa chỉ bạn thì chỉ có những người biết cách này hiểu thôi chứ người bình thường không hiểu bạn làm gì đâu mình nói thật
Trong để có câu "trong đó số hạt mang điện gấp 1.833" nên mình cx hơi rối
thật là mình cũng k biết bạn ghi cái gì luôn ấy chứ @@ nhưng mà bạn thử ghi từng bước ra rồi giải thích step by step thì chắc mình sẽ hiểu đó.mình tin bạn giải thích cách làm của bạn được mà!!
À mình hiểu rồi

mình sai ở khúc gấp 1,833
Mình xin lỗi, mình bị nhầm

Mình sai từ khúc này nha
\(1,833N=2Z\)