Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Nguyên tử heli có 2 proton, mỗi proton mang điện tích dương +1 nên tổng điện tích dương là +2. Phần vỏ có 2 electron, mỗi electron mang điện tích âm – 1, tổng điện tích âm là – 2. Do tổng điện tích dương và âm bằng nhau, tổng điện tích của nguyên tử heli bằng 0 nên nguyên tử heli trung hòa về điện.

Đi từ đầu tới cuối chu kì, hóa trị cao nhất của các nguyên tố với oxi tăng dần từ 1 đến 7; hóa trị cao nhât với hiđro giảm từ 1 đến 4. Ta có thể biểu diễn như sau:
1234567
4321
Vậy nguyên tố Y có hóa trị cao nhất với oxi bằng hóa trị với hiđro thuộc nhóm IV A.
Khi Y kết hợp với Z tạo hợp chất có công thức YZ4 suy ra Z hóa trị I và thuộc nhóm VINA ( vì Z là nguyên tố ko kim loại) nhóm halogen. Khi X kết hợp Z tạo thành hợp chất XZ và phản ứng mãnh liệt. Vậy X hóa trị I và thuộc nhóm IA, nhóm kim loại kiềm. Các nguyên tố này lại phổ biến trong vỏ trái đất này là: Na, Si, Cl

Câu 28:
-Ta luôn có: \(n_{H_2O}=n_{H_2SO_4}=0,5.0,1=0,05mol\)
Âp dụng định luật bảo toàn khối lượng:
moxit+\(m_{H_2SO_4}=\)mmuối+\(m_{H_2O}\)
\(\rightarrow\)2,81+0,05.98=mmuối+0,05.18
\(\rightarrow\)mmuối=2,81+0,05.98-0,05.18=6,81gam
\(\rightarrow\)Đáp án A
Câu 29:
\(n_{NH_4NO_3}=\dfrac{m}{M}=\dfrac{8}{80}=0,1mol\)
\(n_{Zn\left(NO_3\right)_2}=\dfrac{m}{M}=\dfrac{113,4}{189}=0,6mol\)
-Goi số mol zn là x
Zn\(\rightarrow\)Zn2++2e
x.................2x
N+5+8e\(\rightarrow\)N-3(N-3H4NO3)
....0,8\(\leftarrow\)0,1
-Bảo toàn e: 2x=0,8\(\rightarrow\)x=0,4
-Sơ đồ tóm tắt:
Zn\(\rightarrow\)Zn(NO3)2
0,4\(\rightarrow\)0,4
ZnO\(\rightarrow\)Zn(NO3)2
0,2\(\leftarrow\)0,4-0,2
%nZn=\(\dfrac{0,4.100}{0,4+0,2}\approx66,67\%\)\(\rightarrow\)Đáp án A
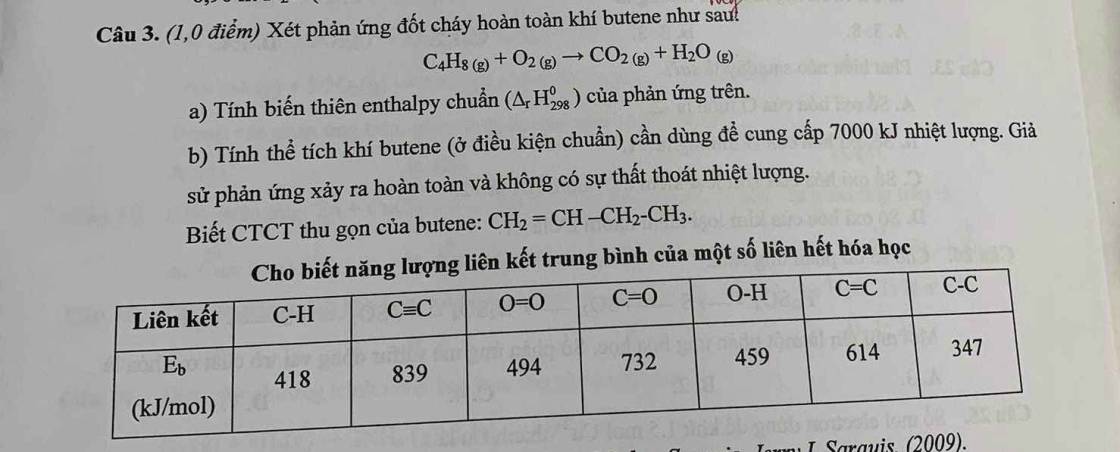


 ai giải cho e bài 10 vs ạaa :<
ai giải cho e bài 10 vs ạaa :< 


 Giúp e bài 55 với ạ
Giúp e bài 55 với ạ