Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

gọi x = nC2H2, y = nCH4 còn lại, z = nH2. từ phản ứng: z = 3x. tỉ khối: (26x +16y +2z)/(x+y+z) = 10 ⇒ (26x+16y+6x)/(4x+y)=10 ⇒ 32x+16y=40x+10y ⇒ y=4x/3. hiệu suất = nCH4 chuyển thành C2H2 / nCH4 ban đầu = x / (x + y) = x / (x + 4x/3) = 3/7 ≈ 42,86%.

Câu 1 :
\(a.CH_4+Cl_2\underrightarrow{as,1:1}CH_3Cl+HCl\)
\(b.C_2H_4+H_2O\underrightarrow{^{H^+,t^0}}C_2H_5OH\)
\(c.CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
\(d.C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
\(e.CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(f.\left(RCOO\right)_3C_3H_5+3NaOH\rightarrow3RCOONa+C_3H_5\left(OH\right)_3\)
Câu 2 :
a) CTCT C2H2 và C2H6 :
\(CH\equiv CH\)
\(CH_3-CH_3\)
b) Nhận biết CH4, C2H4 :
Sục lần lượt các khí qua dung dịch Br2 dư :
- Mất màu : C2H4
- Không HT : CH4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
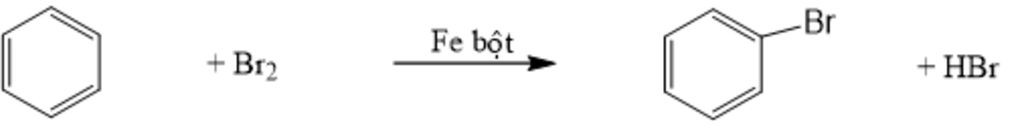
c)
TN1 : Mất màu nâu đỏ Br2 và có khí HBr thoát ra.
 TN2 :
TN2 :
Dầu ăn không tan trong nước , nổi trên bề mặt
Câu 3 :
\(n_{CH_4}=a\left(mol\right),n_{C_2H_6}=b\left(mol\right)\)
\(n_X=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+b=0.2\left(1\right)\)
\(n_{CaCO_3}=\dfrac{30}{100}=0.3\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{^{t^0}}CO_2+2H_2O\)
\(C_2H_6+\dfrac{7}{2}O_2\underrightarrow{^{t^0}}2CO_2+3H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(..............0.3......0.3\)
\(n_{CO_2}=a+2b=0.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%V_{CH_4}=\%V_{C_2H_6}=\dfrac{0.1}{0.2}\cdot100\%=50\%\)
Câu 4 :
\(\text{ Trong 100 ml cồn 70 độ có 70 ml rượu etylic và 30 ml nước.}\)
\(V_{C_2H_5OH}=\dfrac{70}{100}\cdot50=35\left(ml\right)\)
\(n_{C_2H_5OH}=\dfrac{9.2}{46}=0.2\left(mol\right)\)
\(n_{CH_3COOH}=\dfrac{6}{60}=0.1\left(mol\right)\)
\(CH_3COOH+C_2H_5OH\underrightarrow{H^+,t^0}CH_3COOC_2H_5+H_2O\)
\(0.1.........................0.1....................0.1\)
\(H\%=\dfrac{5.28}{0.1\cdot88}\cdot100\%=60\%\)

Bài toán:
- Hỗn hợp Zn, Mg, Fe nặng 38,7g.
- Tác dụng với H₂SO₄ ra 20,16 lít H₂ (0,9 mol).
- Cho NaOH 0,6 mol tạo kết tủa tối đa, nung còn 18,1g oxit.
- Cho NaOH dư tạo kết tủa \(a\) gam.
Trả lời:
- Tổng số mol kim loại = 0,9 mol.
- Từ khối lượng hỗn hợp 38,7g và tổng mol, xác định được mol từng kim loại Zn, Mg, Fe.
- Với 0,6 mol NaOH, số mol kết tủa là 0,3 mol (vì mỗi kết tủa cần 2 mol OH⁻).
- Nung kết tủa thu 18,1g oxit tương ứng với 0,3 mol kết tủa.
- Dùng NaOH dư, tạo kết tủa của toàn bộ 0,9 mol kim loại → khối lượng kết tủa \(a\) sẽ gấp 3 lần phần 1 (vì 0,9 mol gấp 3 lần 0,3 mol), nên \(a = 18 , 1 \times 3 = 54 , 3\) gam.

ác khí độc: H₂S, SO₂, NO₂, Cl₂
Dùng nước vôi trong (Ca(OH)₂ dư) để khử sạch:
- H₂S + Ca(OH)₂ → CaS (kết tủa) + H₂O
\(H_{2} S + C a \left(\right. O H \left.\right)_{2} \rightarrow C a S \downarrow + 2 H_{2} O\) - SO₂ + Ca(OH)₂ → CaSO₃ (kết tủa) + H₂O
\(S O_{2} + C a \left(\right. O H \left.\right)_{2} \rightarrow C a S O_{3} \downarrow + H_{2} O\) - NO₂ + Ca(OH)₂ → Ca(NO₃)₂ + Ca(NO₂)₂ + H₂O
\(2 N O_{2} + 2 C a \left(\right. O H \left.\right)_{2} \rightarrow C a \left(\right. N O_{3} \left.\right)_{2} + C a \left(\right. N O_{2} \left.\right)_{2} + 2 H_{2} O\) - Cl₂ + Ca(OH)₂ → CaCl₂ + Ca(ClO)₂ + H₂O (phản ứng tẩy trắng)
\(C l_{2} + C a \left(\right. O H \left.\right)_{2} \rightarrow C a C l_{2} + C a \left(\right. C l O \left.\right)_{2} + H_{2} O\)
Tóm lại: Nước vôi trong sẽ phản ứng với các khí độc tạo thành chất rắn hoặc muối an toàn, giúp loại bỏ khí độc khỏi môi trường.

TRẢ LỜI:
CO - Cacbon monoxit
CO2 - Cacbon đioxit
HNO3 - Axit nitric
Cl2O - Điclo monoxit
B2H6 - Điboran
PH3 - Photphin
PH5 - Photphoran
C6H12 - Xiclohexan
CO : cacbon oxit
\(CO_2\): cacbon đioxit
\(HNO_3\): axit nitric
\(Cl_2O\): điclo monooxxit
\(B_2H_6\): điboran
\(PH_3\): photphin
\(PH_5\): ??? làm g có
\(C_6H_{12}\): xiclohexan

1
c/ Cho que đóm còn tàn lửa vào mỗi lọ
Nếu khí nào làm que đóm bùng cháy-> O2
Dẫn 2 khí còn lại vào dung dịch nước Brom, nếu khí nào làm đổi màu dd nước brom -> SO2
Còn lại là CO2
PTHH : SO2 + 2H2O + Br2 ----> H2SO4 + 2HBr
a- Trích mẫu thử đánh STT
- Nhỏ 4 mẫu thử vào mẫu giấy quì tím, mẫu thử nào làm quì tím đổi màu đỏ ---> HCl, H2SO4 ( nhóm 1 ), Còn lại NaCl, Na2SO4( nhóm 2) không làm quì tím đổi màu.
- Cho nhóm 1 tác dụng dd BaCl2, nếu đung dịch nào xuất hiện kết tủa --> H2SO4, còn lại HCl không tác dụng.
_ Cho nhóm 2 tác dụng với dung dịch BaCl2, nếu dung dịch nào xuất hiện kết tủa --> Na2SO4. Còn lại NaCl không hiện tượng
PTHH : H2SO4 + BaCl2 ---> BaSO4 + 2HCl
Na2SO4 + BaCl2 ---> BaSO4 + 2NaCl
b/ Bạn chép sai đề nhé
2/a, PTHH : Mg + 2HCl ---> MgCl2 + H2
b. nHCl = 0,05 x 3 = 0,15 mol
nMg = 1,2 : 24 = 0,05 mol
Lập tỉ lệ theo PT -> HCl dư , Mg hết
Theo Pt , ta có: nH2 = nMg = 0,05 mol
=> VH2 ( đktc) = 0,05 x 22,4 = 1,12 lít
c/ Ta có: dung dịch sau pứ gồm MgCl2 và HCl(dư)
nHCl(dư) = 0,15 - 0,1 = 0,05 mol
=> CM(HCl)= 0,05 : 0,05 = 1M
Theo PT, nMgCl2 = nMg = 0,05 mol
=> CM(MgCl2)= 0,05 : 0,05 = 1M


Đặt CTTQ của A là C x H y O z
Vậy x = 1, y = 2, z = 1.
Vậy CTĐGN là C H 2 O .
⇒ Chọn B.