
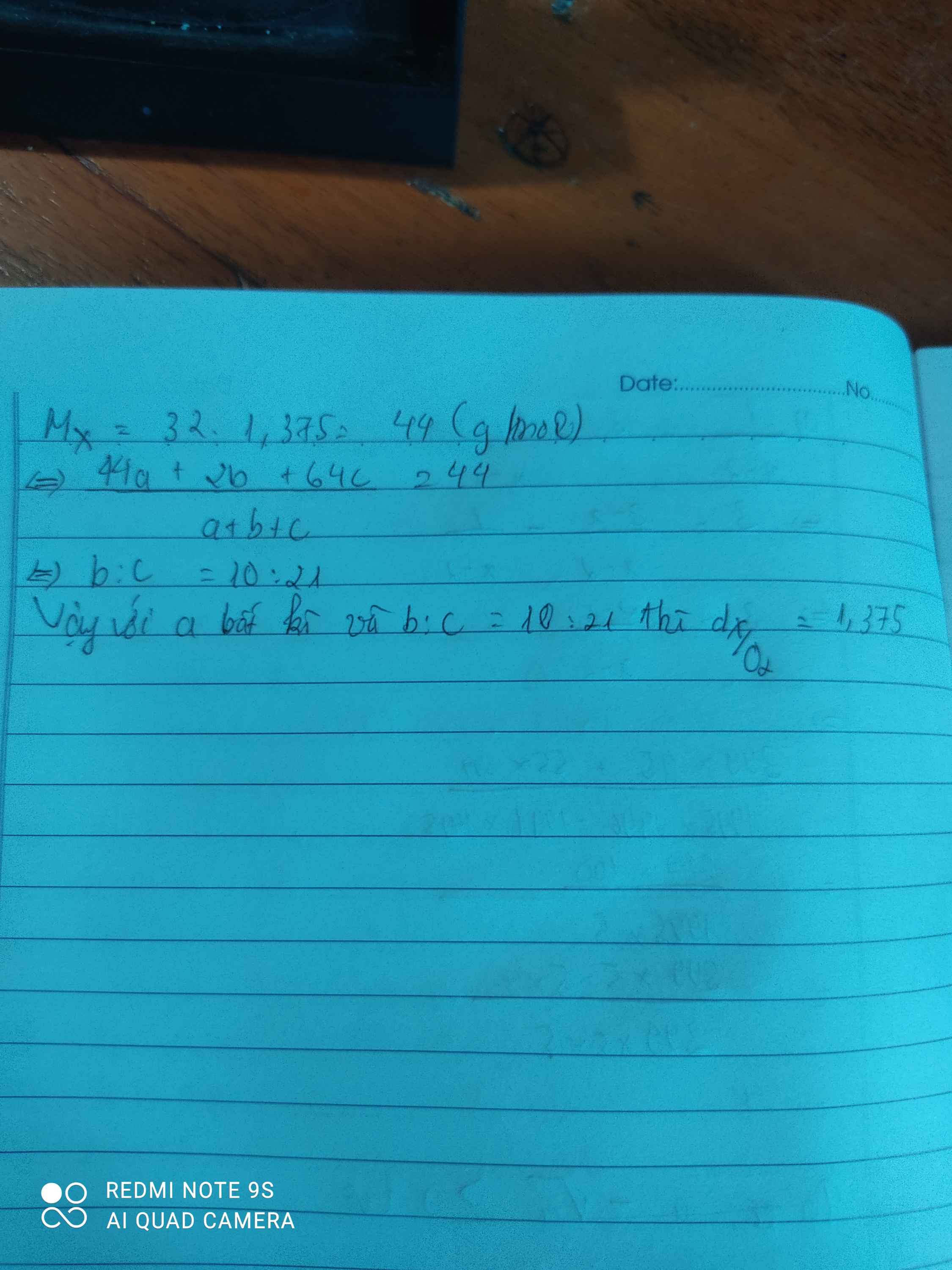
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

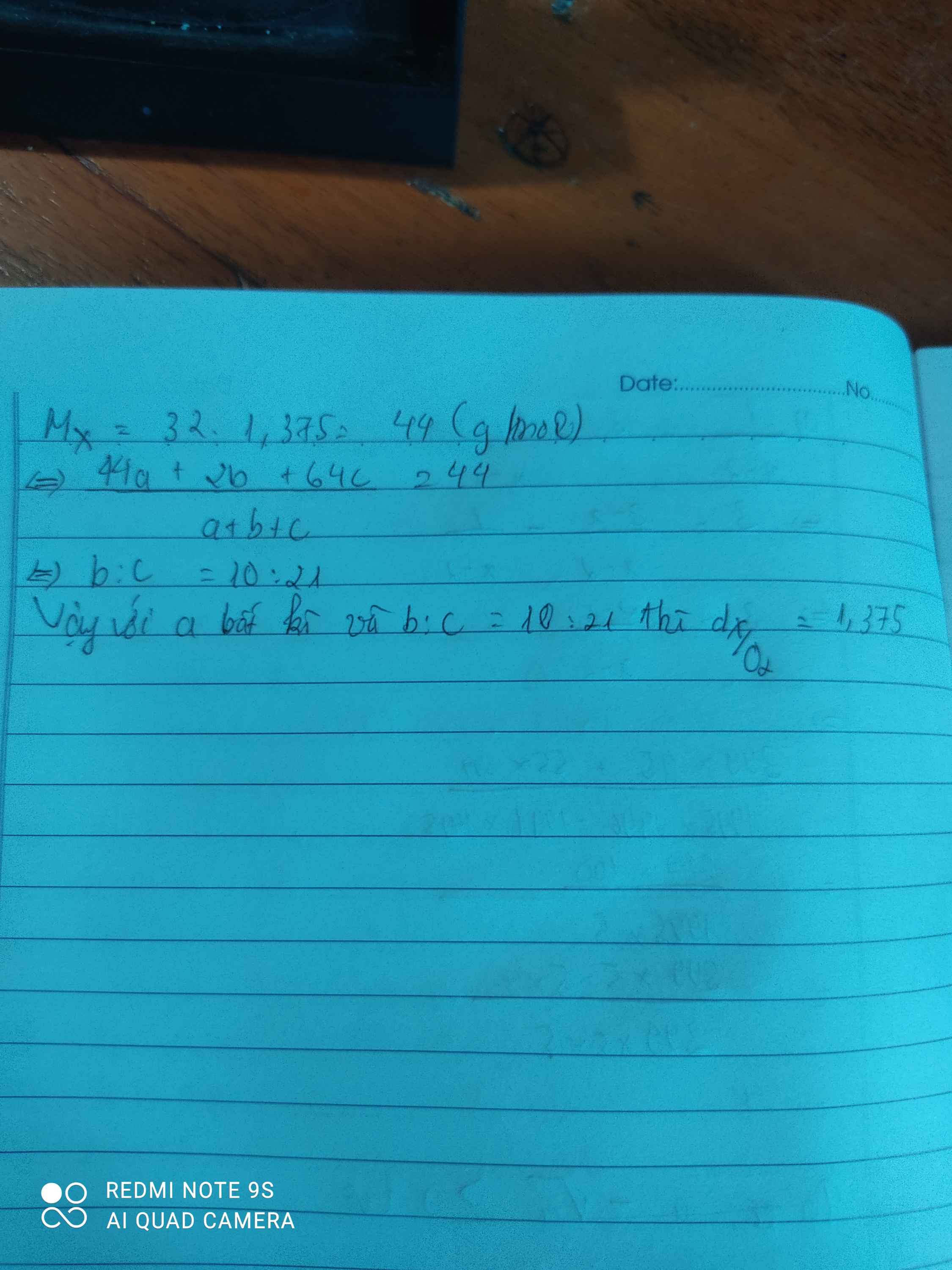

1, a, + 8.2=16 => CH4
+ 8,5 . 2 = 17 => NH3
+ 16 . 2 =32 => O2
+ 22 . 2 = 44 => CO2
b, + 0,138 . 29 \(\approx4\) => He
+ 1,172 . 29 \(\approx34\) => H2S
+ 2,448 . 29 \(\approx71\Rightarrow Cl_2\)
+ 0,965 . 29 \(\approx28\) => N

a) Khối lượng mol phân tử của khí Z: 2.22=44(gam/mol)
b) công thức phân tử: Gọi công thức hóa học chung của hợp chất là NxOy
Ta có: 14x+16y=44
=> x=2; y=1
Công thức hóa học là N2O
c) Tỉ khối của khí Z so với không khí là
dz/dkk=44/29

Ta có :
\(\left\{{}\begin{matrix}n_{CO}=2\left(mol\right)\\n_{CO_2}=3\left(mol\right)\end{matrix}\right.\Rightarrow n_X=2+3=5\left(mol\right)\)
\(\Rightarrow M_X=\dfrac{M_{CO}.n_{CO}+M_{CO_2}.n_{CO_2}}{5}=\dfrac{28.2+44.3}{5}=37,6\)
Tỉ khối của X so với \(H_2\) là :
\(\dfrac{M_X}{M_{H_2}}=\dfrac{37,6}{2}=18,8\)
Đáp án B .

a/ Theo quy tắc đường chéo ta có:
\(\dfrac{2}{3}=\dfrac{0,5-C_{MC}}{C_{MC}-0,2}\)
\(\Leftrightarrow C_{MC}=0,38\left(M\right)\)
b/ Theo quy tắc đường chéo ta có:
\(\dfrac{V_A}{V_B}=\dfrac{0,5-0,3}{0,3-0,2}=2\)

\(Mx=\)44g/mol
-> \(\frac{44a+2b+64c}{a+b+c}=44\)
-->\(b:c=10:21\)
Vậy với a bất kì và \(b:c=10:21\) thì tỉ khối của X so với khí oxi bằng 1,375
Tại sao lại vs bất kì a và b:c=10:21 thì tỉ khối của X so vs khí oxi bằng 1,375.

Theo định luật BTKL ta có :
\(m_{C_2H_2}+m_{H_2}=m+m_y\)
\(\Rightarrow0,06.26+0,04.2=m+0,02.0,5.32\)
\(\Rightarrow m=1,32g\)

a) Khối lượng mol của các khí có tỉ khối với oxi là:
=
=
= 1,375 => MX = 1,375 . 32 = 44g
=
=
= 0,0625 => MY = 0,0625 . 32 = 2 g
b) Khối lượng mol của các khí có tỉ khối với không khí là:
dx/kk = =
= 2,207 => MX = 29 . 2,207 = 64 g
dy/kk = =
= 1,172 => MY = 29 . 1,172 = 34 g
a) Khối lượng mol của các khí có tỉ khối với oxi là:
=
=
= 1,375 => MX = 1,375 . 32 = 44g
=
=
= 0,0625 => MY = 0,0625 . 32 = 2 g
b) Khối lượng mol của các khí có tỉ khối với không khí là:
dx/kk = =
= 2,207 => MX = 29 . 2,207 = 64 g
dy/kk = =
= 1,172 => MY = 29 . 1,172 = 34 g