Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử có 1 mol RCO3
PTHH: RCO3 + 2HCl → RCl2 + CO2↑ + H2O
1 → 2 1 1 1 (mol)
Ta có mdd(sau pứ) = mRCO3+mdd(HCl)−mCO2
⟹ mdd(sau pứ) = \(\dfrac{\text{MR+60+(2.36,5.100%)}}{7,3\%-1,44}\)=MR+1016
⟹ C%(RCl2)=mRCl2mdd(sau).100%=\(\dfrac{M_{R_{ }}+71}{_{ }M_R+1016}\).100%=9,135%
⟹ MR = 24 (Mg)
Vậy công thức của muối là MgCO3.

Giả sử có 1 mol HCl
\(\Rightarrow m_{HCl}=36,5\left(g\right)\Rightarrow m_{dd\text{ }HCl}=500\left(g\right)\)
M + 2HCl ---> MCl2 + H2
0,5__1________0,5____0,5
\(\Rightarrow m_{dd\text{ }sau}=0,5M+499\left(g\right)\\ m_{MCl_2}=0,5\left(M+71\right)\left(g\right)\\ \Rightarrow C\%\left(MCl_2\right)=\frac{0,5\left(M+71\right)}{0,5M+499}=11,96\%\\ \Rightarrow M=55\left(Mn\right)\)

Thể tích khí hiđro thu được: $V_{H_2}=4{,}48\ \text{lít}$ (đktc)
Số mol khí hiđro: $n_{H_2}=\dfrac{4{,}48}{22{,}4}=0{,}2\ \text{mol}$
Phương trình phản ứng: $R + 2HCl \rightarrow RCl_2 + H_2$
Theo phương trình: $n_R = n_{H_2} = 0{,}2\ \text{mol}$
Khối lượng mol của kim loại R: $M_R=\dfrac{4{,}8}{0{,}2}=24\ \text{g/mol}$
=> $R$ là $Mg$
Số mol $HCl$ đã dùng:
$n_{HCl}=2n_{Mg}=2 \times 0{,}2=0{,}4\ \text{mol}$
Khối lượng $HCl$ nguyên chất:
$m_{HCl}=0{,}4 \times 36{,}5=14{,}6\ \text{g}$
Dung dịch $HCl$ có nồng độ $7{,}3\%$ nên:
$m_{\text{dd HCl}}=\dfrac{14{,}6}{0{,}073}=200\ \text{g}$
Khối lượng muối tạo thành:
$n_{MgCl_2}=n_{Mg}=0{,}2\ \text{mol}$
$m_{MgCl_2}=0{,}2 \times 95=19\ \text{g}$
Khối lượng dung dịch sau phản ứng:
$m_{\text{dd}}=200 + 4{,}8 - 0{,}4=204{,}4\ \text{g}$
Nồng độ phần trăm của muối:
$C\%=\dfrac{19}{204{,}4} \times 100\% \approx 9{,}3\%$

Đáp án A
Hướng dẫn Gọi số mol oxit MO = x mol
MO + H2SO4 ® MSO4 + H2O
(mol): x x x
Ta có: (M + 16)x = a
Khối lượng dung dịch axit H2SO4 ban đầu = ![]() = 560x (gam)
= 560x (gam)
Khối lượng dung dịch sau phản ứng = a + 560x = (M + 16)x + 560x
Theo bài: C% (MSO4) = 20% nên: ![]()
Từ đây tìm được M = 24 (magie). Oxit kim loại cần tìm là MgO

Đáp án B
Hướng dẫn
Gọi số mol oxit MO = x mol.
MO + H2SO4 → MSO4 + H2O
(mol): x x x
Ta có: (M + 16)x = a
Khối lượng dung dịch axit H2SO4 ban đầu ![]() = 560x (gam)
= 560x (gam)
Khối lượng dung dịch sau phản ứng = a + 560x = (M + 16)x + 560x.
Theo bài: C% (MSO4) = 20% nên: ![]()
Từ đây ta tìm được M = 24 (magie). Oxit kim loại cần tìm là MgO

\(n_Y=\dfrac{6,72}{22,4}=0,3mol\)
\(2R+2HCl\rightarrow2RCl+H_2\)
0,6 0,6 0,6 0,3
Mà \(n_R=\dfrac{23,4}{M_R}=0,6\Rightarrow M_R=39\left(K\right)\)
\(m_{HCl}=0,6\cdot36,5=21,9\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{21,9}{25}\cdot100=87,6\left(g\right)\)
\(m_{H_2}=0,3\cdot2=0,6\left(g\right)\)
\(m_{KCl\left(lt\right)}=0,6\cdot74,5=44,7\left(g\right)\)
\(m_{ddsau}=23,4+87,6-0,6=110,4\left(g\right)\)
\(\Rightarrow C\%=\dfrac{44,7}{110,4}\cdot100=40,5\%\)

Đáp án A
Gọi n là hoá trị của M; x là số mol của M
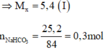
Phương trình hoá học:
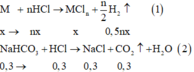
Dung dịch X thu được gồm NaCl: 0,3 mol; MCn: x mol; HCl dư

Tổ hợp (I) và (II) ta được:
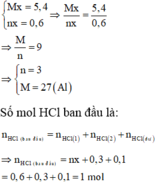
Số mol các khí thu được theo (1), (2) là:
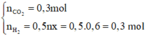
Nồng độ phần trăm của NaCl trong dung dịch X là:
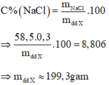
Mặt khác, ta có:
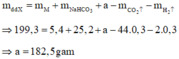
Nồng độ phần trăm dung dịch HCl ban đầu là: