Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) %Cl = 60,68%
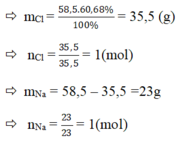
Vậy trong 1 phân tử hợp chất A có : 1 nguyên tử Na, 1 nguyên tử Cl.
⇒ CTHH của hợp chất A : NaCl
b)
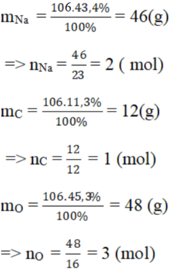
Vậy trong 1 phân tử hợp chất B có: 2 nguyên tử Na, 1 nguyên tử C, 3 nguyên tử O.
⇒ CTHH của hợp chất B : Na2CO3.

b. Ta có: \(\%_{Na}=100\%-60,68\%=39,32\%\)
Gọi CTĐG của A là: NaxCly
Ta lại có: \(\dfrac{x}{y}=\dfrac{\dfrac{39,32\%}{23}}{\dfrac{60,68\%}{35,5}}\approx\dfrac{1,7}{1,7}=\dfrac{1}{1}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
Gọi CTHH của A là: \(\left(NaCl\right)_n\)
Theo đề, ta có: \(M_{\left(NaCl\right)_n}=\left(23+35,5\right).n=58,5\)(g/mol)
\(\Leftrightarrow n=1\)
Vậy CTHH của A là NaCl
b. Gọi CTĐG của B là: \(Na_aC_bO_c\)
Ta có: \(x:y:z=\dfrac{43,4\%}{23}:\dfrac{11,3\%}{12}:\dfrac{45,3\%}{16}\approx1,9:0,9:2,8\approx2:1:3\)
Gọi CTHH của B là: \(\left(Na_2CO_3\right)_t\)
Theo đề, ta có: \(M_{\left(Na_2CO_3\right)_t}=\left(23.2+12+16.3\right).t=106\)(g/mol)
\(\Leftrightarrow t=1\)
Vậy CTHH của B là Na2CO3

bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g

a. %Na = 39,32%
đặt CTHH là ClxNay
\(\dfrac{35,5x}{60,68}=\dfrac{23y}{39,32}\)=\(\dfrac{58,5}{100}=0,585\)
x = \(\dfrac{0,585.60,68}{35,5}\)≃1
y= \(\dfrac{0,585.39,32}{23}\)≃1
=> CTHH là ClNa
b. %O = 45,3%
Đặt CTHH là NaxClyOz
\(\dfrac{23x}{43,4}=\dfrac{12y}{11,3}=\dfrac{16z}{45,3}=\dfrac{106}{100}=1,06\)
x = \(\dfrac{1,06.43,4}{23}=2\)
y = \(\dfrac{1,06.11,3}{12}=1\)
z = \(\dfrac{1,06.45,3}{16}=3\)
CTHH cần lập là Na2CO3
c. Đặt tên phân tử đó là A
\(\dfrac{M_A}{M_{H2}}=8,5\)
=> MA = 17 g/mol
Đặt CTHH là NxHy
\(\dfrac{14x}{82,35}=\dfrac{y}{17,65}=\dfrac{17}{100}=0,17\)
x = \(\dfrac{0,17.82,35}{14}=1\)
y = \(\dfrac{0,17.17,65}{1}=3\)
Vậy CTHH cần lập là NH3

a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
Bài giải:
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl =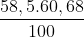 = 35,5 đvC => nCl = 1 mol
= 35,5 đvC => nCl = 1 mol
=> MNa =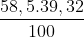 = 23 đvC => nNa = 1 mol
= 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa =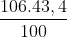 = 46 => nNa =
= 46 => nNa = 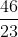 = 2 mol
= 2 mol
MC =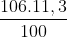 = 12 => nC = 1 mol
= 12 => nC = 1 mol
MO = = 48 => nO =
= 48 => nO = 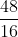 = 3 mol
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl =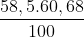 = 35,5 đvC => nCl = 1 mol
= 35,5 đvC => nCl = 1 mol
=> MNa =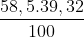 = 23 đvC => nNa = 1 mol
= 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa =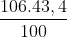 = 46 => nNa =
= 46 => nNa = 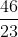 = 2 mol
= 2 mol
MC =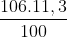 = 12 => nC = 1 mol
= 12 => nC = 1 mol
MO = = 48 => nO =
= 48 => nO = 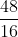 = 3 mol
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
Bài 2 trang 71 sgk hóa học 8 - loigiaihay.com
Bài 2 trang 71 sgk hóa học 8 - loigiaihay.com
a) Ta có: MA=58,5(g/mol)
%Cl=60,68% -> %Na=100%-60,68=39,32%
-> MCl=60,68%÷100%×58,5=35,5 đvC -> nCl=1(mol)
và MNa=58,5%-35,5=23 đvC -> nNa=1(mol)
vậy công thức hóa học của A là: NaCl
b)ta có:
MB=106(g/mol)
MNa=43,4%÷100%×106=46(g/mol)->nNa=2(mol)
MC=11,3%:100%×106=12(g/mol)->nC=1(mol)
MO=45,3%÷100%×106=48(g/mol)->nO=3(mol)
vậy công thức hóa học của B là: Na2CO3
a,
mCl = (60,68 . 58,5)/100 = 35,5g.
nCl = 35,5/35.5 = 1 nguyên tử Cl.
mNa = 58,5 - 35,5 = 23g.
nNa = 23/23 = 1 nguyên tử Na.
Vậy công thức hóa học của hợp chất là NaCl.
b,
MB =106 g
MNa = 106 . 43,4 : 100 = 46 => nNa = 46 : 23 = 2 mol
MC = 106.11,3100106.11,3100 = 12 => nC = 1 mol
MO = 106 . 45,3 : 100 = 48 => nO = 48 : 16 = 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = 58,5.60,6810058,5.60,68100 = 35,5 đvC => nCl = 1 mol
=> MNa = 58,5.39,3210058,5.39,32100 = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = 106.43,4100106.43,4100 = 46 => nNa = 46234623 = 2 mol
MC = 106.11,3100106.11,3100 = 12 => nC = 1 mol
MO = 106.45,3100106.45,3100 = 48 => nO = 48164816 = 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = 58,5.60,6810058,5.60,68100 = 35,5 đvC => nCl = 1 mol
=> MNa = 58,5.39,3210058,5.39,32100 = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = 106.43,4100106.43,4100 = 46 => nNa = 46234623 = 2 mol
MC = 106.11,3100106.11,3100 = 12 => nC = 1 mol
MO = 106.45,3100106.45,3100 = 48 => nO = 48164816 = 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
♫ ♫ ♫ a) MA= 58,5g/mol
%mNa=100% - %mCl=100% - 60,68%= 39,32%
✔ Khối lượng mỗi nguyên tố trong 1 mol hợp chất:
mCl= \(\dfrac{60,68\times58,5}{100}\)\(\approx\) 35,5 (g)
mNa= \(\dfrac{39,32\times58,5}{100}\)\(\approx\) 23 (g)
✔ Số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất:
nCl= \(\dfrac{35,5}{35,5}\)= 1 (mol)
nNa= \(\dfrac{23}{23}\)= 1 (mol)
⇒ Công thức hóa học của hợp chất A: NaCl
♬ ♬ ♬ b) MB=106g/mol
✔ Khối lượng mỗi nguyên tố trong 1 mol hợp chất:
mNa= \(\dfrac{43,4\times106}{100}\)\(\approx\) 46 (g)
mC= \(\dfrac{11,3\times106}{100}\approx\) 12 (g)
mO= \(\dfrac{45,3\times106}{100}\approx\) 48 (g)
✔ Số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất:
nNa= \(\dfrac{46}{23}\)= 2 (mol)
nC= \(\dfrac{12}{12}=\) 1 (mol)
nO= \(\dfrac{48}{16}=\) 3 (mol)
⇒ Công thức hóa học của hợp chất B: Na2CO3
cx dc
a)mCl=58,5.60,68/100=35,5(g)
mNa=58,5.39,32/100=23(g)
nCl=35,5/35,5=1(mol)
nNa=23/23=1(mol)
⇒CTHH:NaCl