Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Lượng nhôm oxit trong 0,5 tấn quặng boxit:
\(0 , 5 \times 50 \% = 0 , 25 \textrm{ } \text{t} \overset{ˊ}{\hat{\text{a}}} \text{n} = 250 \textrm{ } \text{kg}\)Lượng nhôm thu được từ 250 kg nhôm oxit:
\(250 \times \frac{1}{2} = 125 \textrm{ } \text{kg}\)Lượng nhôm tinh khiết (sau khi loại tạp chất):
\(125 \times 0 , 985 = 123 , 125 \textrm{ } \text{kg}\)Lượng nhôm thu được với hiệu suất 90%:
\(123 , 125 \times 90 \% = 110 , 8125 \textrm{ } \text{kg}\)
Kết quả: Lượng nhôm thu được là 110,81 kg.

a. PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
b. Có \(n_{Mg}=\frac{3,6}{24}=0,15mol\)
\(140ml=0,14l\)
\(n_{H_2SO_4}=0,14.1,2=0,168mol\)
Lập tỉ lệ \(\frac{n_{Mg}}{1}< \frac{n_{H_2SO_4}}{1}\)
Vậy Mg đủ, \(H_2SO_4\) dư
Theo phương trình \(n_{H_2SO_4}=n_{Mg}=0,15mol\)
\(\rightarrow n_{H_2SO_4\left(\text{(dư)}\right)}=0,168-0,15=0,018mol\)
\(\rightarrow m_{H_2SO_4\left(\text{(dư)}\right)}n.M=0,018.98=1,764g\)
c. MgSO\(_4\) là muối
Theo phương trình \(n_{MgSO_4}=n_{Mg}=0,15mol\)
\(\rightarrow m_{\text{muối}}=m_{MgSO_4}=n.M=0,15.120=18g\)
d. \(H_2\) là khí
Theo phương trình \(n_{H_2}=n_{Mg}=0,15mol\)
\(\rightarrow V_{H_2\left(ĐKTC\right)}=n.22,4=0,15.22,4=3,36l\)

Phương trình hóa học:
a) H2 (k) + Cl2 (k) → 2HCl(k) (HCl ở trạng thái khí, không màu)
b) S + H2 (k) → H2S (k) (H2S ở trạng thái khí, không màu, có mùi trứng thối)
c) H2 + Br2 → 2HBr(to) (HBr ở trạng thái khí, không màu)

Phương trình hóa học:
a) S + O2 → SO2
b) C + O2 → CO2
c) 2Cu + O2 → 2CuO
d) 2Zn + O2 → 2ZnO
Oxit tạo thành là oxit axit:
SO2 axit tương ứng là H2SO3.
CO2 axit tương ứng là H2CO3.
Oxit tạo thành là oxit bazơ :
CuO bazơ tương ứng là Cu(OH)2.
ZnO bazơ tương ứng là Zn(OH)2.
Ta có các PTHH theo đề:
\(S+O_2\rightarrow^{t^0}SO_2\) SO2 là một oxit axit, có axit tương ứng là H2SO3.
\(C+O_2\rightarrow^{t^0}CO_2\) CO2 là một oxit axit, có axit tương ứng là H2CO3.
\(2Cu+O_2\rightarrow^{t^0}2CuO\) CuO là một oxit bazo, có bazo tương ứng là Cu(OH)2.
\(2Zn+O_2\rightarrow^{t^0}2ZnO\) ZnO là một oxit lưỡng tính.

Các phương trình hóa học:
a) С + 2CuO 2Cu + CO2
b) С + 2PbO 2Pb + CO2
c) С + CO2 2CO
d) С + 2FeO 2Fe + CO2
Các phản ứng trên dều thuộc loại phản ứng oxi hóa - khử. Vai trò của с là chất khử. Các phản ứng:
a), b) dùng điều chế kim loại.
c), d) xảy ra trong quá trình luyện gang, dùng luyện gang.

a) Sơ đồ phản ứng:
S → SO2 → SO3 → H2SO4 → Na2SO4 → BaSO4.
b) Phương trình phản ứng:

PTHH: Zn + H2SO4 ===> ZnSO4 + H2\(\uparrow\)
a) Do Cu không tác dụng với H2SO4 (loãng) => 4,48 lít khí là sản phẩm của phản ứng giữa Zn và H2SO4
nH2 = 4,48 / 22,4 = 0,2 (mol)
=> nZn = nH2 = 0,2 (mol)
=> mZn = 0,2 x 65 = 13 (gam)
=> mCu = 20 - 13 = 7 (gam)
b) Thoe phương trình trên, nH2SO4 = nH2 = 0,2 mol
=> mH2SO4 = 0,2 x 98 = 19,6 (gam)
\(\Rightarrow C\%_{H2SO4}=\frac{19,6}{196}.100\%=10\%\)
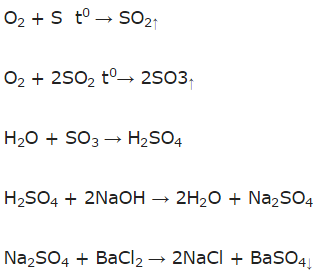

a, Metyl axetat
\(CH_3COOH+CH_3OH⇌CH_3COOCH_3+H_2O\)
b, Etyl axetat
\(CH_3COOH+C_2H_5OH⇌CH_3COOC_2H_5+H_2O\)
c, Etyl fomat
\(HCOOH+C_2H_5OH⇌HCOOC_2H_5+H_2O\)
(Các pư trên đều có nhiệt độ và H2SO4 đặc làm xúc tác)
d, Vinyl axetat
\(CH_3COOH+C_2H_2\underrightarrow{t^o,xt}CH_3COOC_2H_3\)
câu d) lạ vậy ạ
Câu d không điều chế trực tiếp được từ alcol tương ứng vì CH2=CH-OH kém bền bạn nhé.
chỗ \(C_2H_2\) r đến \(\underrightarrow{t^o,xt}\) đk bn
Ý bạn là sao nhỉ?