Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
C sai vì Khối lượng bình tăng lên chính là khối lượng H 2 O và khối lượng CO 2

nC=nCO2=0,672:22,4=0,03
=> mC=0,03.12=0,36 g
=> %C=60%
nH2O=2.nH=2.0,72/18=0,08
=< mH=0,08
=> %H=13,3%
=> %O=100-13.3-60=26,7%

Ta có : mdd =70.0,9162/0,9= 71,26 (g) khối lượng của dd sau khi hấp thụ hơi H2O và CO2
mH2O=71,26 -70=1,26(g)
nH2O=1.26/18=0,07(mol)
nCaCO3=1,4/100=0,014 ( mol)
vì CO2+Ca(OH)2⟶CaCO3+H2O
nCa(OH)2=0,02.2,1=0,042(mol)
nOH- = 0,042.2=0,084(mol)
nCO2=nOH- -nCaCO3 =0,084-0,014=0,07
đặt công thức phân tử là CxHyOz => nCxHyOz = 1,3/130 =0,01 (mol) nCxHyOz->xCO2 +y/2H20
=> bảo toàn C và H => 0,01x=0,07 => x=7
0,01y=2.0,07 => y=2
16z=130-7.12-14=> z=2
công thức phân tử của X là C7H14O2

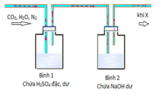
Khối lượng bình (1) tăng 0,63g chính là khối lượng H2O.
\(\Rightarrow m_H=\frac{0,63}{18}.2=0,07g\)
Ở bình (2) : \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
\(0,05\leftarrow\frac{5}{100}=0,05\)
\(\Rightarrow m_C=0,05.12=0,6g\)
\(\Rightarrow m_O=0,67-\left(m_C+m_H\right)=0\)
\(\Rightarrow\%m_C=\frac{0,6}{0,67}.100=89,55\%\)
\(\%m_H=100\%-89,55\%=10,45\%\)

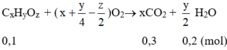

Chọn D
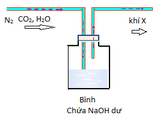
Đốt cháy hoàn toàn hợp chất hữu cơ E bằng O 2 thu được sản phẩm gồm CO 2 , H 2 O và N 2 chứng tỏ trong hợp chất hữu cơ E có C, H, N và có thể có O.