Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
NaOH: 0,05
KOH: 0,1
Gọi công thức chung 2 bazo là MOH (M=101/3) với nMOH=0,15
- Nếu chỉ tạo muối dạng MH2PO4:
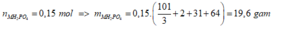
- Nếu chỉ tạo muối dạng M2HPO4:
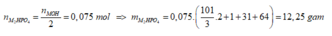
- Nếu chỉ tạo muối M3PO4:
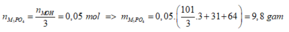
Ta thấy m muối<9,8 gam => MOH dư, H3PO4 hết
Giả sử chất rắn gồm: 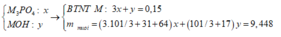
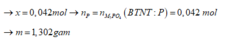

Đáp án C
Phương pháp: Gọi công thức chung 2 bazo là MOH (M = 101/3) với nMOH = 0,15
- Giả sử tạo các muối
+ Nếu chỉ tạo muối dạng MH2PO4
+ Nếu chỉ tạo muối dạng M2HPO4:
+ Nếu chỉ tạo muối M3PO4:
Để biết được hỗn hợp rắn gồm những chất nào, bảo toàn nguyên tố, bảo toàn khối lượng muối => đáp án
Hướng dẫn giải:
NaOH: 0,05
KOH: 0,1
Gọi công thức chung 2 bazo là MOH (M=101/3) với nMOH=0,15
- Nếu chỉ tạo muối dạng MH2PO4:
![]()
![]()
- Nếu chỉ tạo muối dạng M2HPO4:
![]()
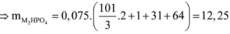
- Nếu chỉ tạo muối dạng M3PO4:
![]()
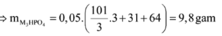
Ta thấy mmuối < 9,8 gam => MOH dư, H3PO4 hết
Giả sử chất rắn gồm:
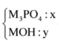
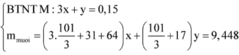
![]()
![]()
![]()

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam

Đáp án D
Gọi số mol của ancol A là: x(mol)
Gọi tổng số mol của axit cacboxylic B và este C là : y (mol)
Đốt cháy B, C luôn cho nH2O = nCO2
Đốt cháy A cho nH2O > nCO2 và có x = nH2O – nCO2
=> nH2O = x + 0,14
BTNT O: x + 2y + 0,18.2 = 0,14.2 + ( 0,14 + x)
=> y = 0,03 (mol)
nNaOH pư = n(B+C) = 0,03 (mol) => nNaOH dư = 0,02 (mol)
=> 0,03 (RCOONa) + 0,02. NaOH = 3,26 (g)
=> 0,03 ( R + 67) + 0,02. 40 = 3,26
=> R = 15
Vậy rắn Y: CH3COONa: 0,03 mol và NaOH: 0,02 (mol)
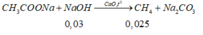
=> nCH4 = nNaOH = 0,025 (mol) => mCH4= 0,025. 16 = 0,4(g)
=> gần nhất với Đáp án D là 4,1 g

Đáp án D
► Đặt CT chung của A là CnH2n+2O (n ≥ 1), B và C là CmH2mO2 (m > 1).
⇒ Phương trình cháy:
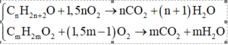
⇒ ∑nB,C = 1,5.∑nCO2 – ∑nO2 = 0,03 mol ⇒ Q gồm 0,03 mol muối và 0,02 mol NaOH dư.
► nNaOH = 0,02 + 0,005 = 0,025 mol || RCOONa + NaOH → t o C a O RH + Na2CO3.
⇒ muối dư, NaOH. Thêm 0,005 mol NaOH ⇄ 0,2 gam NaOH vào để đủ. Bảo toàn khối lượng:
⇒ m = (3,26 + 0,2 + 0,2 – 0,03 × 106) × 0,025 ÷ 0,03 = 0,4(g)


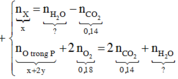
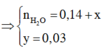

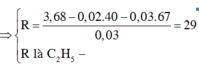
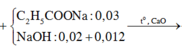

Đáp án C
n N a O H = 0 , 5 . 0 , 1 = 0 , 05 m o l ; n K O H = 0 , 5 . 0 , 2 = 0 , 1 m o l
Gọi công thức chung của 2 bazơ mà MOH
Ta có: n M O H = 0 , 1 + 0 , 05 = 0 , 15 m o l
M M O H = 40 . 0 , 05 + 56 . 0 , 1 0 , 15 = 152 3 → M M = 101 3
TH1: Muối là MH2PO4
→ n M H 2 P O 4 = 0 , 15 m o l → m M H 2 P O 4 = 0 , 15 . 101 3 + 97 = 19 , 6 g a m
TH2: Muối là M2HPO4
→ n M H 2 P O 4 = 0 , 075 m o l → m M H 2 P O 4 = 0 , 075 . 101 3 . 2 + 96 = 12 , 25 g a m
TH3: Muối là M3PO4
→ n M 3 P O 4 = 0 , 05 m o l → m M 3 P O 4 = 9 , 8 g a m
Nhận thấy: m M 3 P O 4 < m c h ấ t r ắ n
Chất rắn có chứa MOH dư (a mol) và M3PO4 (b mol)
Ta có hệ phương trình:
BTNT.P ta có: n P = 0 , 042 m o l → m p = 0 , 042 . 31 = 1 , 302 g a m