Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n C O 2 = 8,8 44 = 0,2 m o l → n C = 0,2 m o l ; m C = 2,4 g a m . n H 2 O = 5,4 18 = 0,3 m o l → n H = 0,6 m o l ; m H = 0,6 g a m .
Bảo toàn khối lượng có: m A + m O 2 = m C O 2 + m H 2 O
→ m A = 8 , 8 + 5 , 4 – 11 , 2 = 3 g a m .
Giả sử trong A có O → m O ( A ) = m A – m C – m H = 3 – 2 , 4 – 0 , 6 = 0 .
Vậy trong A không có Oxi.
Đặt công thức tổng quát của A là C x H y ta có:
x : y = n C : n H = 0 , 2 : 0 , 6 = 1 : 3 .
Vậy A có công thức đơn giản nhất là C H 3 n .
Lại có 25 < M A < 35 → n = 1 thỏa mãn. A là C 2 H 6 .
⇒ Chọn A.

a) Tính \(m\):
- Số mol khí:
\(n_{k h \overset{ˊ}{\imath}} = \frac{11 , 2}{22 , 4} = 0 , 5 \&\text{nbsp};\text{mol}\)
- Khối lượng Fe và Al theo tỉ lệ:
\(m_{A l} = 0 , 3 m , m_{F e} = 0 , 7 m\)
- Khối lượng rắn còn lại:
\(m_{r \overset{ˊ}{\overset{ }{a}} n} = 0 , 75 m\)
- Khối lượng kim loại phản ứng:
\(m_{p h ả n ứ n g} = m - 0 , 75 m = 0 , 25 m\)
- Giải hệ phương trình dựa vào phản ứng và số mol khí để tìm \(m\).
b) Tính thể tích dung dịch NaOH:
- Số mol kết tủa tính theo khối lượng 7,8 g.
- Tính số mol OH\(^{-}\) cần theo tỉ lệ phản ứng với Al và Fe trong dung dịch.
- Tính thể tích NaOH 2M:
\(V = \frac{n_{O H^{-}}}{2}\)

Gọi hiệtrocacbon là CxHy với số mol n. - Từ khối lượng nước: n(H2O) = 3,6/18 = 0,2\,mol. Theo phản ứng đốt cháy, n(H2O) = \frac{y}{2} \cdot n \Rightarrow y\cdot n = 0,4. (1) - Từ thể tích O2: n(O2) = 7,437/22,4 \approx 0,332\,mol. Theo phản ứng: n(O2) = \left(x + \frac{y}{4}\right) \cdot n. (2) Giải hệ (1) và (2) trong điều kiện x,y nguyên dương ta thu được x = 9, y = 16 và n = 0,025\,mol. **a)** Số mol CO2: n(CO2) = x\,n = 9\times0,025 = 0,225\,mol \Rightarrow a = m_{CO2} = 0,225 \times 44 \approx 9,9\,g. Khối lượng hiệtrocacbon: M = 12x + y = 12\cdot9 +16 = 124\,g/mol \Rightarrow m = n\times M = 0,025\times124 \approx 3,1\,g. **b)** 8\,g brom tương ứng 0,05\,mol Br2. Tỷ số mol Br2 : n = 0,05/0,025 = 2, nên mỗi phân tử X có 2 liên kết đôi. Kiểm tra độ bất bão hòa của C9H16: \frac{2\cdot9+2-16}{2} = 2, phù hợp. Do đó, công thức phân tử của X là C9H16, một ankađien có hai liên kết đôi.

Đốt cháy A thu được sản phẩm chứa C, H, O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\Rightarrow n_H=0,2\left(mol\right)\)
Xét mC + mH = 0,1.12 + 0,2.1 = 1,4 (g) < 2,2 (g)
=> A chứa C, H, O
\(n_O=\dfrac{2,2-1,4}{16}=0,05\left(mol\right)\)
Xét nC : nH : nO = 0,1 : 0,2 : 0,05 = 2 : 4 : 1
=> CTPT: (C2H4O)n
\(M_A=\dfrac{3,3}{\dfrac{0,84}{22,4}}=88\left(g/mol\right)\)
=> n = 2
=> CTPT: C4H8O2

\(M_X=2.13=26\left(\dfrac{g}{mol}\right)\\ n_C=n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\\ n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\rightarrow n_H=0,1.2=0,2\left(mol\right)\\ Đặt:C_aH_b\left(a,b:nguyên,dương\right)\\ Có:a:b=n_C:n_H=0,2:0,2=1:1\\ \Rightarrow CTTQ:\left(CH\right)_m\left(m:nguyên,dương\right)\\ M_{\left(CH\right)_m}=26\\ \Leftrightarrow13m=26\\ \Leftrightarrow m=2\\ \Rightarrow CTPT:C_2H_2\\ CTCT:CH\equiv CH\)
b) Nhận biết C2H2 và CH4
- Dẫn 2 khí qua bình đựng nước brom:
+ Dung dịch Br2 bị mất màu -> C2H2
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
+ Còn lại -> CH4

Gọi công thức của A là C x H y O z
Đốt cháy 3 gam A được 6,6 gam CO 2 và 3,6 gam H 2 O
Vậy m C trong 3 gam A là 6,6/44 x 12 = 1,8g
m H trong 3 gam A là 3,6/18 x 2 = 0,4g
Vậy trong 3 gam A có 3 - 1,8 - 0,4 = 0,8 (gam) oxi.
Ta có quan hệ:
60 gam A → 12x gam C → y gam H → 16z gam O
3 gam A → 1,8 gam C → 0,4 gam H → 0,8 gam O
=> x = 60 x 1,8 /36 = 3 ; y = 60 x 0,4/3 = 8
z = 60 x 0,8/48 = 1
Công thức của A là C 3 H 8 O



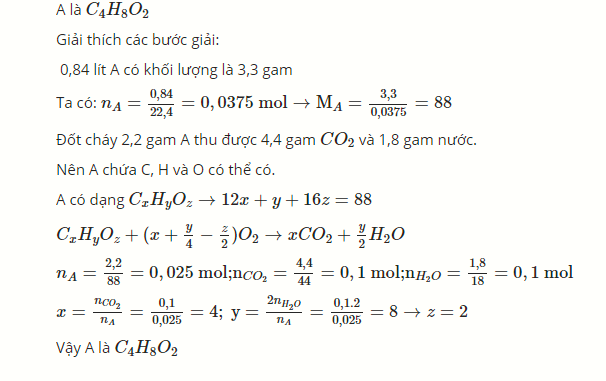
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.