Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo định luật bảo toàn khối lượng, ta có:
m o x i t = m K L + m O / o x i t
⇔ m O / o x i t = m o x i t - m K L
=44-2,86 = 1,28g
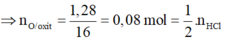
⇒ = n H C l = 0,08.2 = 0,16 mol
Áp dụng định luật bảo toàn khối lượng, ta có khối lượng của muối khan thu được là:
m m u o i = m K L + m C l
= 2,86 + 0,16.35,5 = 8,54g
⇒ Chọn C.

So sánh các phản ứng của hỗn hợp X với oxi và hỗn hợp Y với dung dịch HCl, ta thấy :
n HCl = 2 n trong oxit ; m O 2 = 8,7 - 6,7 = 2g
n O trong oxit = 0,125 mol; n HCl = 0,25 mol
V HCl = 0,25/2 = 0,125l

Ta có : \(m_{oxit}=m_{KL}+m_O=58,4\)
\(\Rightarrow m_O=14,4g\)
\(\Rightarrow n_O=\dfrac{m}{M}=0,9\left(mol\right)\)
\(BTNT\left(O\right):n_{H2O}=n_O=0,9\left(mol\right)\)
\(BTNT\left(H\right):n_{H2SO4}=n_{H2O}=0,9\left(mol\right)\)
\(\Rightarrow V_{H2SO4}=0,45l\)
nO2- = (58,4-44)/16 = 0,9 => ne = 0,9.2= 0,18 => nSO42- = 0,9 => V = 450 ml

Bước 1: Viết các phản ứng chính
- Đốt cháy hỗn hợp Mg, Fe trong O₂:
\(M g + \frac{1}{2} O_{2} \rightarrow M g O\)\(F e + \frac{3}{4} O_{2} \rightarrow F e_{3} O_{4}\)
Lưu ý: Thông thường, sắt cháy tạo Fe₃O₄ (oxi hóa sắt hỗn hợp Fe²⁺ và Fe³⁺).
Bước 2: Gọi số mol của Mg và Fe là:
\(n_{M g} = x \left(\right. m o l \left.\right) n_{F e} = y \left(\right. m o l \left.\right)\)
Bước 3: Viết các biểu thức khối lượng ban đầu:
\(24 x + 56 y = 4 , 16 \left(\right. 1 \left.\right)\)
Bước 4: Viết khối lượng oxit sau phản ứng
Khối lượng oxit X = 5,92 g gồm:
- MgO: khối lượng = \(24 x + 16 x = 40 x\) g
- Fe₃O₄: khối lượng = \(56 y + 64 y / 3 = 56 y + \frac{64}{3} y = \frac{168 y + 64 y}{3} = \frac{232 y}{3}\) g
Vì Fe₃O₄ gồm 3 Fe (3 × 56 =168) và 4 O (4 × 16 =64), tổng 232 g/mol.
Vậy khối lượng Fe₃O₄ tạo ra từ y mol Fe là:
\(\text{Fe}_{3} \text{O}_{4} = \frac{232}{3} y\)
Tổng khối lượng oxit:
\(40 x + \frac{232}{3} y = 5 , 92 \left(\right. 2 \left.\right)\)
Bước 5: Giải hệ (1) và (2)
\(\left{\right. 24 x + 56 y = 4 , 16 \\ 40 x + \frac{232}{3} y = 5 , 92\)
Bước 6: Dung dịch Y chứa:
- MgCl₂: số mol = \(x\) (từ MgO + 2HCl → MgCl₂ + H₂O)
- FeCl₂ và FeCl₃ (từ Fe₃O₄ hòa tan trong HCl theo phản ứng hỗn hợp)
Phản ứng hòa tan Fe₃O₄ trong HCl:
\(F e_{3} O_{4} + 8 H C l \rightarrow F e C l_{2} + 2 F e C l_{3} + 4 H_{2} O\)
Số mol FeCl₂ = 1 mol, FeCl₃ = 2 mol trên 1 mol Fe₃O₄.
Với y mol Fe nguyên tố:
\(n_{F e_{3} O_{4}} = \frac{y}{3} \left(\right. \left(\text{v} \overset{ˋ}{\imath} \&\text{nbsp};\text{Fe}\right)_{3} O_{4} \&\text{nbsp};\text{c} \overset{ˊ}{\text{o}} \&\text{nbsp};\text{3}\&\text{nbsp};\text{Fe} \left.\right)\)
Do đó:
- \(n_{F e C l_{2}} = \frac{y}{3}\)
- \(n_{F e C l_{3}} = 2 \times \frac{y}{3} = \frac{2 y}{3}\)
Bước 7: Kết tủa Z khi cho NaOH dư:
- MgCl₂ + 2NaOH → Mg(OH)₂↓ + 2NaCl
- FeCl₂ + 2NaOH → Fe(OH)₂↓ + 2NaCl
- FeCl₃ + 3NaOH → Fe(OH)₃↓ + 3NaCl
Số mol các kết tủa hydroxyd:
- Mg(OH)₂: \(x\) mol
- Fe(OH)₂: \(\frac{y}{3}\) mol
- Fe(OH)₃: \(\frac{2 y}{3}\) mol
Bước 8: Nung kết tủa Z (gồm Mg(OH)₂, Fe(OH)₂, Fe(OH)₃) đến khối lượng không đổi (6 g):
- Mg(OH)₂ → MgO:
Khối lượng giảm 18 g/mol (do mất H₂O)
M₁(Mg(OH)₂) = 58 g/mol, M₁(MgO) = 40 g/mol
Tỉ lệ: 40/58 - Fe(OH)₂ → FeO:
M(Fe(OH)₂) = 89.86 g/mol, M(FeO) = 71.84 g/mol
Tỉ lệ: 71.84/89.86 ≈ 0.8 - Fe(OH)₃ → Fe₂O₃ (để đơn giản) hoặc Fe₃O₄ (phức tạp hơn)
Ở đây chúng ta giả sử Fe(OH)₃ → Fe₂O₃:
M(Fe(OH)₃) = 106.87 g/mol, M(Fe₂O₃) = 159.69 g/mol
Hai mol Fe(OH)₃ tạo thành 1 mol Fe₂O₃. Nên cần tính theo số mol tương ứng.
Bước 9: Viết biểu thức khối lượng sau nung:
Khối lượng sau nung = 6 g
\(40 x + 0.8 \times 89.86 \times \frac{y}{3} + \left(\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{l}ượ\text{ng}\&\text{nbsp};\text{Fe}(\text{OH})\right)_{3} \&\text{nbsp};\text{sau}\&\text{nbsp};\text{nung} = 6\)
Phần Fe(OH)₃ chuyển thành Fe₂O₃:
\(\frac{2 y}{3} \&\text{nbsp};\text{mol}\&\text{nbsp};\text{Fe}(\text{OH})_{3} \rightarrow \frac{y}{3} \&\text{nbsp};\text{mol}\&\text{nbsp};\text{Fe}_{2} O_{3}\)
Khối lượng Fe(OH)₃ ban đầu:
\(106.87 \times \frac{2 y}{3}\)
Khối lượng Fe₂O₃ sau nung:
\(159.69 \times \frac{y}{3}\)
Khối lượng Fe(OH)₃ sau nung = \(\frac{159.69}{106.87} \times \left(\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{l}ượ\text{ng}\&\text{nbsp};\text{Fe}(\text{OH})\right)_{3}\) ban đầu
≈ \(1.495 \times 106.87 \times \frac{2 y}{3} = 159.69 \times \frac{y}{3}\)
Bước 10: Viết lại biểu thức khối lượng sau nung
\(40 x + 0.8 \times 89.86 \times \frac{y}{3} + 159.69 \times \frac{y}{3} = 6\)
Tính từng phần:
- \(0.8 \times 89.86 \times \frac{y}{3} = 71.89 \times \frac{y}{3} = 23.96 y\)
- \(159.69 \times \frac{y}{3} = 53.23 y\)
Nên:
\(40 x + 23.96 y + 53.23 y = 6 \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } 40 x + 77.19 y = 6 \left(\right. 3 \left.\right)\)
Bước 11: Giải hệ (1), (2), (3):
\(\left{\right. 24 x + 56 y = 4.16 \left(\right. 1 \left.\right) \\ 40 x + \frac{232}{3} y = 5.92 \left(\right. 2 \left.\right) \\ 40 x + 77.19 y = 6 \left(\right. 3 \left.\right)\)
Hệ (2) và (3) gần giống, chênh lệch nhỏ do xấp xỉ, ta dùng (1) và (3):
Từ (1):
\(24 x = 4.16 - 56 y \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } x = \frac{4.16 - 56 y}{24}\)
Thay vào (3):
\(40 \times \frac{4.16 - 56 y}{24} + 77.19 y = 6\)\(\frac{40 \times 4.16}{24} - \frac{40 \times 56 y}{24} + 77.19 y = 6\)\(6.93 - 93.33 y + 77.19 y = 6\)\(6.93 - 16.14 y = 6\)\(- 16.14 y = 6 - 6.93 = - 0.93\)\(y = \frac{0.93}{16.14} \approx 0.0576 \&\text{nbsp};\text{mol}\)
Thay y vào (1):
\(x = \frac{4.16 - 56 \times 0.0576}{24} = \frac{4.16 - 3.225}{24} = \frac{0.935}{24} = 0.0389 \&\text{nbsp};\text{mol}\)
Bước 12: Tính m gam kết tủa AgCl khi cho Y tác dụng với AgNO₃ dư
Dung dịch Y chứa:
- MgCl₂: số mol = \(x = 0.0389\)
- FeCl₂: \(y / 3 = 0.0576 / 3 = 0.0192\)
- FeCl₃: \(2 y / 3 = 0.0384\)
Khi cho AgNO₃ dư:
- Mỗi mol Cl⁻ tạo 1 mol AgCl (kết tủa)
Số mol Cl⁻ tổng:
\(\text{MgCl}_{2} : 2 \times 0.0389 = 0.0778\)\(\text{FeCl}_{2} : 2 \times 0.0192 = 0.0384\)\(\text{FeCl}_{3} : 3 \times 0.0384 = 0.1152\)
Tổng số mol Cl⁻:
\(0.0778 + 0.0384 + 0.1152 = 0.2314\)
Bước 13: Tính khối lượng kết tủa AgCl
Khối lượng mol AgCl = 143.5 g/mol
\(m = 0.2314 \times 143.5 = 33.2 \&\text{nbsp};\text{g}\)
Kết luận:
\(\boxed{m = 33.2 \&\text{nbsp};\text{g}}\)
Tk

a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,2<---0,6<--------------0,3
=> \(\left\{{}\begin{matrix}\%Al=\dfrac{0,2.27}{15,6}.100\%=34,615\%\\\%Al_2O_3=\dfrac{15,6-0,2.27}{15,6}.100\%=65,385\%\end{matrix}\right.\)
b) \(n_{Al_2O_3}=\dfrac{15,6-0,2.27}{102}=0,1\left(mol\right)\)
PTHH: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
______0,1--->0,6
=> nHCl = 0,6+0,6 = 1,2(mol)
=> \(V_{dd}=\dfrac{1,2}{2}=0,6\left(l\right)\)

\(n_{Mg}=0,07mol;n_{Al}=0,08mol\\ n_{Cl_2}=a;n_{O_2}=b\\ 2H^++O^{2-}->H_2O\\ n_{H^+}=0,12\cdot\dfrac{2}{2}=2b\\ b=0,06mol\\ BTDT:0,07\cdot2+0,08\cdot3=2a+4b\\ a=0,07\\ \%V_{Cl_2}=\dfrac{a}{a+b}=53,85\%\)
mO = 5,96 - 4,04 = 1,92 (g)
=> \(n_O=\dfrac{1,92}{16}=0,12\left(mol\right)\)
=> \(n_{H_2O}=0,12\left(mol\right)\)
=> \(n_{HCl}=0,24\left(mol\right)\)
=> \(V_{ddHCl}=\dfrac{0,24}{2}=0,12\left(l\right)\)
0,12 lít
Cho em xin lời giải cụ thể nha mọi người. Em cảm ơn mọi người nhiều ạ.
Anh/Chị ơi dòng đầu em không hiểu ạ :(( Em cảm ơn anh chị nhiều ạ.
mình lm = bảo toàn nguyên tố thôi bn
nếu bn thích lm theo kiểu viết phương trình thì lm như sau:
Quy đổi hỗn hợp kim loại thành R (hóa trị n)
\(n_R=\dfrac{4,04}{M_R}\left(mol\right)\)
PTHH: 4R + nO2 --to--> 2R2On
\(\dfrac{4,04}{M_R}\)------------>\(\dfrac{2,02}{M_R}\)
=> \(\dfrac{2,02}{M_R}\left(2M_R+16n\right)=5,96\)
=> \(M_R=\dfrac{101}{6}n\) => \(n_{R_2O_n}=\dfrac{2,02}{M_R}=\dfrac{2,02}{\dfrac{101}{6}n}=\dfrac{0,12}{n}\left(mol\right)\)
PTHH: R2On + 2nHCl --> 2RCln + nH2O
\(\dfrac{0,12}{n}\)-->\(0,24\)
=> \(V_{ddHCl}=\dfrac{0,24}{2}=0,12\left(l\right)\)