
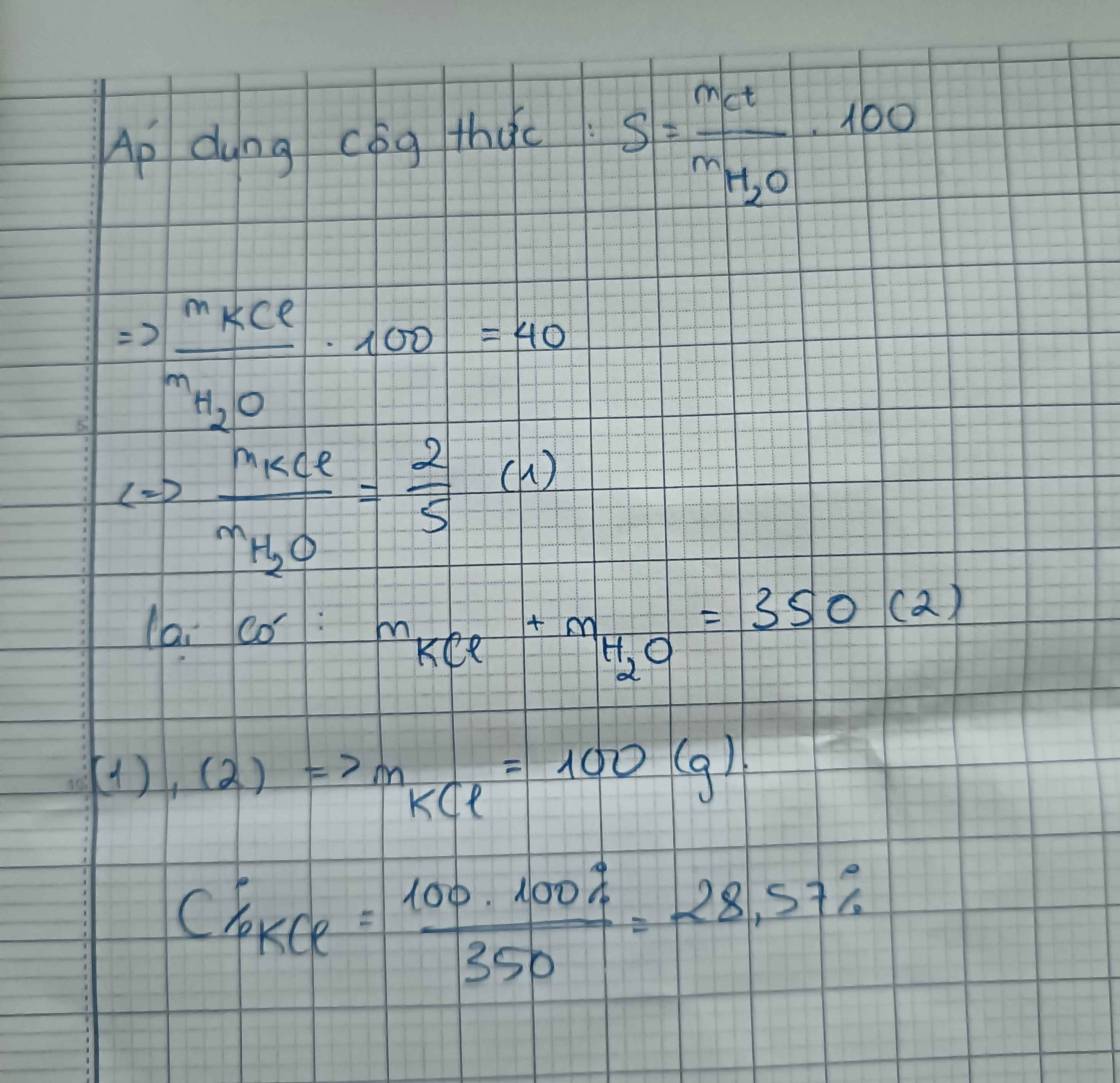
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

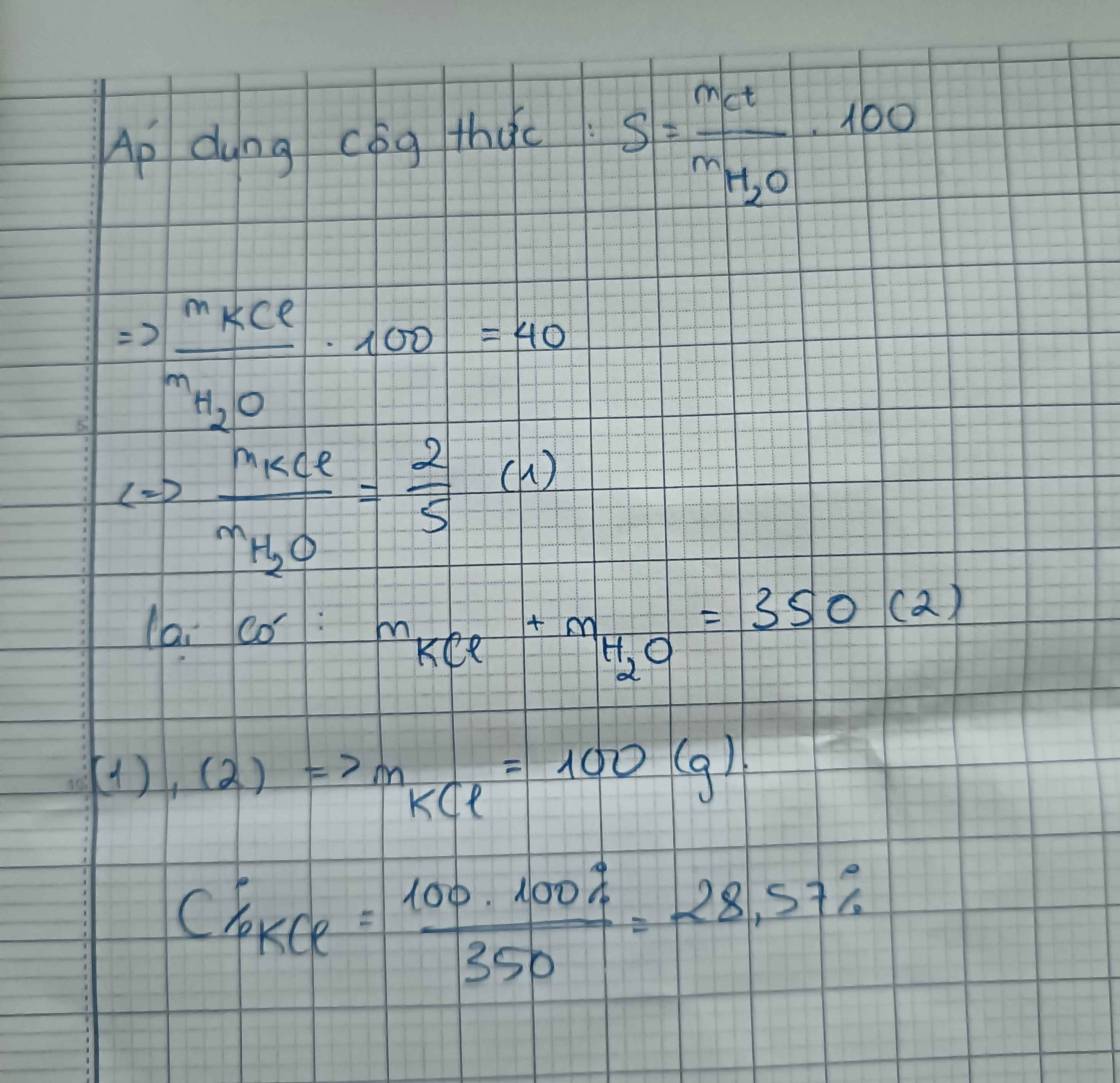

Phương trình: \text{Zn} + \text{H}_{2}\text{SO}_{4} \rightarrow \text{ZnSO}_{4} + \text{H}_{2} \uparrow. Số mol các chất: n_{\text{Zn}} = \frac{19,5}{65} = 0,3 \text{ mol}. m_{\text{H}_{2}\text{SO}_{4}} = \frac{200 \cdot 24,5\%}{100\%} = 49 \text{ g} \Rightarrow n_{\text{H}_{2}\text{SO}_{4}} = \frac{49}{98} = 0,5 \text{ mol}. Biện luận: Vì 0,3 < 0,5 nên \text{Zn} hết, \text{H}_{2}\text{SO}_{4} dư. Tính toán sau phản ứng: n_{\text{H}_{2}\text{SO}_{4} \text{ pư}} = n_{\text{ZnSO}_{4}} = n_{\text{H}_{2}} = 0,3 \text{ mol}. m_{\text{H}_{2}\text{SO}_{4} \text{ dư}} = 49 - (0,3 \cdot 98) = 19,6 \text{ g}. m_{\text{ZnSO}_{4}} = 0,3 \cdot 161 = 48,3 \text{ g}. Khối lượng dung dịch sau phản ứng: m_{\text{dd}} = m_{\text{Zn}} + m_{\text{dd } \text{H}_{2}\text{SO}_{4}} - m_{\text{H}_{2}} = 19,5 + 200 - (0,3 \cdot 2) = 218,9 \text{ g}. Nồng độ phần trăm (C\%): C\%_{\text{ZnSO}_{4}} = \frac{48,3}{218,9} \cdot 100\% \approx 22,06\%. C\%_{\text{H}_{2}\text{SO}_{4} \text{ dư}} = \frac{19,6}{218,9} \cdot 100\% \approx 8,95\%.

Độ tan của Na2CO3 trong nước ở 18 độ C là: S = (53 : 250) = 0,212
\(S_{Na_2CO_3\left(18^oC\right)}=\dfrac{100.53}{250}=21,2\left(g\right)\)

- Nồng độ mol (CM) là số mol chất tan có trong 1 lít dung dịch.
độ tan (S) cho biết lượng chất tan có trong 100 gam nước để tạo thành dung dịch bão hòa

Mình hệ thống lại tính chất hóa học của các loại oxit để bạn dễ học nhé 👇
✅ Tóm gọn: