

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



C. Gọi kim loại cần tìm là R. Các PTHH:
R + H2SO4 → RSO4 +H2 (1)
H2SO4 + 2NaOH → Na2SO4 + H2O (2)
Số mol của H2SO4 bằng: 0,15.0,5 = 0,075 (mol);
Số mol của NaOH bằng: 0,03.1 = 0,03 (mol)
=> Số mol của H2SO4 ở (1) bằng: 0,075 - = 0,06 (mol).
Từ (1) => nR = = 0,06; mR =
= 24 (g/mol)
Vậy R là Mg

Đáp án D.
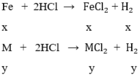
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 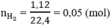
theo bài ra ta có hệ phương trình
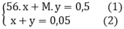
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 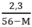
Ta có 0 < y < 0,05
y > 0 ↔ 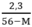 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 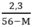 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be

C. Gọi kim loại cần tìm là R. Các PTHH:
R + H2SO4 → RSO4 +H2 (1)
H2SO4 + 2NaOH → Na2SO4 + H2O (2)
Số mol của H2SO4 bằng: 0,15.0,5 = 0,075 (mol);
Số mol của NaOH bằng: 0,03.1 = 0,03 (mol)
=> Số mol của H2SO4 ở (1) bằng: 0,075 - = 0,06 (mol).
Từ (1) => nR = = 0,06; mR =
= 24 (g/mol)
Vậy R là Mg
Hòa tan 1,44 gam một kim loại hóa trị II trong 150 ml dung dịch H2SO4 0,5M. Để trung hòa axit dư trong dung dịch thu được thì phải dùng hết 30ml dung dịch NaOH 1M. Kim loại đó là
A. Ba
B. Ca
C. Mg
D. Be

\(n_{CO_2}=\dfrac{0.896}{22.4}=0.04\left(mol\right)\)
\(\Rightarrow n_{HCl}=0.04\cdot2=0.08\left(mol\right)\Rightarrow m_{HCl}=0.08\cdot36.5=2.92\left(g\right)\)
\(\Rightarrow n_{H_2O}=0.04\left(mol\right)\Rightarrow m_{H_2O}=0.04\cdot18=0.72\left(g\right)\)
\(BTKL:\)
\(m_{Muối}=3.34+2.92-0.04\cdot44-0.72=3.78\left(g\right)\)