Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{HCl}=\dfrac{300.7,3}{100}=21,9g\)
gọi x la hoa tri cua X
2X + 2xHCl \(\rightarrow\) 2XClx + xH2
pt: 2X 73x
de: 5,4 21,9
Ta co: 21,9. 2X = 5,4. 73x
=> 43,8X = 394,2x
=> X = 9x
biện luận:
+ x = 1 => X = 9 (loại)
+ x = 2 => X = 18 (loại)
+ x = 3 => X = 27 (lấy)
a, X là Al
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
Ta co: \(\dfrac{0,2}{2}=\dfrac{0,6}{6}\) => k có chất nào dư
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
de: 0,2 \(\rightarrow\) 0,2 \(\rightarrow\) 0,3
\(m_{AlCl_3}=0,2.133,5=26,7g\)
\(m_{dd}=300+5,4-0,3.2=304,8g\)
b,\(C\%_{AlCl_3}=\dfrac{26,7}{304,8}.100\%\approx8,76\%\)

1/ PT : X + 2H2O -> X[OH]2 + H2
mol : \(\frac{6}{M_X}\) -> \(\frac{6}{M_X}\)
=> mH2 = \(\frac{12}{M_X}\) => mdd = m+6 - \(\frac{12}{M_X}\)
Ta có: m+5,7 = m+6 - \(\frac{12}{M_X}\)
<=> \(\frac{12}{M_X}\)= 0,3 => MX = 40 => X là Canxi [Ca]
2/ Dặt nHCl= a [a> 0] => mddHCl= 36,5a : 14,6 x 100= 250a
PT : X + 2HCL => XCl2 + H2
mol : a/2 a -> a/2 a/2
mH2 = a/2 x 2 = a ; mX = a/2 . MX
m XCl2= a/2 x [MX +71]
mdd XCL2= a/2 .MX + 250a - a = a/2 .MX +249a
Ta có :\(\frac{\frac{a}{2}\times M_X+\frac{71}{2}a}{M_X\times a:2+249a}\times100\%=24,15\%\)
<=> \(\frac{M_X+71}{M_X+498}=24,15\%\Leftrightarrow M_X=65\)=> X là kẽm [Zn]

\(n_{HCl}=\dfrac{200\cdot7.3\%}{36.5}=0.4\left(mol\right)\)
\(M+2HCl\rightarrow MCl_2+H_2\)
\(0.2.....0.4.........0.2........0.2\)
\(m_{MCl_2}=0.2\cdot\left(M+71\right)\left(g\right)\)
\(m_{dd}=0.2M+200-0.2\cdot2=0.2M+199.6\left(g\right)\)
\(C\%MCl_2=\dfrac{0.2\cdot\left(M+71\right)}{0.2M+199.6}\cdot100\%=12.05\%\)
\(\Rightarrow M=56\)
\(M:Sắt\)

nCO2 = 0,15 mol
MgCO3 + 2HCl ---> MgCl2 + CO2 + H2O
0.1 0,1 --> 0,1
RCO3 + 2HCl ---> RCl2 + CO2 + H2O
0,05 <---- (0,15-0,1)
Ta thấy: n HCl = 2n CO2 = 2.0,15 = 0,3 mol
m dd HCl = (0,3.36,5).100/7,3 = 150g
m CO2 = 0,15.44 = 6,6g
m dd sau phản ứng = m X + m dd HCl - m CO2 = 157,6 g
m MgCl2 = m dd sau phản ứng.C%/100 ~ 9,5g
n MgCl2 = 0,1 mol (thế vào pt trên)
Ta có: m RCO3 = m X - m MgCO3
=> 0,05(R + 60) = 14,2 - 0,1.84
=> R = 56
Vậy R là Fe
Chúc em học tốt!!

nH2=\(\frac{6,72}{22,4}=0,3\)mol
PTHH
M+2HCl--> MCl2+H2
0,3mol<---------------0,3mol
=>MM=\(\frac{19,5}{0,3}=64\)
=> km loại là kẽm (Zn)
b) nNaOH=0,2.1=0,2 mol
PTHH
NaOH+HCl-->NaCl + H2O
0,2 mol--> 0,2 mol
---> thể tích HCl 1M đã dùng là V=\(\frac{0,2+0,3}{1}=0,5\)lít
=> CM(ZnCl2)=\(\frac{0,3}{0,5}=0,6M\)

Gọi CT oxit là R2On
R2On + nH2SO4 => R2(SO4)n + nH2O
nR2On=20,4/(2R+16n) mol
nR2(SO4)n=68,4/(2R+96n) mol
MÀ nR2On=nR2(SO4)n
=>20,4(2R+96n)=68,4(2R+16n)
=>96R=864n=>M=9n
Chọn n=3 có M=27 =>M là Al ct oxit là Al2O3
nAl2O3=20,4/102=0,2 mol
Al2O3 + 3H2SO4 => Al2(SO4)3 +3H2O
0,2 mol=>0,6 mol
CM dd H2SO4=0,6/0,3=2 M
@DoMinhTam nhưng mà nhỡ đâu kim loại A hóa trị thay đổi thì sao

Ta có: \(n_{HCl}=0,12.2=0,24\left(mol\right)\)
Gọi CTHH của oxit kim loại là A2On.
PT: \(A_2O_n+2nHCl\rightarrow2ACl_n+nH_2O\)
Theo PT: \(n_{A_2O_n}=\dfrac{1}{2n}n_{HCl}=\dfrac{0,24}{2n}=\dfrac{0,12}{n}\left(mol\right)\)
\(\Rightarrow M_{A_2O_n}=\dfrac{4,8}{\dfrac{0,12}{n}}=40n=2M_A+16n\Rightarrow M_A=12n\)
Với n = 2 thì MA = 24 (g/mol)
Vậy: A là Mg.
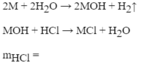
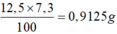

a, Ta có nHCl = \(\dfrac{300\times7,3\%}{36,5}\) = 0,6 ( mol )
2X + 2nHCl \(\rightarrow\) 2XCln + nH2
\(\dfrac{0,6}{n}\).....0,6.........\(\dfrac{0,6}{n}\)........0,3
=> nX = \(\dfrac{0,6}{n}\) = \(\dfrac{5,4}{M_X}\)
Vì n là hóa trị của kim loại
=> 1 \(\le\) n \(\le\) 3
=> Lập bảng
=> X là Al ( Nhôm )
b, Ta có mH2 = 2 . 0,3 = 0,6 ( gam )
=> Mdung dịch = Mtham gia - MH2
= 300 + 5,4 - 0,6
= 304,8 ( gam )
=> nAlCl3 = \(\dfrac{0,6}{3}\) = 0,2 ( mol )
=> mAlCl3 = 0,2 . 133,5 = 26,7 ( gam )
=> C%AlCl3 = \(\dfrac{26,7}{304,8}\) . 100 \(\approx\) 8,76 %
Gọi n là hóa trị của kim loại X
\(m_{HCl}=\dfrac{300.7,3}{100}=21,9\left(g\right)\)
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
PT: \(2X+2nHCl\rightarrow2XCl_n+nH_2\)
----\(\dfrac{0,6}{n}\)-----0,6---------\(\dfrac{0,6}{n}\)-------------(mol)
\(M_X=\dfrac{5,4}{\dfrac{0,6}{n}}=9n\left(\dfrac{g}{mol}\right)\)
Vậy X là kim loại nhôm. KHHH: Al
b) \(n_{AlCl_3}=\dfrac{0,6}{3}=0,2\left(mol\right)\)
\(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
\(C\%=\dfrac{26,7}{26,7+100}.100=21,07\%\)
Phần tính C% bị sai rồi nha bạn
Cảm ơn bạn nka
Bài của bạn Elly Phạm đúng rồi. Em xem cách làm của bạn đê lần sau không mắc phải lỗi sai tương tự nhé
Dạ