Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Số mol canxi cacbonat tham gia phản ứng
=
= 0,1 mol
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Theo phương trình hóa học, ta có:
=
= 0,1 mol
Khối lượng của canxi clotua tham gia phản ứng:
= 0,1 . (40 + 71) = 11,1 g
b) Số mol canxi cacbonat tham gia phản ứng:
=
= 0,05 mol
Theo phương trình hóa học, ta có:
=
= 0,05 mol
Thể tích khí CO2 ở điều kiện phòng là:
= 24 . 0,05 = 1,2 lít

a) Số mol canxi cacbonat tham gia phản ứng nCaCO3= 10/100 = 0,1 mol.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
Theo phương trình hóa học, ta có: nCaCl2= nCaCO3 = 0,1 mol.
Khối lượng của canxi clorua tham gia phản ứng: mCaCl2 = 0,1 . (40 + 71) = 11,1 g.
b) Số mol canxi cacbonat tham gia phản ứng: nCaCO3= 5/100 = 0,05 mol.
Theo phương trình hóa học, ta có: nCO2= nCaCO3 = 0,05 mol.
Thể tích khí CO2 ở điều kiện phòng là: VCO2 = 24 . 0,05 = 1,2 lít.

Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g
Bài giải:
Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g

a) Ta có:
\(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\\ n_{Cu}=\dfrac{64}{64}=1\left(mol\right)\\ n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
b) Ta có:
Thể tích của 0,175 mol CO2 (ở đktc):
\(V_{CO_2\left(đktc\right)}=0,175.22,4=3,92\left(l\right)\)
Thể tích của 1,25 mol H2 (ở đktc):
\(V_{H_2\left(đktc\right)}=1,25.22,4=28\left(l\right)\)
Thể tích của 3 mol N2 (ở đktc):
\(V_{N_2\left(đktc\right)}=22,4.3=67,2\left(l\right)\)
c) Ta có: \(n_{CO_2}=\dfrac{0,44}{44}=0,01\left(mol\right)\\ n_{H_2}=\dfrac{0,04}{2}=0,02\left(mol\right)\\ n_{N_2}=\dfrac{0,56}{28}=0,02\left(mol\right)\)
Số mol hỗn hợp: \(n_{hh}=0,01+0,02+0,02=0,05\left(mol\right)\)
Thể tích hỗn hợp (đktc):\(V_{hh}=0,01.22,4+0,02.22,4+0,02.22,4=1,12\left(l\right)\)
a)
nFe = = 0,5 mol
nCu = = 1 mol
nAl = = 0,2 mol
b) Thể tích khí ở đktc:
= 22,4 . 0,175 = 3,92 lít
= 22,4 . 1,25 = 28 lít
= 22,4 . 3 = 67,2 lít
c) Số mol và thể tích của hỗn hợp:
=
= 0,01 mol;
= 22,4 . 0,01 = 0,224 lít
=
= 0,02 mol;
= 22,4 . 0,2 = 0,448 lít;
=
= 0,02 mol;
= 22,4 . 0,02 = 0,448 lít.
Vậy số mol của hỗn hợp là:
nhh = 0,01 + 0,02 + 0,02 = 0,05 mol
Thể tích hỗn hợp là:
Vhh = 0,224 + 0,448 + 0,448 = 1,12 lít
Hoặc Vhh = 0,05 . 22,4 = 1,12 lít

a) Khối lượng H2SO4 là: m = 10 g
Nồng độ phần trăm dung dịch H2SO4 sau khi pha loãng là:
C% = . 100% = 20%
b) Thể tích dung dịch H2SO4 là: V = 45,45 ml
Số mol của H2SO4 là: n = 0,102 mol
Nồng độ mol của dung dịch H2SO4 sau khi pha loãng:
CM = = 2,24 (mol/lít)

PTHH: 2H2 + O2 -to-> 2H2O
Ta có: \(\dfrac{8,4}{2}>\dfrac{2,8}{1}\)
=> H2 dư, O2 hết nên tính theo \(V_{O_2}\)
Theo PTHH và đề bài, ta có:
\(m_{H_2O}=2.\dfrac{2,8}{22,4}.18=4,5\left(g\right)\)

Bài 1:
\(n_{C_4H_{10}}=\frac{m}{M}=\frac{11,6}{58}=0,2mol\)
PTHH: \(2C_4H_{10}+13O_2\rightarrow^{t^o}8CO_2\uparrow+10H_2O\)
0,2 1,3 0,8 1 mol
\(\rightarrow n_{O_2}=n_{C_4H_{10}}=\frac{13.0,2}{2}=1,3mol\)
\(V_{O_2\left(ĐKTC\right)}=n.22,4=1,3.22,4=29,12l\)
\(\rightarrow n_{CO_2}=n_{C_4H_{10}}=\frac{8.0,2}{2}=0,8mol\)
\(m_{CO_2}=n.M=0,8.44=35,2g\)
\(\rightarrow n_{H_2O}=n_{C_4H_{10}}=\frac{10.0,2}{2}=1mol\)
\(m_{H_2O}=n.M=1.18=18g\)

a)CaCO3 +2HCl-----> CaCl2 + CO2 +H2O
b) Ta có
n\(_{CaCO3}=\frac{10}{100}=0,1\left(mol\right)\)
Theo pthh
n\(_{CaCl2}=n_{CaCO3}=0,1\left(mol\right)\)
m\(_{CaCl2}=0,1.111=11,1\left(g\right)\)
c) Theo pthh
n\(_{CO2}=n_{CaCO3}=0,1\left(mol\right)\)
V\(_{CO2}=0,1.22,4=2,25\left(l\right)\)
Chúc bạn học tốt

Trước tiên ta cần chuyển đổi khối lượng các khí ra số mol phân tử. Số mol của các chất khí:
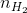 =
=  = 0,5 mol;
= 0,5 mol; 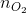 =
= 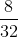 = 0,25 mol
= 0,25 mol
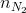 =
= 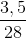 = 0,125 mol;
= 0,125 mol; 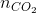 =
= 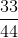 = 0,75 mol.
= 0,75 mol.
Tỉ lệ về số mol các khí cũng là tỉ lệ về thể tích các chất khí ở cùng một điều kiện, ta có sơ đồ biểu diễn:
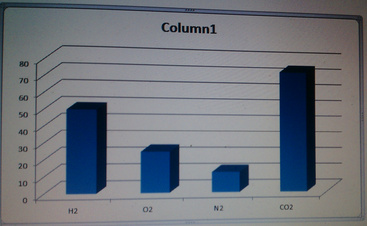

a, nCaCO3=10/100=0,1 mol
PTHH: CaCO3+2HCl---> CaCl2+CO2+H2O
Theo pthh ta có: nCaCl2=nCaCO3=0,1 mol
=> mCaCl2=0,1.111=11,1 (g)
b, nCaCO3=5/100=0,05 mol
Theo pthh ta có : nCO2=nCaCO3=0,05 mol
=> VO2(điều kiện phòng)= 0,05.24= 1,2 l
a) Số mol canxi cacbonat tham gia phản ứng
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Theo phương trình hóa học, ta có:
Khối lượng của canxi clotua tham gia phản ứng:
b) Số mol canxi cacbonat tham gia phản ứng:
Theo phương trình hóa học, ta có:
Thể tích khí CO2 ở điều kiện phòng là:
a) Số mol canxi cacbonat tham gia phản ứng
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Theo phương trình hóa học, ta có:
Khối lượng của canxi clotua tham gia phản ứng:
b) Số mol canxi cacbonat tham gia phản ứng:
Theo phương trình hóa học, ta có:
Thể tích khí CO2 ở điều kiện phòng là:
nCaCO3=10÷100=0,1(mol)
PTHH:CaCO3 + 2HCl -> CaCl2 + CO2↑ + H2O
Theo pt ta có: nCaCO3=nCaCl2=0,1(mol)
->mCaCl2=0,1×111=11,1(g)
b)nCaCO3=5÷100=0,05(mol)
PTHH: CaCo3 + 2HCl -> CaCl2 + CO2↑ +H2O
Theo pt ta có: nCO2=nCaCO3=0,05(mol)
->VCO2=0,05×22,4=1,2(l)
Bài 4 trang 79 sgk hóa học 8 - loigiaihay.com
Bài 4 trang 79 sgk hóa học 8 - loigiaihay.com
@Cẩm Vân Nguyễn Thị bạn ấy tự làm đó cô.
@Cẩm Vân Nguyễn Thị bạn này làm đúng.
a) Theo đề bài, ta có nCaCO3 = \(\dfrac{m_{CaCO_3}}{M_{CaCO_3}}\)= \(\dfrac{10}{40+12+16.3}\)= 0,1 mol.
Vì theo đề bài, axit clohidric dùng dư nên số mol các chất sản phẩm tính theo số mol của CaCO3.
Từ phương trình phản ứng, ta có: nCaCO3 = nCaCl2 = 0,1 mol.
Suy ra, khối lượng CaCl2 lthu được sau phản ứng là:
mCaCl2 = nCaCl2 . MCaCl2 = 0,1.(40 + 35,5.2) = 0,1.111= 11,1 gam.
Vậy khối lượng muối CaCl2 thu được sau phản ứng là 11,1 gam.
b) Vì theo đề bài CaCO3 tác dụng hết với axit và không có dư nên số mol các chất sản phẩm sẽ tính theo số mol cuả CaCO3.
ta có nCaCO3 = \(\dfrac{m_{CaCO_3}}{M_{CaCO_3}}\)= \(\dfrac{5}{40+12+16.3}\)= 0,05 mol.
Từ phương trình phản ứng, ta có: nCaCO3 = nCO2 = 0,05 mol.
Ta có tỉ lệ cứ 1 mol khí CO2 ở điều kiện phòng có thể tích là 24 lít.
Suy ra 0,05 mol khí CO2 ở điều kiện phòng có thể tích là X lít.
Hay X= \(\dfrac{0,05.24}{1}\)= 1,2.
Vậy thể tích khí CO2 thu được là 1,2 lít.
a/ \(n_{CaCO_3}=\dfrac{m}{M}=\dfrac{10}{100}=0.1\)mol
PTHH : \(CaCO_3+2HCl->CaCl_2+CO_2+H_2O\)
Từ PTHH có \(n_{CaCO_3}=0,1mol\)
=> \(m_{CaCl_2}=0,1.111=11,1\)(g)
b/ \(n_{CaCO_3}=\dfrac{m}{M}=\dfrac{5}{100}=0,05mol\)
Từ PTHH có \(n_{CO_2}=n_{CaCO_3}=0.05mol\)
\(V_{O_2}=0,05.24=1,2l\)