Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ct FexOy
FexOy + 2yHCl ====xFeCl2y/x + yH2O
a.............2ay
=> 2ay = 0,45 => ay = 0,225
FexOy + yCO ====xFe + yCO2
a.............................ax
=> ax = 8,4/56 = 0,15
=> ay/ax = 0,225/0,15 = 3 : 2
=> Ct sắt oxit là Fe2O3

n(H2)=1,68/22=0,075m0l
n(CaC03)=10/1O0=0,1m0l
gọi công thức oxit sát là FexOy
Ptpu:
Fex0y + yCO ===> xFe + yC02 (1)
Fe + 2HCL ===> FeCl2 + H2
0,075m0l <-----. . . . . . . . . . ---- 0,075m0l
C02 + Ca(0H)2 ===> CaC03 + H20
0,1m0l <-----. . . . . . . . . . 0,1m0l
Theo tỉ lệ số mol theo phương trình (1) ta co:
x/y=n(Fe)/n(C02)=0,075/0,1=3/4
Vay oxit sat can tim la oxit sat tu Fe304
Than yC02
0,15/x(m0l) <=== 0,15
Theobài thì khối lượng oxit sắt oh 2 p/u = nhau nên số mol = nhau hay (0,225/y)=(0,15/x)
<=>0,225x=0,15y
<=>x=2y/3
<=>x/y=2/3
Vậy oxit có công thức là Fe203

nO(Oxit)=\(\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,15.3=0,225mol\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
-Gọi công thức là FexOy
-Ta có:
x:y=0,15:0,225=2:3\(\rightarrow\)Fe2O3

\(CTTQ:Fe_xO_y\)
\(n_{HCl}=0,2\left(mol\right);n_{Fe}=0,1\left(mol\right)\)
\(PTHH:Fe_xO_y+2yHCl\rightarrow xFeCl_{2y/x}+yH_2O\)
(mol)_____\(\frac{0,1}{y}\)______0,2_____________________
\(PTHH:Fe_xO_y+yCO\underrightarrow{t^o}xFe+yCO_2\)
(mol)______\(\frac{0,1}{x}\)___________0,1__________
Vì cùng hóa tan và cùng khử a (g) oxit nên số mol của oxit 2 pt là như nhau
\(\Rightarrow\frac{0,1}{y}=\frac{0,1}{x}\Leftrightarrow\frac{x}{y}=\frac{0,1}{0,1}=\frac{1}{1}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
\(\rightarrow CTHH:FeO\)
Đặt công thức oxit sắt là FexOy
\(nFe=\frac{5,6}{56}=0,1\left(mol\right)\)
\(nHCl=2\cdot0,1=0,2\left(mol\right)\)
FexOy + 2yHCl ----> xFeCl2y/x + yH2O (1)
..0,1/y.......0,2.............
FexOY + yCO ----> xFe + yCO2 (2)
..0,1/x.......................0,1.
Vì ở PTHH (1) và (2) đều có lượng oxit sắt như nhau
\(\Rightarrow\frac{0,1}{y}=\frac{0,1}{x}\Rightarrow\frac{x}{y}=\frac{1}{1}\)
Vậy công thức của oxit sắt là FeO

\(n_{HCl}=0,15.3=0,45\left(mol\right)\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
Gọi cthc: FexOy , x,y \(\in Z^+\)
\(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2O\)(1)
0,45/2y <---- 0,45
\(Fe_xO_y+yCO\rightarrow xFe+yCO_2\) (2)
0,15/x <--------------0,15
(1)(2) \(\dfrac{0,45}{2y}=\dfrac{0,15}{x}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy cthc: Fe2O3

FexOy+2yHCl->xFeCl2y/x+yH2O
nHCl=0.225(mol)
->nFexOy=0.225*1/2y=0.225/2y
FexOy+yH2->xFe+yH2O
nFe=0.075(mol)->nFe=0.075*1/x=0.075/x
Vì lượng oxit sắt ở hai pt bằng nhau
->số mol oxit sắt cũng bằng nhau
->\(\frac{0.225}{2y}=\frac{0.075}{x}\)
->0.225x=2y*0.075
0.225x=0.15y
->x/y=0.15:0.225=2/3
->công thức của oxit sắt đó là Fe2O3



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3
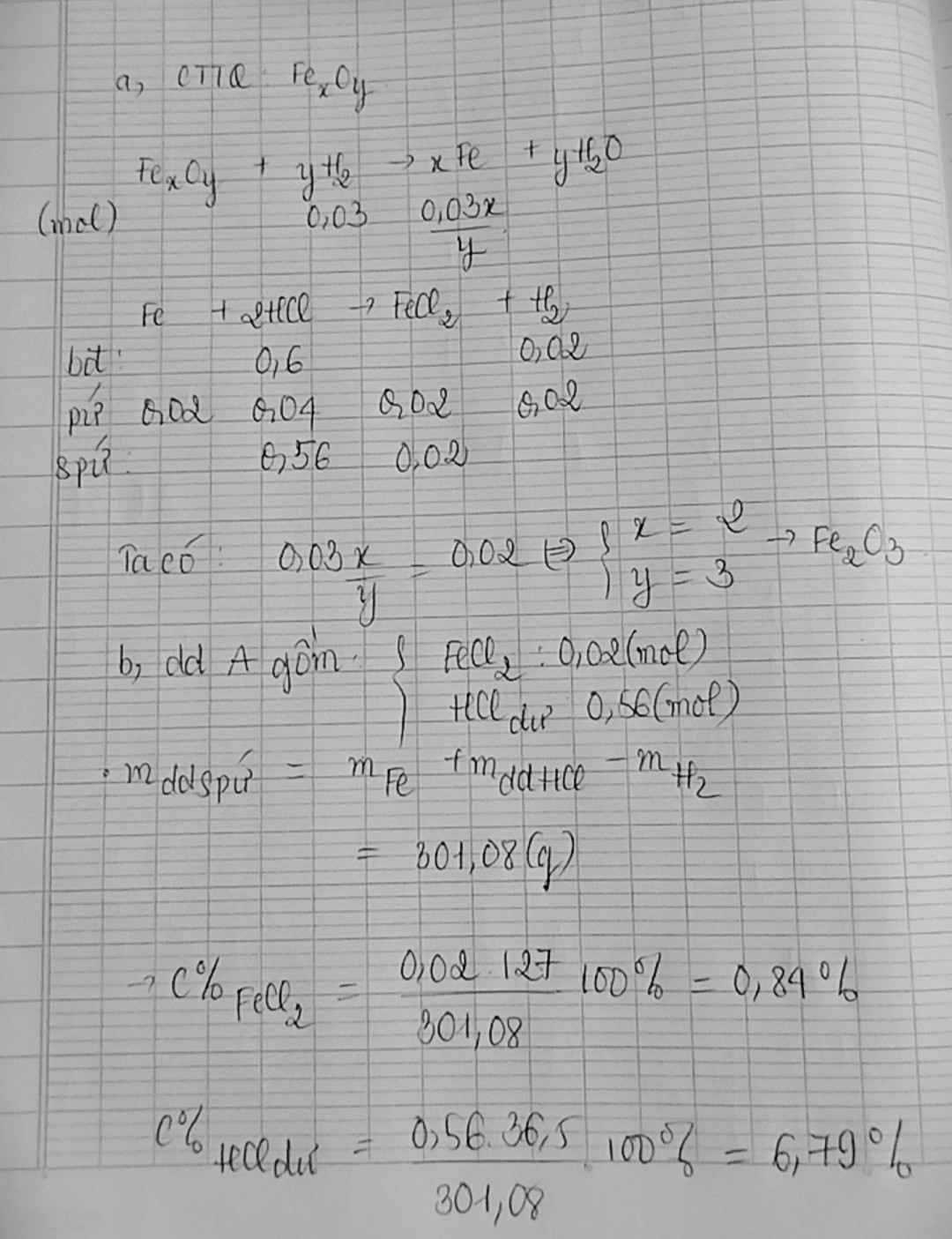
nHCl = 0,15.3 = 0,45 mol
FexOy + 2yHCl = xFeCl(2y/x) + yH2O
nFexOy = nHCl/2y = 0,45/2y mol (1)
FexOy + yCO = xFe + yCO2
nFexOy = nFe/x = (8,4/56)/x = 0,15/x mol (2)
Cho (1) bằng (2) => x/y = 2/3 (Fe2O3)
cảm ơn vì câu trả lời của bạn Lê Nguyên Hạo.
kcj
Hạo giúp mình hai bài trên nữa đc ko
gọi CTTQ của oxit sắt là: FexOy
nHCl = 0,15. 3 = 0,45 mol
nFe = 8,4 : 56 = 0,15 mol
FexOy + 2yHCl ---> xFeCl2y/x + yH2O
\(\dfrac{0,45}{2y}\) 0,45
FexOy + yCO ---> xFe + yCO2
\(\dfrac{0,15}{x}\) 0,15
Từ 2 pt trên ta có
=> \(\dfrac{0,45}{2y}=\dfrac{0,15}{x}\)
=> 0,45x = 0,3y
=> \(\dfrac{x}{y}=\dfrac{0,3}{0,45}=\dfrac{2}{3}\)
=> x= 2; y=3
Vậy CTHH: Fe2O3
tại sao chỗ FeCl2x/y lại như thế mà không phải là FeCly(do hóa trị của Fe trong oxit là y) bạn có thể giải thích giúp mình được ko
vì FexOy thì tổng hóa trị của nó bắt buộc phải bằng 0 . Mà Oxi có hóa trị 2 thì lấy hóa trị nhân chỉ số của O rồi chia cho chỉ số của Fe . thì hóa trị của Fe = (2.x)/y