Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
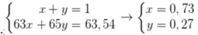
Phần trăm khối lượng của 63Cu trong Cu2O là
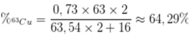

Đáp án D
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt
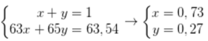
Phần trăm khối lượng của 63Cu trong CuCl2 là
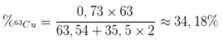

Đáp án A
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
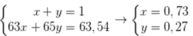
Phần trăm khối lượng của 63Cu trong CuSO4 là
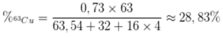

Ta có: nCu = 6,354 : 63,54 = 0,1 (mol)
Gọi tỉ lệ phần trăm của đồng vị 63Cu trong tự nhiên là x
=> Tỉ lệ phần trăm của đồng vị 65Cu trong tự nhiên là 100 – x
- Nguyên tử khối trung bình của Cu là 63,54
=> \(63,54 = \frac{{63.x + 65.(100 - x)}}{{100}}\)
=> x = 73
=> Tỉ lệ phần trăm của đồng vị 63Cu trong tự nhiên là 73%
=> Trong 0,1 mol Cu sẽ có 0,1.73% = 0,073 mol 63Cu
=> Trong 0,1 mol Cu sẽ có 0,1 - 0,073 = 0,027 mol 65Cu
nguyên tử khối của 2 đồng vị của đồng hơn kém nhau 2đvC
muốn tính % của 65Cu thì lấy |63-63,54|/2=0,27=27%
tương tự % của 63Cu = |65-63,54|/2 = 0,73 = 73%
gọi x là thành phần phần trăm của đồng vị 65Cu
(65x+63(100-x))/100=63,54
=> x=27% 65Cu ,vậy thành phần 63Cu là 73%