Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

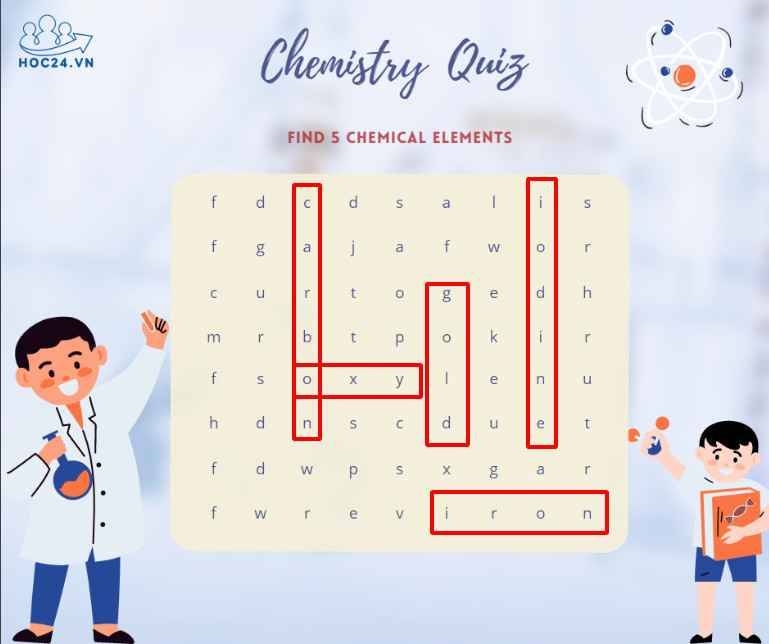
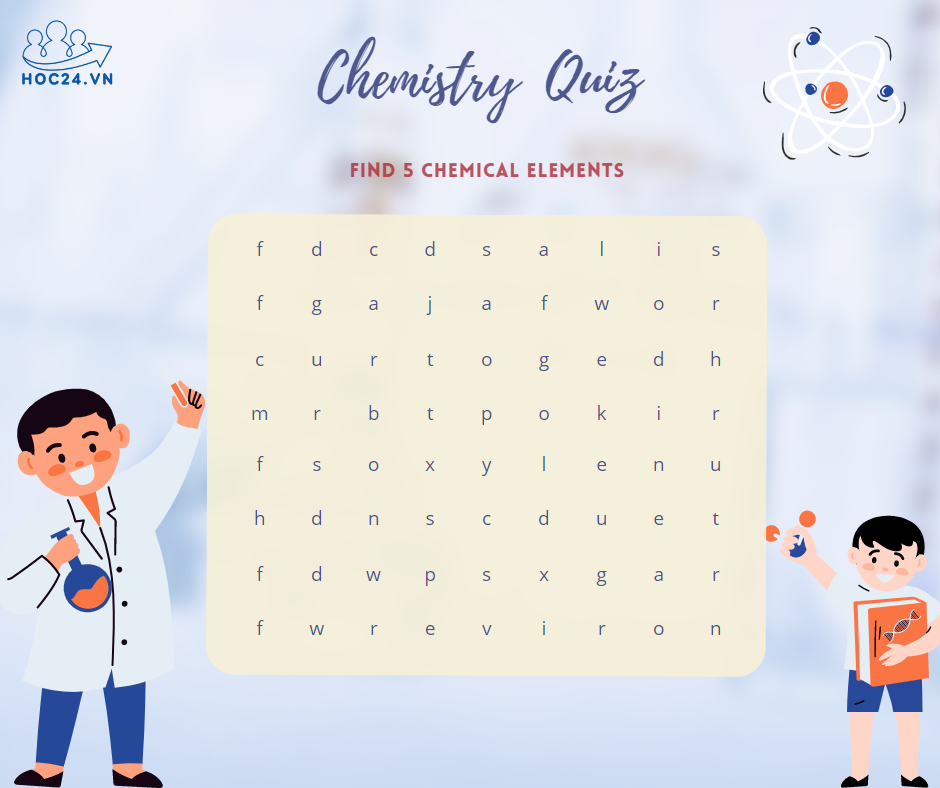
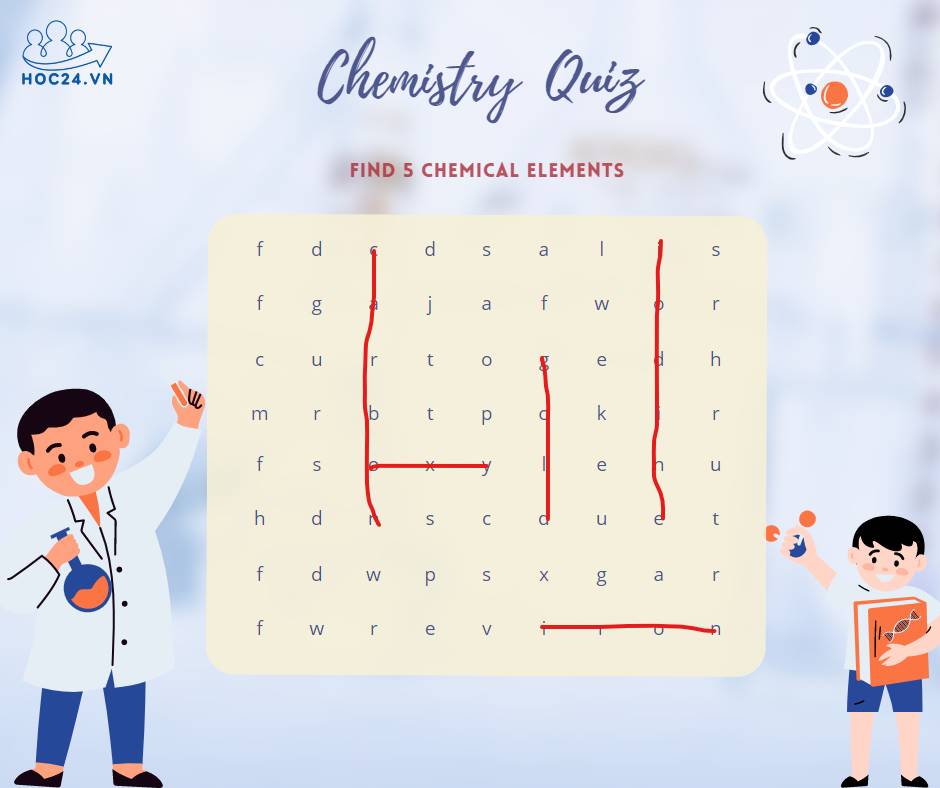
*cái oxy em k chắc á cô:<< em tìm được mấy nguyên tố này th ạ:<.

Cho: Cracking butan → hỗn hợp X (ankan + anken)
- Phản ứng với Br\(_{2}\) dư:
- Khí thoát ra = 60% thể tích X → khí HBr
- Brom phản ứng = 25,6g → số mol Br\(_{2}\) = 0,16 mol = số mol anken (vì anken + Br\(_{2}\) → sản phẩm cộng)
- Khối lượng dung dịch brom tăng 5,6g → Br\(_{2}\) bị hấp thụ (tạo sản phẩm cộng).
Bước 1: Gọi tổng mol hỗn hợp X = \(n\).
- Khí thoát ra = 0,6 \(n\) mol (HBr)
- Anken = 0,16 mol → ankan = \(n - 0 , 16\) mol
Bước 2: Tính mol CO\(_{2}\) và H\(_{2}\)O khi đốt cháy:
- Butan (C4) → mỗi mol cho 4 mol C và 10 mol H (ankan) hoặc 8 mol H (anken)
- CO\(_{2}\) = \(4 n\) mol
- H\(_{2}\)O = \(\frac{1}{2} \times\) tổng số mol H trong hỗn hợp
Tính tổng H:
\(H = 10 \times \left(\right. n - 0.16 \left.\right) + 8 \times 0.16 = 10 n - 1.6 + 1.28 = 10 n - 0.32\)
Nên:
\(b = \frac{H}{2} = \frac{10 n - 0.32}{2} = 5 n - 0.16\)
Kết quả:
\(a = 4 n , b = 5 n - 0.16\)

- số mol Br2 phản ứng: nBr2 = 6,4 / 160 = 0,04 mol → phản ứng với các hiđrocacbon không no trong X.
- hỗn hợp Y thoát ra: V = 4,704 lít → nY = 4,704 / 22,4 = 0,21 mol
- tỉ khối hơi Y so với H2: M̄ = 117/7 ≈ 16,71 g/mol → khối lượng Y = n·M̄ = 0,21·16,71 ≈ 3,51 g
- m isobutan = khối lượng Y + khối lượng phần đã phản ứng với Br2 = 3,51 + 6,4 = 9,91 g ≈ 9,92 g
kết quả: m ≈ 9,92 g

Thành phần chính của thuốc muối là natri hiđrôcacbonat, CTHH: NaHCO3. Trong dạ dày thường chứa dung dịch axit. Người bị đau dạ dày là người có nồng độ dung dịch axit HCl cao làm dạ dày bị bào mòn. NaHCO3 dùng để làm thuốc trị đau dạ dày vì nó làm giảm hàm lượng dung dịch HCl có trong dạ dày nhờ có phản ứng hóa học.
NaHCO3 + HCl → NaCl + CO2 + H2O
Thành phần chính của thuốc muối nabica là natri hidrocacbonat (NaHCO3).
Cơ chế hoạt động của thuốc: Trong dạ dày có 1 lượng axit HCl giúp hòa tan các loại muối khó tan trong quá trình ăn uống. Khi axit dạ dày tăng cao, nếu uống thuốc muối nabica thì NaHCO3 trong thuốc muối tác dụng với axit HCl trong dạ dày theo phương trình hóa học:
NaHCO3 + HCl \(\rightarrow\) NaCl + CO2\(\uparrow\) + H2O.
Lượng axit thừa trong dạ dày đã tác dụng với NaHCO3 có trong thuốc muối nabica, do vậy không còn, nhờ vậy người bị ợ chua, thừa axit không còn bị như vậy nữa.

- Dòng chứa tất cả các axit là dòng D.
- Tên các axit đó là
- \(H_3BO_3\) - Axit boric
- \(H_2SO_4\) - Axit sunfuric
- \(H_2SO_3\) - Axit sunfurơ
- \(HCl\) - Axit clohydric
- \(HNO_3\) - Axit nitric
Vừa qua nó bị lỗi dòng, cô gửi lại nhé:
Dòng chứa tất cả các chất axit là dòng D.
\(H_3BO_3-\text{Axit boric}\)
\(H_2SO_4-\text{Axit sunfuric}\)
\(H_2SO_3-\text{Axit sunfurơ}\)
\(HCl-\text{Axit clohiđric}\)
\(HNO_3-\text{Axit nitric}\)

phản ứng với Br2: các hiđrocacbon không no + Br2 → dẫn xuất brom
khối lượng Br2 phản ứng = 55,23 g → nBr2 = 55,23/160 ≈ 0,345 mol
hỗn hợp Y còn lại là các hiđrocacbon no (CH4, C2H6…)
đốt cháy Y: CxHy + O2 → CO2 + H2O
hấp thụ CO2, H2O vào Ba(OH)2: CO2 + Ba(OH)2 → BaCO3↓, H2O tạo dung dịch Z chứa Ba²⁺ dư
thêm NaOH: Ba²⁺ + OH⁻ → BaCO3↓
nNaOH = 0,02 mol → xác định Ba²⁺ và HCO3⁻
từ số mol khí, tính lại m isobutan ban đầu = 25,8 g
các phương trình hóa học chính:
- C4H10 → C4H8 + H2 (tách H2)
- C4H10 → CH4 + C3H6 (cracking)
- C4H10 → C2H6 + C2H4 (cracking)
- CxHy + Br2 → CxHyBrz
- Y + O2 → CO2 + H2O
- CO2 + Ba(OH)2 → BaCO3↓ + H2O
- Ba²⁺ + OH⁻ → BaCO3↓
kết quả: m = 25,8 g

gọi x = nC2H2, y = nCH4 còn lại, z = nH2. từ phản ứng: z = 3x. tỉ khối: (26x +16y +2z)/(x+y+z) = 10 ⇒ (26x+16y+6x)/(4x+y)=10 ⇒ 32x+16y=40x+10y ⇒ y=4x/3. hiệu suất = nCH4 chuyển thành C2H2 / nCH4 ban đầu = x / (x + y) = x / (x + 4x/3) = 3/7 ≈ 42,86%.


Áp dụng định luật bảo toàn Clo, ta được:
\(\%Cl\left(pư\right)=\%Cl\left(sp\right)\)
=>\(32,85\%=24,2\%+\left(2a\right)\%\)
=>\(32,85=24,2+a\cdot2\)
=>\(a\cdot2=32,85-24,2=8,65\)
=>\(a=\dfrac{8.65}{2}=4.325\)
Áp dụng định luật bảo toàn Clo, ta được:
%Cl(pư)=%Cl(sp)%��(�ư)=%��(��)
=>32,85%=24,2%+(2a)%32,85%=24,2%+(2�)%
=>32,85=24,2+a⋅232,85=24,2+�⋅2
=>a⋅2=32,85−24,2=8,65�⋅2=32,85−24,2=8,65
=>a=8.652=4.325