Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\)
Phương trình hóa học : \(Fe + 2HCl \to FeCl_2 + H_2\)
Theo PTHH :
\(n_{HCl} = 2n_{H_2} = 0,3(mol)\\ n_{Fe} = n_{H_2} = 0,15(mol)\)
Vậy :
\(m_{HCl} = 0,3.36,5 = 10,95(gam) \\m_{Fe} = 0,15.56 = 8,4(gam)\)
b)
Bảo toàn khối lượng :
\(m_{Fe} + m_{HCl} = m_{FeCl_2} + m_{H_2} \\m_{FeCl_2} = 10,95 + 8,4 - 0,15.2 = 19,05(gam)\)
Fe + 2HCl-> FeCl2 + H2
theo phương trình:1 2 1 1 theo đề bài: 0,15 0,3 0,15 0,15 Số mol của H2: nH2=3,361:22,4≈0,15(mol) a)Khối lượng của các chất lần lượt là
mFe=0,15.56=8,4(g)mFe=0,15.56=8,4(g)
mHCl=0,3.36,5=10,95(g).mHCl=0,3.36,5=10,95(g).
b) Khối lượng của FeCl2: mFeCl2=0,15.127=19,059(g)

a) PTPU

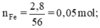
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (l)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)

a, nFe = 11,2/56 = 0,2 (mol)
b, PTHH: Fe + 2HCl -> FeCl2 + H2
Mol: 0,2 ---> 0,4 ---> 0,2 ---> 0,2
mFeCl2 = 0,2 . 127 = 25,4 (g)
c, VH2 = 0,2 . 22,4 = 4,48 (l)
d, CMddHCl = 0,4/0,4 = 1M

a.b.\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,3 0,6 0,3 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
c. Cách 1:
\(m_{FeCl_2}=0,3.127=38,1g\)
Cách 2:
\(m_{HCl}=0,6.36,5=21,9g\)
\(m_{H_2}=0,3.2=0,6g\)
Áp dụng ĐLBTKL, ta có:
\(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(\Rightarrow m_{FeCl_2}=\left(16,8+21,9\right)-0,6=38,1g\)

Lời giải Ta có:
\(F e + 2 H C l \rightarrow F e C l_{2} + H_{2}\)
- Tính số mol Fe tham gia:
\(n\left(\right.Fe\left.\right)=\frac{m}{M}=\frac{2,8\text{g}}{56\text{g}/\text{mol}}=0,05\text{mol}.\)
- Tỉ lệ mol từ phương trình: \(1molFe\rightarrow1molH_2\).
Vậy số mol \(H_{2}\): \(n\left(\right.H_2\left.\right)=0,05\text{mol}.\)
a) Thể tích khí hidro ở ĐKTC:
\(V_{H_2}=n\cdot V_{m}=0,05\cdot22,4=1,12\text{L}.\)
b) Khối lượng axit HCl cần: từ phương trình 1 mol Fe cần 2 mol HCl, nên
\(n\left(\right.HCl\left.\right)=2\cdot n\left(\right.Fe\left.\right)=2\cdot0,05=0,10\text{mol}.\)
Lấy \(M_{HCl}=36,5\text{g}/\text{mol}\), ta có
\(m\left(\right.HCl\left.\right)=n\cdot M=0,10\cdot36,5=3,65\text{g}.\)
Kết luận:
- a) Thể tích \(H_{2}\) ở ĐKTC: 1,12 L.
- b) Khối lượng HCl cần: 3,65 g.
\(Fe+2HCl\to FeCl_2+H_2\)
0,05 0,1 0,05 0,05
a, số mol sắt tham gia phản ứng là:
\(n_{Fe}=\frac{m_{Fe}}{M_{Fe}}=\frac{2,8}{56}=0,05\left(mol\right)\)
thể tích khí hidro thu được ở ĐKTC là:
\(V_{H2}=22,4\cdot n_{H2}=22,4\cdot0,05=1,12\left(L\right)\)
b, khối lượng axit clohidric cần dùng là:
\(m_{HCl}=n_{HCl}\cdot M_{HCl}=0,1\cdot36,5=3,65\left(g\right)\)

\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{Fe}=0,1\left(mol\right)\)
a, \(m_{FeCl_2}=0,1.\left(56+35,5.2\right)=12,7\left(g\right)\)
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)

Câu 1:
\(n_{Fe}=\dfrac{11,2}{56}=0,2(mol)\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{H_2}=n_{FeCl_2}=0,2(mol);n_{HCl}=0,4(mol)\\ a,V_{H_2}=0,2.22,4=4,48(l)\\ b,m_{HCl}=0,4.36,5=14,6(g)\\ c,m_{FeCl_2}=0,2.127=25,4(g)\)
Câu 2:
\(n_{Fe}=\dfrac{1,4}{56}=0,025(mol)\)
Theo PT bài 1: \(n_{HCl}=0,05(mol);n_{H_2}=0,025(mol)\\ a,m_{HCl}=0,05.36,5=1,825(g)\\ b,V_{H_2}=0,025.22,4=0,56(l)\)
Câu 3:
\(4Al+3O_2\xrightarrow{t^o}2Al_2O_3\\ n_{Al}=\dfrac{2,4.10^{22}}{6.10^{23}}=0,04(mol)\\ \Rightarrow n_{O_2}=0,03(mol);n_{Al_2O_3}=0,02(mol)\\ a,V_{O_2}=0,03.22,4=0,672(l)\Rightarrow V_{kk}=0,672.5=3,36(l)\\ b,m_{Al_2O_3}=0,02.102=2,04(g)\)
Câu 4:
\(S+O_2\xrightarrow{t^o}SO_2\\ a,ĐC:S,O_2\\ HC:SO_2\\ b,n_{O_2}=1,5(mol)\\ \Rightarrow V{O_2}=1,5.22,4=33,6(l)\\ c,d_{S/kk}=\dfrac{32}{29}>1\)
Vậy S nặng > kk

nH2 = \(\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo pt : nFe = nH2 = 0,2(mol)
=> mFe = 0,2.56=11,2g
PTHH:Fe+2HCl---FeCl2+H2 (1)
áp dụng công thức: n=v/22,4
nH2=4,48/22,4=0,2 mol
theo pt(1) có
nFe/nH2=1/1
nFe= 1/1*0,2=0,2 mol
ADCT: m=n*M
mFe= 0,2 *56 =11,2 g