Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
+ n M O H = 2 n M 2 C O 3 ⇒ 26 . 28 % M + 17 = 2 . 8 , 97 2 M + 60 ⇒ M = 39 ( K ) n K O H = 0 , 13 + n R C O O K = n R C O O R ' = n R ' O H n H O H ⏟ 26 . 72 % 18 + n R ' O H ⏟ ? = 2 n H 2 ⏟ 0 , 57 ⇒ n R C O O K = n R C O O R ' = n R ' O H = 0 , 1 Y g ồ m R C O O K : 0 , 1 m o l v à K O H d ư : 0 , 03 m o l % m R C O O K = 10 , 08 - 0 , 03 . 56 10 , 08 = 83 , 33 % ≈ 85 %
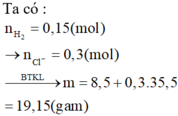

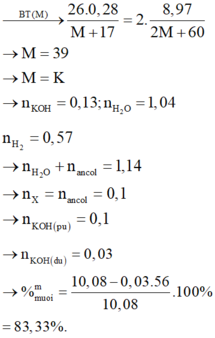

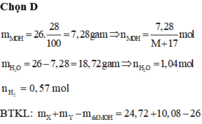
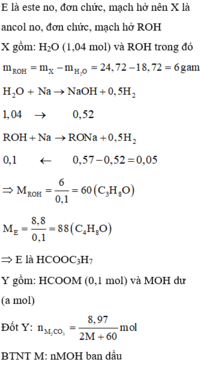

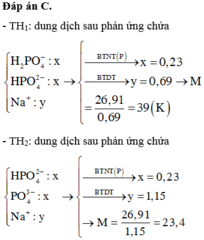
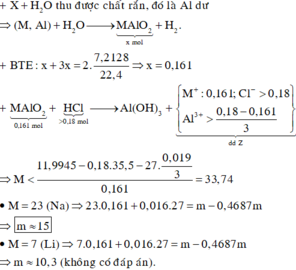
Ta có phản ứng:
X + HCl \(\rightarrow\) XCl + 1/2H2 (1)
m 36,5x 26,6 g x (g)
Dung dịch Y chứa XCl và HCl dư (có cùng nồng độ nên sẽ có cùng số mol).
Nếu gọi x là số mol của XCl thì 0,4 - x sẽ là số mol của HCl dư. Do đó: x = 0,4 - x, suy ra: x = 0,2 (mol).
Áp dụng định luật bảo toàn khối lượng cho phương trình (1), thu được: m + 36,5x = 26,6 + x. Như vậy: m = 19,5 (g).
2X + Cl2 \(\rightarrow\) 2XCl (2)
m 0,1.71 m1 (g)
m1 = m + 7,1 = 26,6 (g).
#Tien Xét trường hợp X dư thì sao?
X không thể dư vì dd Y chứa 2 chất tan, do đó chắc chắn HCl phải dư và X đã hết.
X là kim lại kiềm. Tại sao không thể là chất tan?
Bạn phải xem lại khái niệm thế nào là chất tan, kim loại không bao giờ xếp vào loại chất tan.
nếu X dư vẫn có 2 chất tan là MCl và MOH (do X dư tác dụng với H2O)
vậy nên cô giáo phải xét thêm trường hợp X dư