Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

Bước 1: Viết các phản ứng chính
- Đốt cháy hỗn hợp Mg, Fe trong O₂:
\(M g + \frac{1}{2} O_{2} \rightarrow M g O\)\(F e + \frac{3}{4} O_{2} \rightarrow F e_{3} O_{4}\)
Lưu ý: Thông thường, sắt cháy tạo Fe₃O₄ (oxi hóa sắt hỗn hợp Fe²⁺ và Fe³⁺).
Bước 2: Gọi số mol của Mg và Fe là:
\(n_{M g} = x \left(\right. m o l \left.\right) n_{F e} = y \left(\right. m o l \left.\right)\)
Bước 3: Viết các biểu thức khối lượng ban đầu:
\(24 x + 56 y = 4 , 16 \left(\right. 1 \left.\right)\)
Bước 4: Viết khối lượng oxit sau phản ứng
Khối lượng oxit X = 5,92 g gồm:
- MgO: khối lượng = \(24 x + 16 x = 40 x\) g
- Fe₃O₄: khối lượng = \(56 y + 64 y / 3 = 56 y + \frac{64}{3} y = \frac{168 y + 64 y}{3} = \frac{232 y}{3}\) g
Vì Fe₃O₄ gồm 3 Fe (3 × 56 =168) và 4 O (4 × 16 =64), tổng 232 g/mol.
Vậy khối lượng Fe₃O₄ tạo ra từ y mol Fe là:
\(\text{Fe}_{3} \text{O}_{4} = \frac{232}{3} y\)
Tổng khối lượng oxit:
\(40 x + \frac{232}{3} y = 5 , 92 \left(\right. 2 \left.\right)\)
Bước 5: Giải hệ (1) và (2)
\(\left{\right. 24 x + 56 y = 4 , 16 \\ 40 x + \frac{232}{3} y = 5 , 92\)
Bước 6: Dung dịch Y chứa:
- MgCl₂: số mol = \(x\) (từ MgO + 2HCl → MgCl₂ + H₂O)
- FeCl₂ và FeCl₃ (từ Fe₃O₄ hòa tan trong HCl theo phản ứng hỗn hợp)
Phản ứng hòa tan Fe₃O₄ trong HCl:
\(F e_{3} O_{4} + 8 H C l \rightarrow F e C l_{2} + 2 F e C l_{3} + 4 H_{2} O\)
Số mol FeCl₂ = 1 mol, FeCl₃ = 2 mol trên 1 mol Fe₃O₄.
Với y mol Fe nguyên tố:
\(n_{F e_{3} O_{4}} = \frac{y}{3} \left(\right. \left(\text{v} \overset{ˋ}{\imath} \&\text{nbsp};\text{Fe}\right)_{3} O_{4} \&\text{nbsp};\text{c} \overset{ˊ}{\text{o}} \&\text{nbsp};\text{3}\&\text{nbsp};\text{Fe} \left.\right)\)
Do đó:
- \(n_{F e C l_{2}} = \frac{y}{3}\)
- \(n_{F e C l_{3}} = 2 \times \frac{y}{3} = \frac{2 y}{3}\)
Bước 7: Kết tủa Z khi cho NaOH dư:
- MgCl₂ + 2NaOH → Mg(OH)₂↓ + 2NaCl
- FeCl₂ + 2NaOH → Fe(OH)₂↓ + 2NaCl
- FeCl₃ + 3NaOH → Fe(OH)₃↓ + 3NaCl
Số mol các kết tủa hydroxyd:
- Mg(OH)₂: \(x\) mol
- Fe(OH)₂: \(\frac{y}{3}\) mol
- Fe(OH)₃: \(\frac{2 y}{3}\) mol
Bước 8: Nung kết tủa Z (gồm Mg(OH)₂, Fe(OH)₂, Fe(OH)₃) đến khối lượng không đổi (6 g):
- Mg(OH)₂ → MgO:
Khối lượng giảm 18 g/mol (do mất H₂O)
M₁(Mg(OH)₂) = 58 g/mol, M₁(MgO) = 40 g/mol
Tỉ lệ: 40/58 - Fe(OH)₂ → FeO:
M(Fe(OH)₂) = 89.86 g/mol, M(FeO) = 71.84 g/mol
Tỉ lệ: 71.84/89.86 ≈ 0.8 - Fe(OH)₃ → Fe₂O₃ (để đơn giản) hoặc Fe₃O₄ (phức tạp hơn)
Ở đây chúng ta giả sử Fe(OH)₃ → Fe₂O₃:
M(Fe(OH)₃) = 106.87 g/mol, M(Fe₂O₃) = 159.69 g/mol
Hai mol Fe(OH)₃ tạo thành 1 mol Fe₂O₃. Nên cần tính theo số mol tương ứng.
Bước 9: Viết biểu thức khối lượng sau nung:
Khối lượng sau nung = 6 g
\(40 x + 0.8 \times 89.86 \times \frac{y}{3} + \left(\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{l}ượ\text{ng}\&\text{nbsp};\text{Fe}(\text{OH})\right)_{3} \&\text{nbsp};\text{sau}\&\text{nbsp};\text{nung} = 6\)
Phần Fe(OH)₃ chuyển thành Fe₂O₃:
\(\frac{2 y}{3} \&\text{nbsp};\text{mol}\&\text{nbsp};\text{Fe}(\text{OH})_{3} \rightarrow \frac{y}{3} \&\text{nbsp};\text{mol}\&\text{nbsp};\text{Fe}_{2} O_{3}\)
Khối lượng Fe(OH)₃ ban đầu:
\(106.87 \times \frac{2 y}{3}\)
Khối lượng Fe₂O₃ sau nung:
\(159.69 \times \frac{y}{3}\)
Khối lượng Fe(OH)₃ sau nung = \(\frac{159.69}{106.87} \times \left(\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{l}ượ\text{ng}\&\text{nbsp};\text{Fe}(\text{OH})\right)_{3}\) ban đầu
≈ \(1.495 \times 106.87 \times \frac{2 y}{3} = 159.69 \times \frac{y}{3}\)
Bước 10: Viết lại biểu thức khối lượng sau nung
\(40 x + 0.8 \times 89.86 \times \frac{y}{3} + 159.69 \times \frac{y}{3} = 6\)
Tính từng phần:
- \(0.8 \times 89.86 \times \frac{y}{3} = 71.89 \times \frac{y}{3} = 23.96 y\)
- \(159.69 \times \frac{y}{3} = 53.23 y\)
Nên:
\(40 x + 23.96 y + 53.23 y = 6 \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } 40 x + 77.19 y = 6 \left(\right. 3 \left.\right)\)
Bước 11: Giải hệ (1), (2), (3):
\(\left{\right. 24 x + 56 y = 4.16 \left(\right. 1 \left.\right) \\ 40 x + \frac{232}{3} y = 5.92 \left(\right. 2 \left.\right) \\ 40 x + 77.19 y = 6 \left(\right. 3 \left.\right)\)
Hệ (2) và (3) gần giống, chênh lệch nhỏ do xấp xỉ, ta dùng (1) và (3):
Từ (1):
\(24 x = 4.16 - 56 y \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } x = \frac{4.16 - 56 y}{24}\)
Thay vào (3):
\(40 \times \frac{4.16 - 56 y}{24} + 77.19 y = 6\)\(\frac{40 \times 4.16}{24} - \frac{40 \times 56 y}{24} + 77.19 y = 6\)\(6.93 - 93.33 y + 77.19 y = 6\)\(6.93 - 16.14 y = 6\)\(- 16.14 y = 6 - 6.93 = - 0.93\)\(y = \frac{0.93}{16.14} \approx 0.0576 \&\text{nbsp};\text{mol}\)
Thay y vào (1):
\(x = \frac{4.16 - 56 \times 0.0576}{24} = \frac{4.16 - 3.225}{24} = \frac{0.935}{24} = 0.0389 \&\text{nbsp};\text{mol}\)
Bước 12: Tính m gam kết tủa AgCl khi cho Y tác dụng với AgNO₃ dư
Dung dịch Y chứa:
- MgCl₂: số mol = \(x = 0.0389\)
- FeCl₂: \(y / 3 = 0.0576 / 3 = 0.0192\)
- FeCl₃: \(2 y / 3 = 0.0384\)
Khi cho AgNO₃ dư:
- Mỗi mol Cl⁻ tạo 1 mol AgCl (kết tủa)
Số mol Cl⁻ tổng:
\(\text{MgCl}_{2} : 2 \times 0.0389 = 0.0778\)\(\text{FeCl}_{2} : 2 \times 0.0192 = 0.0384\)\(\text{FeCl}_{3} : 3 \times 0.0384 = 0.1152\)
Tổng số mol Cl⁻:
\(0.0778 + 0.0384 + 0.1152 = 0.2314\)
Bước 13: Tính khối lượng kết tủa AgCl
Khối lượng mol AgCl = 143.5 g/mol
\(m = 0.2314 \times 143.5 = 33.2 \&\text{nbsp};\text{g}\)
Kết luận:
\(\boxed{m = 33.2 \&\text{nbsp};\text{g}}\)
Tk

a)
Mg + 2HCl --> MgCl2 + H2
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
MgCl2 + 2KOH + 2KCl + Mg(OH)2
FeCl3 + 3KOH --> 3KCl + Fe(OH)3
Mg(OH)2 --to--> MgO + H2O
2Fe(OH)3 --to--> Fe2O3 + 3H2O
b) Gọi số mol Mg, Fe2O3 là a, b (mol)
Theo PTHH: \(a=n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PTHH: \(n_{MgO}=n_{Mg}=a=0,15\left(mol\right)\)
=> \(n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=\dfrac{22-0,15.40}{160}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Fe_2O_3\left(bđ\right)}=n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=0,1\left(mol\right)\)
=> b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,15.24}{0,15.24+0,1.160}.100\%=18,37\%\\\%m_{Fe_2O_3}=\dfrac{0,1.160}{0,15.24+0,1.160}.100\%=81,63\%\end{matrix}\right.\)

CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,34 ←0,34
CO + O(Oxit) → CO2
Nhận thấy:
nO = nCO2
mX = mO (oxit) + mY
=> mY = 37,68 – 16 . 0,34 = 32,24g

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
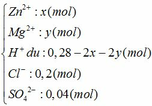
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
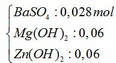
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam