Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Fe}=\dfrac{6,72}{56}=0,12\left(mol\right)\\ Fe+H_2SO_{4\left(loãng\right)}\rightarrow FeSO_4+H_2\uparrow\\ Mol:0,12\rightarrow0,12\rightarrow0,12\rightarrow0,12\\ V_{H_2}=0,12.22,4=2,688\left(l\right)\\ m_{FeSO_4}=0,12.152=18,24\left(g\right)\\ PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\\ Mol:0,04\leftarrow0,12\rightarrow0,08\\ m_{Fe}=0,08.56=4,48\left(g\right)\)

\(n_{H_2\left(đkc\right)}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ n_{Al}=n_{AlCl_3}=\dfrac{2}{3}.n_{H_2}=\dfrac{2}{3}.0,1=\dfrac{1}{15}\left(mol\right)\\ \Rightarrow m_{Al}=27.\dfrac{1}{15}=1,8\left(g\right)\\ m_{AlCl_3}=\dfrac{1}{15}.133,5=8,9\left(g\right)\)
\(n_{H_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
\(\dfrac{1}{15}\)<--------------\(\dfrac{1}{15}\)<-----0,1
=> \(m_{Al}=\dfrac{1}{15}.27=1,8\left(g\right)\)
=> \(m_{AlCl_3}=\dfrac{1}{15}.133,5=8,9\left(g\right)\)

nFe = 11,2/56 = 0,2 (mol)
PTHH: Fe + 2HCl -> FeCl2 + H2
Mol: 0,2 ---> 0,4 ---> 0,2 ---> 0,2
VH2 = 0,2 . 22,4 = 4,48 (l)
PTHH: CuO + H2 -> (to) Cu + H2O
Mol: 0,2 <--- 0,2 ---> 0,2
mCu = 0,2 . 64 = 12,8 (g)

PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
a, \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Al}=0,1.27=2,7\left(g\right)\)
b, \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}n_{H_2}=0,05\left(mol\right)\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1\left(g\right)\)
c, \(n_{H_2SO_4}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2SO_4}=\dfrac{0,15}{1,5}=0,1\left(l\right)=100\left(ml\right)\)

a, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
b, Theo PT: \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.24,79=4,958\left(l\right)\)
c, Theo PT: \(n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\)
\(\Rightarrow m_{MgCl_2}=0,2.95=19\left(g\right)\)

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{Zn}=\dfrac{4,8}{65}=\dfrac{24}{325}\left(mol\right)\)
Đến đây thì ra số mol hơi xấu, bạn xem lại đề nhé.

\(n_{Al}=\dfrac{2,7}{27}=0,1mol\\ a.2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,15 0,05 0,15
\(b.V_{H_2}=0,15.24,79=3,7185l\\ c.m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1g\\ d.C_{M_{H_2SO_4}}=\dfrac{0,15}{0,4}=0,375M\)
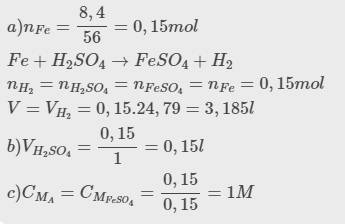
2Al + 3H2SO4 -- > Al2(SO4)3 + 3H2
0,3 0,45 0,15 0,45
nAl = 8,1 / 27 = 0,3(mol)
\(VH_2=0,45.22,4=10,08\left(g\right)\)
\(m\left(muối\right)=0,15.342=51,3\left(g\right)\)
\(H_2+CuO\rightarrow Cu+H_2O\)
0,45 0,45
mCu = 0,45 . 64 = 28,8(g)
bạn giải thích dùm mình tại sao 3H2So4 với 3H2 lại là 0,45 mol ko
có số gam Al là 0,3 trên pt
bn coi chỉ số của mỗi chất trong pt:
2Al + 3H2SO4 -- > Al2(SO4)3 + 3H2
chỉ số của Al = 2
H2SO4 và H2 = 3
tính số mol của H2SO4 theo Al bằng cách lấy chỉ số của H2SO4 chia cho chỉ số của Al nhân với số mol của Al
vd nH2SO4 = 3/2 . 0,3 = 0,45(mol)
nAl(2SO4)3 = 1/2 . 0,3 = 0,15(mol)
nH2 = 3/2 . 0,3 = 0,45(mol)
tính theo số mol của chất nào trong pthh thì bạn lấy chỉ số của chất tính theo chất đó chia cho chỉ số của chất biết số mol nhân với số mol chất đó
vd là Al có chỉ số 2
H2SO4 có chỉ số 3 trên pt
tính số mol H2SO4 theo Al thì lấy chỉ số của H2SO4 chia chỉ số của Al nhân với số mol Al .
Bạn hiểu chưa.-.?
À mình hiểu rồi cảm ơn bạn