
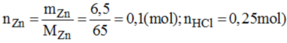
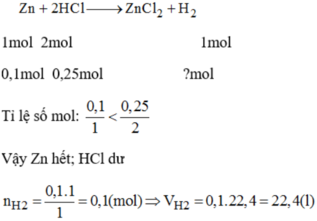
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

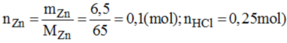
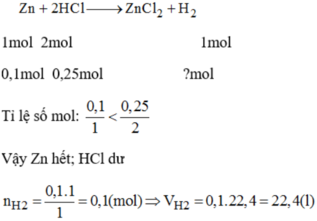

nZn=0,1 mol
nHCl=0,25 mol
Zn +2HCl=>ZnCl2+H2
Pứ 0,1 mol>=0,2 mol. =>0,1 mol
Dư 0,05 mol
VH2=2,24lit
HCl còn dư:0,05 mol
=>mHCl dư=1,825g

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(n_{HCl}=2n_{Zn}=0,2\left(mol\right)\Rightarrow C_{M_{HCl}}=\dfrac{0,2}{0,15}=\dfrac{4}{3}\left(M\right)\)
c, \(n_{H_2}=n_{Zn}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

`Zn + 2HCl -> ZnCl_2 + H_2`
`0,1` `0,2` `0,1` `(mol)`
`n_[Zn]=[6,5]/65=0,1(mol)`
`a)V_[H_2]=0,1.22,4=2,24(l)`
`b)C%_[HCl]=[0,2.36,5]/200 . 100 =3,65%`
`Zn + HCl -> ZnCl_2 + H_2` `\uparrow`
`n_(Zn) = (6,5)/65 = 0,1 mol`.
`n_(H_2) = 0,1 mol`.
`V(H_2) = 0,1 xx 22,4 = 2,24l`.
`C%(HCl) = (0,2.36,5)/200 xx 100 = 36,5%`.

a)
$Fe + 2HCl \to FeCl_2 + H_2$
n H2 = n Fe = 11,2/56 = 0,2(mol)
V H2 = 0,2.22,4 = 4,48(lít)
b)
n HCl = 2n Fe = 0,2.2 = 0,4(mol)
=> CM HCl = 0,4/0,4 = 1M
c)
$CuO + H_2 \xrightarrow{t^o} Cu + H_2O$
Ta thấy :
n CuO = 64/80 = 0,8 > n H2 = 0,2 nên CuO dư
Theo PTHH :
n CuO pư = n Cu = n H2 = 0,2(mol)
n Cu dư = 0,8 - 0,2 = 0,6(mol)
Vậy :
%m Cu = 0,2.64/(0,2.64 + 0,6.80) .100% = 21,05%
%m CuO = 100% -21,05% = 78,95%

a, \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{ZnCl_2}=n_{Zn}=0,3\left(mol\right)\Rightarrow m_{ZnCl_2}=0,3.136=40,8\left(g\right)\)
b, \(n_{H_2}=n_{Zn}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)

Lời giải Ta có:
\(F e + 2 H C l \rightarrow F e C l_{2} + H_{2}\)
\(n\left(\right.Fe\left.\right)=\frac{m}{M}=\frac{2,8\text{g}}{56\text{g}/\text{mol}}=0,05\text{mol}.\)
a) Thể tích khí hidro ở ĐKTC:
\(V_{H_2}=n\cdot V_{m}=0,05\cdot22,4=1,12\text{L}.\)
b) Khối lượng axit HCl cần: từ phương trình 1 mol Fe cần 2 mol HCl, nên
\(n\left(\right.HCl\left.\right)=2\cdot n\left(\right.Fe\left.\right)=2\cdot0,05=0,10\text{mol}.\)
Lấy \(M_{HCl}=36,5\text{g}/\text{mol}\), ta có
\(m\left(\right.HCl\left.\right)=n\cdot M=0,10\cdot36,5=3,65\text{g}.\)
\(Fe+2HCl\to FeCl_2+H_2\)
0,05 0,1 0,05 0,05
a, số mol sắt tham gia phản ứng là:
\(n_{Fe}=\frac{m_{Fe}}{M_{Fe}}=\frac{2,8}{56}=0,05\left(mol\right)\)
thể tích khí hidro thu được ở ĐKTC là:
\(V_{H2}=22,4\cdot n_{H2}=22,4\cdot0,05=1,12\left(L\right)\)
b, khối lượng axit clohidric cần dùng là:
\(m_{HCl}=n_{HCl}\cdot M_{HCl}=0,1\cdot36,5=3,65\left(g\right)\)