Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

oxi hóa
khử
trừ Au(vàng) và Pt(Bạch kim), giải phóng khí \(H_2\)
Khi đó kim loại bị oxi hóa đến mức oxi hóa cao nhất.
Các sản phẩm khử của \(HNO_3\) là \(NO_2\) (nâu đỏ), NO(khí không màu, hóa nâu ngoài không khí). \(N_2O\) (khí không màu, nặng hơn không khí), \(N_2\) (khí không màu, nhẹ hơn không khí), \(NH_4NO_3\) (muối), Đối với \(HNO_3\) đặc thì sản phẩm khử là \(NO_2\)

Áp dụng bđt \(\sqrt[3]{a_1^3+b_1^3}+\sqrt[3]{b_1^3+b_2^3}+\sqrt[3]{a_3^3+b_3^3}\ge\sqrt[3]{\left(a_1+a_2+a_3\right)^3+\left(b_1+b_2+b_3\right)^3}\)
và bđt \(\left(a+b+c\right)^3\ge27abc\)
Ta thu đc \(M\ge\sqrt[3]{\left(x+y+z\right)^3+\left(\frac{1}{x}+\frac{1}{y}+\frac{1}{z}\right)^3}\ge\sqrt[3]{27abc+\frac{27}{abc}}\)
Đặt \(0< t=abc\le\left(\frac{a+b+c}{3}\right)^3\le\frac{1}{8}\)ta thu được
\(P\ge\sqrt[3]{f\left(t\right)}=\sqrt[3]{27t+\frac{27}{t}}\)
Lại có \(f\left(t\right)=27\left(64t+\frac{1}{t}-63t\right)\ge27\left(2\sqrt{64}-\frac{63}{8}\right)\)
\(\Leftrightarrow f\left(t\right)\ge27\left(16-\frac{63}{8}\right)=\frac{27.65}{8}\)
\(\Rightarrow P\ge\sqrt[3]{\frac{27.65}{8}}=\frac{3}{2}\sqrt[3]{65}\)(Đpcm !)
Nguồn : Team toán tỉnh 9B Tiên Lữ !!!!

\(pH = - \log \left[ {{H^ + }} \right] = - \log {8.10^{ - 8}} \approx 7,1\)
=> Độ pH không phù hợp cho tôm sú phát triển.

Đáp án C
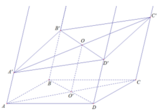
Trên Ax lấy điểm A’ sao cho AA’= x
Trên By lấy điểm B’ sao cho BB’ = y
Trên Cz lấy điểm C’ sao cho CC’ = z
Gọi α là mặt phẳng chứa tia Cz và Dt
Xét (A’B’C’) và α có:
C’ là điểm chung
A’B’ // α
⇒ giao tuyến của α và (A’B’D’) là đường thẳng d đi qua C’ và song song với A’B’
Trong mặt phẳng α , ta có: d cắt Dt tại D’
Gọi O = A C ∩ B D , O ' = A C ' ∩ B ' D '
Xét hình thang AA’C’C có: OO’ là đường trung bình
⇒ O O ' = A A ' + C C ' 2 = x + z 2
Xét tam giác BDD’D có: OO’ là đường trung bình
⇒ O O ' = D D ' + B B ' 2 ⇒ DD’ = x + z – y






nNO3-= nNaNO3 = 0,5.1= 0,5
nH+ = nHCl = 0,5.2+ 0.2.1 = 1,2
gọi x, y, z lần lượt là nAl, nFe, nCu
⇒27x + 56y + 64z = 20,7 (1)
Al + 4H+ + NO3- → Al+3 + NO + 2H2O
Fe + 4H+ +NO3- → Fe+3 + NO + H2O
3Cu + 8H+ + 2NO3- → 3Cu+2 +2NO + 4H2O
theo phương trình nNO = 1/4nH+ = 0,3
vì ban đầu tác dụng thì Al mạnh hơn nên tác dụng trước sau đó đến Fe vì cuối cùng còn 1 kim loại chưa tan hết nên kim loại đó là Cu, vì kim loại còn dư nên muối thu được là Fe(NO3)2
áp dụng định luật bảo toàn e cho cả 2 quá trình
Al → Al+3 + 3e N+5 + 3e → N+2
x → 3y 0,9 ←0,3
Fe → Fe+2 + 2e
y→ 2y
Cu → Cu+2 + 2e
z → 2z
tổng số mol e nhường = tổng số mol nhận
⇒ 3x + 2y + 2z = 0,9 (2)
0
khi 1 nửa Y tác dụng với NaOH dư thì kết tủa thu được là
Fe(OH)3 : y/2 mol
Cu(OH)2 : z/2 mol
khi nung đến khối lượng không đổi thì rắn gồm
Fe2O3 : y/4 mol
CuO : z/2 mol
⇒ 160. y/4. + 80. z/2 = 12 (3)
từ (1), (2) (3) ⇒ x = 0,1
y = 0,15
z = 0,15
%mAl = 0,1.27/20,7 = 13,04%
%mFe = 0,15.56/20,7 =40,58%
%mCu = 100 - 13,04 - 40,58 = 46,38%
nNO3- pư= nNO = 0,3
⇒nNO3-dư = 0,5=0,3=0,2
nCl- = nHCl = 1
CmAl+3 = 0,1/0,7 = 0,14M
CmFe+3 = CmCu+2= 0,15/0,7 = 0,21M
CmNO3- = 0,2/0,7 =0,29M
CmCl- = 1/0,7 = 1,43M
Nung ngoài không khí thì sản phẩm là Fe3O4 mà