Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 4:
\(CH_3-C\equiv CH\underrightarrow{^{AgNO3/NH3}}CH_3-C\equiv CAg\downarrow\)
\(\Rightarrow n_{C3H4}=n_{\downarrow}=\frac{14,7}{147}=0,1\left(mol\right)\)
Dẫn qua KMnO4 dư, khí thoát ra là butan
\(\Rightarrow n_X=\frac{7,84}{22,4}=035\left(mol\right)\)
\(n_{C4H8}=0,35-0,05-0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{C4H8}=0,2.56=11,2\left(g\right)\)

(2)Thổi hỗn hợp qua binh chứa dung dịch AgNO3/NH3 dư. Lọc tách kết tủa, hòa tan kết tủa trong dung dịch HCl dư thu được khí C2H2.
C2H2 + 2AgNO3 + 2NH3 \(\rightarrow\) C2Ag2 \(\downarrow\) + 2NH4NO3
C2Ag2 + 2HCl \(\rightarrow\) C2H2 + 2AgCl \(\downarrow\)
Khí ra khỏi bình chứa dung dịch AgNO3/NH3, thổi tiếp qua dung dịch nước brom dư. Chiết lấy sản phẩm và đun nóng với bột Zn (trong CH3COOH) thu được C2H4 :
C2H4 + Br2 \(\rightarrow\) C2H4Br2
C2H4Br2 + Zn \(\rightarrow\) C2H4 + ZnBr2
Khí ra khỏi bình chứa dung dịch brom là khí C2H6
(1) Nếu ankin có dạng RC\(\equiv\)CH :
RC\(\equiv\)CH + AgNO3 + NH3 \(\rightarrow\) RC\(\equiv\)CAg + NH4NO3
\(\Rightarrow n\left(ankin\right)=\frac{3,4g}{170g\text{/}mol}=0,02mol\) và \(n_{Br_2}\ge2\times n\left(ankin\right)=0,04mol\)
Điều này trái giả thiết, vì số mol Br2 chỉ bằng \(0,2L.0,15mol\text{/}L=0,03mol\)
Vậy ankin phải là C2H2 và như vậy ankan là C2H6, anken là C2H4.
Từ phản ứng :
C2H2 + 2AgNO3 + 2NH3 \(\rightarrow\) C2Ag2 + 2NH4NO3
\(\Rightarrow\) n(C2H2) = 1/2n(AgNO3) = 0,01 mol
Từ các phản ứng :
C2H2 + 2Br2 \(\rightarrow\) C2H2Br4
C2H4 + Br2 \(\rightarrow\) C2H4Br2
\(\Rightarrow\) n(C2H4) = 0,01 mol
\(\Rightarrow\) n(C2H6) = \(\frac{0,672L}{22,4L\text{/}mol}-0,01mol-0,01mol=0,01mol\)
\(\Rightarrow\) Khối lượng của: C2H2: 0,26gam; C2H4: 0,28 gam; C2H6: 0,3 gam.

a) PI : C3H6 +Br2 --> C3H6Br2 (1)
C3H4 +2Br2 --> C3H4Br4 (2)
PII : C3H4 + AgNO3 +NH3 --> C3H3Ag\(\downarrow\) + NH4NO3
nC3H3Ag=0,04(mol)
=> nC3H4=0,04(mol)=> nC3H4( hh đầu)=0,08(mol)
Theo (1,2) : nB2=2nC3H4+nC3H6=0,11
=> nC3H6=0,03(mol) => nC3H6(hh đầu)=0,06(mol)
=>nC2H6(bđ)=0,02(mol)
=> %mC2H6=9,49(%)
%mC3H4=50,63(%)
%mC3H6=39,87(%)
b) C2H6-->2CO2
0,02 --> 0,04
C3H4 --> 3CO2
0,08 --> 0,24
C3H6 --> 3CO2
0,06 --> 0,18
=> \(\Sigma\)nCO2(tạo ra)=0,46(mol)
CO2 + Ba(OH)2 --> BaCO3 +H2O (3)
CO2 + BaCO3 +H2O --> Ba(HCO3)2 (4)
Tho (3,4) : nBaCO3(tạo ra)=0,18(mol)
=> mBaCO3=35,46(g)

Gọi số mol của etilen và propilen lần lượt là x và y mol.
Khối lượng dung dịch sau phản ứng tăng lên chính là khối lượng của hỗn hợp etilen và propilen.
Ta có hệ phương trình:
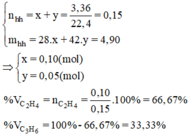

Ta có:
\(n_{H2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(CH_3COOH+Na\rightarrow CH_3COONa+H_2\)
0,1_______________________________0,1
\(CH_3CH_2CHO+Na\underrightarrow{^X}\)
\(m_{CH3COOH}=0,1.64=6,4\left(g\right)\)
\(m_{CH3CH2CHO}=18,6-6,4=12,2\left(g\right)\)
\(CH_3CH_2CHO+H_2O+Br_2\rightarrow C_2H_5COOH+2HBr\)
0,2___________________0,2____________________0,9
\(\Rightarrow m_{Br2}=0,2.80.2=32\left(g\right)\)

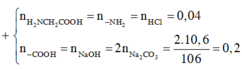
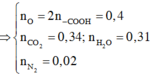

phần trăm khối lượng của ÂlKene là 40%
Phần trăm khối lượng của alkane là 60%
gam
2𝑚alkane=𝑚hnhp−𝑚alkene=2,0−0,8=1,2gam
- Phần trăm khối lượng của alkene:
%malkene=malkenemhn hp×100%=0,82,0×100%=40%%𝑚alkene=𝑚alkene𝑚hnhp×100%=0,82,0×100%=40%Phần trăm khối lượng của alkene là 40% và của alkane là 60%
malkene=0,8malkene=0,8 gam
2 malkene=mhnhp-2,0-0,8=1,2 gam
- phần trăm khối lượng của alkene:
%malkene=malkenemhn
hpx100%=0,82,0x=40%%malkene
=Malkenemhn hpx100%=0,82,0x=40%
- phần trăm khối lượng của alkene:
bsns
Khối lượng alkene = Khối lượng dung dịch tăng = 0,8 g. Khối lượng alkane = 2,0 - 0,8 = 1,2 g. Phần trăm khối lượng: 0.8 %malkene = x 100% = 40% 2.0 %malkane = 100%-40% = 60%
Bài làm: Chỉ có anken phản ứng với Br₂ nên khối lượng tăng chính là khối lượng anken: m(anken) = 0,8 gam m(ankan) = 2,0 – 0,8 = 1,2 gam % m(anken) = (0,8 / 2,0) × 100% = 40% % m(ankan) = 60% Kết luận: Anken: 40% Ankan: 60%
Xác định khối lượng các chất trong hỗn hợp: Khối lượng alkene ( ) = Khối lượng dung dịch tăng thêm = gam. Khối lượng alkane ( ) = Khối lượng hỗn hợp X - Khối lượng alkene Tính phần trăm khối lượng từng chất: Phần trăm khối lượng của alkene: Phần trăm khối lượng của alkane: (Hoặc tính trực tiếp: )
Phân tích đề bài Hỗn hợp X (2,0 gam): Gồm 1 alkene và 1 alkane. Phản ứng: Chỉ có alkene phản ứng với dung dịch . Alkane không phản ứng và thoát ra ngoài. Khối lượng dung dịch tăng thêm (0,8 gam): Đây chính là khối lượng của alkene đã bị giữ lại trong bình do phản ứng cộng với . 2. Tính toán Khối lượng của alkene: Khối lượng của alkane: Phần trăm khối lượng của alkene: Phần trăm khối lượng của alkane: Kết luận Phần trăm khối lượng của alkene là 40%. Phần trăm khối lượng của alkane là 60%.
Khi dẫn hỗn hợp khí X gồm alkene và alkane qua dung dịch Br2 trong CCl4, chỉ có alkene phản ứng cộng với Brom, còn alkane không phản ứng. Khối lượng dung dịch tăng thêm chính là khối lượng của alkene đã phản ứng.
malkene mdung dch tăng = 0,8 gam
Tính khối lượng và phần trăm alkane
Khối lượng của alkane trong hỗn hợp ban đầu là:
Lalkane mx - malkene = 2,0 – 0,8 = 1,2 gam
Phần trăm khối lượng của alkene:
malkene 0,8 %malkene × 100% = × 100% = mx 2,0
Phần trăm khối lượng của alkane:
%malkane = 100% - %malkene = 100% - 40% =60%
Phần trăm khối lượng của alkene là 40% và alkane là 60%.
Chỉ có anken phản ứng với Brz nên khối lượng tăng chính là khối lượng anken: m(anken) = 0,8 gam m(ankan) = 2,0 - 0,8 = 1,2 gam % m(anken) = (0,8 / 2.0) x 100% = 40% % m(ankan) = 60% Kết luận: Anken: 40% Ankan: 60%
Thông tin tổng quan do AI tạo
Dưới đây là lời giải chi tiết cho bài toán hóa học trong ảnh:
1. Phân tích đề bài
Hỗn hợp X (2,0 gam): Gồm một alkene và một alkane.
Phản ứng với dung dịch
B
r
2
𝐵
𝑟
2
: Chỉ có alkene phản ứng và bị giữ lại trong dung dịch. Alkane không phản ứng và thoát ra ngoài.
Khối lượng dung dịch tăng thêm (0,8 gam): Đây chính là khối lượng của alkene đã bị hấp thụ.
Phần trăm khối lượng của alkene là 40%. Phần trăm khối lượng của alkane là 60%.
Alkene 40% : Alkane 60%
Hoặc lấy 100℅ -40℅=60℅
Alkene : 40%
Alkene: 60%
\(m_{alkene} = \Delta m_{tăng} = 0,8\) gam.