Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,3 0,3
\(V_{H_2}=0,3.22,4=6,72l\\ n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12g\\ pthh:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\\ LTL:\dfrac{0,12}{1}>\dfrac{0,3}{3}\)
=> Fe2O3 dư
\(n_{Fe}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\\
m_{Fe}=0,2.56=11,2g\)
a.\(n_{Zn}=\dfrac{19,5}{65}=0,3mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,3 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,12 > 0,3 ( mol )
0,3 0,2 ( mol )
\(m_{Fe}=0,2.56=11,2g\)

nZn = 19.5/65 = 0.3 (mol)
Zn + 2HCl => ZnCl2 + H2
0.3................................0.3
VH2 = 0.3 * 22.4 = 6.72 (l)
nFe2O3 = 19.2/160 = 0.12 (mol)
Fe2O3 + 3H2 -t0-> 2Fe + 3H2O
Bđ: 0.12......0.3
Pư: 0.1........0.3..........0.2
Kt: 0.02.........0...........0.2
mFe = 0.2 * 56 = 11.2 (g)

\(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{H_2}=n_{Zn}=0,3\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\\ b,n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\\ PTHH:3H_2+Fe_2O_3\rightarrow\left(t^o\right)2Fe+3H_2O\\ Vì:\dfrac{0,3}{3}< \dfrac{0,12}{1}\Rightarrow Fe_2O_3dư,H_2.hết\\ n_{Fe}=\dfrac{2}{3}.n_{H_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ m_{Fe}=0,2.56=11,2\left(g\right)\)

a) Nồng độ phần trăm dd KCl:
\(C\%_{ddKCl}=\dfrac{200}{600}.100\approx33,333\%\)
b) Nồng độ phần trăm dd NaCl:
\(C\%_{ddNaCl}=\dfrac{15}{15+45}.100=25\%\)
a, Nồng độ % của dung dịch KCl là :
C%ddKCl = \(\dfrac{mct}{m\text{dd}}.100\%=\dfrac{20}{600}.100\%\approx3,333\%\)
b, ta có
Khối lượng dung dịch NaCl là :
mdd=mct+mdm=15+45=60 g
=> Nồng độ % của dung dịch NaCl là :
C%ddNaCl = \(\dfrac{mct}{m\text{dd}}.100\%=\dfrac{15}{60}.100\%=25\%\)

Câu 5:
PTHH : H2+ Cl2 -to-> 2 HCl
Vì số mol , tỉ lệ thuận theo thể tích , nên ta có:
25/1 = 25/1 => P.ứ hết, không có chất dư, tính theo chất nào cũng được
=> V(HCl)= 2. V(H2)= 2. 25= 50(l)
Câu 4: mFe2O3= 0,6. 80= 48(g)
=> nFe2O3= 48/160=0,3(mol)
mCuO= 80-48=32(g) => nCuO=32/80=0,4(mol)
PTHH: CuO + CO -to-> Cu + CO2
0,4_______0,4_____0,4____0,4(mol)
Fe2O3 + 3 CO -to-> 2 Fe +3 CO2
0,3_____0,9____0,6______0,9(mol)
=>nCO= 0,4+ 0,9= 1,3(mol)
=> V(CO, đktc)= 1,3. 22,4=29,12(l)

a) số mol của 19,5 gam Zn:
\(n_{Zn}=\dfrac{m}{M}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Tỉ lệ : 1 : 1 : 1 : 1
0,3-> 0,3 : 0,3 : 0,3
thể tích của 0,3 mol H2:
\(V_{H_2}=n.22,4=0,3.22,4=6,72\left(l\right)\)
b) số mol của 19,2 gam Fe2O3:
\(n_{Fe_2O_3}=\dfrac{m}{M}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
PTHH:
\(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
3 : 1 : 2 : 3
0,12-> 0,04 : 0,08 : 0,12 (mol)
Khối lượng của 0,08 mol Fe:
\(m_{Fe}=n.M=0,08.56=4,48\left(g\right)\)
PTHH: Zn + 2HCl ---> ZnCl₂ + H₂
1 2 1 1 ( mol)
a):Số mol Zn: nZn = 19,5 ÷ 65 = 0,3 mol.
Theo PTHH => Số mol H₂: nH₂ = 0,3 × 1 ÷ 1 = 0,3 mol
=> Thể tích H₂ (đktc): V = n × 22,4 = 0,3 × 22,4 = 6,72 lít
b) PTHH: Fe₂O₃ + 3H₂ --> 2Fe + 3H₂O
1 3 2 3 (mol)
*Lm tương tự nhưng thay vì tính thể tích thì tính KL Fe

a) +) Ta có: \(V_{ddKNO_3}=500\left(ml\right)=0,5\left(l\right)\\ =>n_{KNO_3}=0,5.2=1\left(mol\right)\\ =>m_{KNO_3}=1.101=101\left(g\right)\)
b) +) Ta có: \(V_{ddCaCl_2}=250\left(ml\right)=0,25\left(l\right)\\ =>n_{ddCaCl_2}=0,25.0,1=0,025\left(mol\right)\\ =>m_{CaCl_2}=111.0,025=2,775\left(g\right)\)

a)
\(Zn+H2SO4\rightarrow ZnSO4+H2\)
\(2Al+3H2SO4\rightarrow Al2\left(SO4\right)3+3H2\)
\(Fe+H2SO4\rightarrow FeSO4+H2\)
b) giải sử khối KL cùng là \(m\left(g\right)\)
\(\Rightarrow n_{Zn}=\frac{m}{65}\Rightarrow n_{H_2}=\frac{m}{65}\)
\(\Rightarrow n_{Al}=\frac{m}{27}\Rightarrow n_{H_2}=1,5.\frac{m}{27}\)
\(\Rightarrow n_{Fe}=\frac{m}{56}\Rightarrow n_{H_2}=\frac{m}{56}\)
\(\Rightarrow Al\)
c) Giả sử : \(n_{H_2}=0,15mol\)
\(\Rightarrow n_{Zn}=0,15mol\Rightarrow m=9,75g\)
\(\Rightarrow n_{Al}=0,1mol\Rightarrow m=2,7g\)
\(\Rightarrow n_{Fe}=0,15mol\Rightarrow m=8,4g\)
\(\Rightarrow Al\)
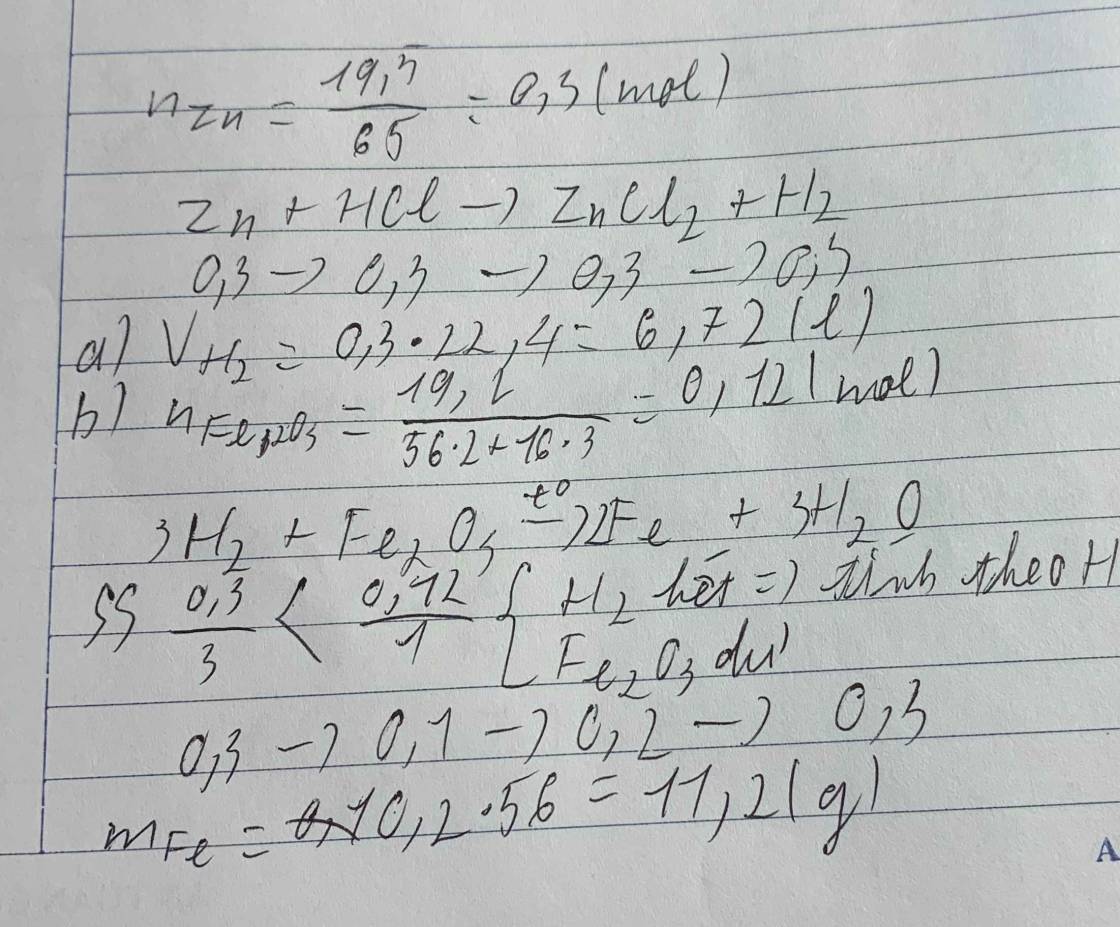

Ta có: \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH: Zn + 2HCl -> ZnCl2 + H2 (1)
a) Ta có: \(n_{H_2}=n_{Zn}=0,3\left(mol\right)\\ =>V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\)
b) PTHH: 3H2 + Fe2O3 -> 2Fe + 3H2O (2)
Ta có: \(\left\{{}\begin{matrix}n_{H_2\left(2\right)}=n_{H_2\left(1\right)}=0,3\left(mol\right)\\n_{Fe_2O_3\left(2\right)}=\dfrac{19,2}{160}=0,12\left(mol\right)\end{matrix}\right.\)
Ta có: \(\dfrac{0,3}{3}< \dfrac{0,12}{1}\)
=> Fe2O3 dư, H2 hết nên tính theo H2.
=> \(n_{Fe}=\dfrac{2.0,3}{3}=0,2\left(mol\right)\\ =>m_{Fe}=0,2.56=11,2\left(g\right)\)
a) PTHH: Zn + 2HCl --> ZnCl2 + H2
Ta có: nZn = \(\dfrac{19,5}{65}\) = 0,3 mol'
Theo PT: nZn = nH2 = 0,3 mol
=> VH2 = 0,3 x 22,4 = 6,72l
b) PTHH: Fe2O3 + 3H2 --> 2Fe + 3H2O
\(n_{Fe_2O_3}\) = \(\dfrac{19,2}{160}\) = 0,12 mol
Vì \(\dfrac{0,12}{1}>\dfrac{0,3}{3}\) => Fe2O3 dư
Cứ 3 mol H2 --> 2 mol Fe
0,3 mol --> 0,2 mol'
=> mFe = 0,2 x 56 = 11,2g
PTHH : Zn + 2HCl -> ZnCl2 + H2
a , nZn = \(\dfrac{19,5}{65}=0,3\left(mol\right)\)
Theo PTHH , nZn = nH2 = 0,3 (mol)
=> VH2(đktc) = 0,3.22,4 =6,72 (l)
b , PTHH : Fe2O3 + 3H2 -> 2Fe + 3H2O
nFe2O3 = \(\dfrac{19,2}{160}=0,12\left(mol\right)\)
Vì 0,12> 0,3/3 <=>0,12>0,1 => Fe2O3 dư , H2 hết => tính theo số mol H2
Theo PTHH , nFe =\(\dfrac{2}{3}n_{H2}\) = 0,3 (mol)
=>mFe = 0,3 . 56 = 16,8 (g)
Số mol của H2 ở Phương trình thứ 2 là bao nhiu vậy? Ko thấy có chỗ ấy
Sai rồi!
Thì là 0,3 mol = nH2 ở PT 1
@Nguyễn Trần Thành Đạt
Vậy thì bạn làm sao cho nó hợp lí
Mỹ Duyên ừ , nhần chỗ số mol Fe = 0,2 (mol)
Cảm ơn bạn đã nhắc nhở
Mỹ Duyên ừ , nhần chỗ số mol Fe = 0,2 (mol)
Cảm ơn bạn đã nhắc nhở
Mỹ Duyên ừ , nhần chỗ số mol Fe = 0,2 (mol)
Cảm ơn bạn đã nhắc nhở
Sao nhiều v?
Tại máy đơ , ấn nhiều vô enter
có 1 sự thật hơi bị "nhoi" trong mấy bài tập của Mỹ Duyên làm Nguyễn Trần Thành Đạt thường hay moi móc lỗi sai nhỉ ?Thường là ở chỗ nhỏ nhất á ^^ Ví dụ bài lần trước gọi CTHH của oxit , Nguyễn Trần Thành Đạt bảo : ko gọi CTHH thì ai biết M là j ? Bộ hai người có mối thù truyền kiếp hả ?
==========
đừng chém , ta sợ giang hồ
Ai mà bk đc! Tui chỉ bk là mk chưa lm j sai vs nó cả (Nguyễn Trần Thành Đạt ) . Haizzzzz! Liếc, liếc! tự hỉu nha @Hoang Thiên Di
HaHa... có ý cả đấy , nhìn là biết mờ
Mỹ Duyên
Mỹ Duyên các bạn cũng có thể nhắc tôi khi tôi làm sai mà! Hoang Thiên Di.
Dù là tôi hay là Như Khương, minh thương, Hậu Trần Công thì nếu sai tôi cũng góp ý
tôi chẳng biết ai trên này cả nên bạn ghi họ vào .... chịu Nguyễn Trần Thành Đạt
nên bạn ghi họ vào .... chịu Nguyễn Trần Thành Đạt
Nguyễn Trần Thành Đạt có j sai cho xin lỗi
tHÔI ! vậy mà cx cãi nhau đc! Hoang Thiên Di ; Nguyễn Trần Thành Đạt
Mỹ Duyên , đầu tiên bình luận cho vui mờ ... mà thôi chúc bạn 1/6 vui vẻ Mỹ Duyên+
Nguyễn Trần Thành Đạt
hjhj! Cảm động quá! Thanks! Hoang Thiên Di
Thanks! Hoang Thiên Di
bài này làm ntn vậy bạn
a) Có: \(n_{Zn}=\frac{19,5}{65}=0,3\left(mol\right)\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0,3-------->0,3\)
Thep phương trình trên, \(n_{H_2}=n_{Zn}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b) \(n_{Fe_2O_3}=\frac{19,2}{160}=0,12\left(mol\right)\)
PTHH:
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(0,3-->0,2\)
Theo phương trình,. ta thấy Fe2O3 còn dư sau phản ứng
\(\Rightarrow n_{Fe}=\frac{2}{3}n_{H_2}=\frac{2}{3}.0,3=0,2\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,2.56=11,2\left(g\right)\)