Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Xét TN2:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,2<--------------------------------0,3
=> mAl = 0,2.27 = 5,4 (g)
- Xét TN1:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2------------------->0,3
Mg + 2HCl --> MgCl2 + H2
0,15<------------------0,15
=> mMg = 0,15.24 = 3,6 (g)

\(n_{H_2}=\dfrac{12,32}{22,4}=0,55mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Gọi x, y lần lượt là số mol của Fe và Al:
\(\left\{{}\begin{matrix}56x+27y=13,7\\x+2y=0,55\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,15\\y=0,2\end{matrix}\right.mol\)
\(\%m_{Fe}=\dfrac{0,15.56}{13,7}.100\%=61,31\%\)

=> mFe + mAl= 11g
viết pt Fe, Al + HCl
đặt a,b là nFe, nAl
mFe + mAl = 56a + 27b= 11g
nH2= a + 1.5b= 0.4
=>a,b
=> mFe, mAl
Ag đứng sau H nên không phản ứng với dd H2SO4 loãng, nên chỉ có Al phản ứng:
2Al + 3H2SO4 → → Al2(SO4)3 + 3H2
0,3 mol
Theo pt trên, số mol Al = 2/3 số mol H2 = 0,2 mol. Nên khối lượng Al = 27.0,2 = 5,4 g.
Tổng khối lượng 2 kim loại = 5,4 + 4,6 = 10 g.
%Al = 5,4.100/10 = 54%; %Cu = 46%.


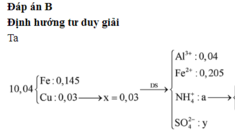
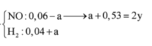
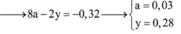
Fe + 2HCl----->FeCl2 +H2
x-------2x---------x--------x
2Al +6HCl------>2AlCl3 +3H2
y-------3y-----------y---------1,5y
Ta có
n\(_{H2}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
Theo bài ra ta có hệ pt
\(\left\{{}\begin{matrix}56x+27y=11\\x+1,5y=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
%m\(_{Fe}=\frac{0,1.56}{11}.100\%=50,91\%\)
%m\(_{Al}=100\%-50,91\%=49,09\%\)
Chúc bạn học tốt
Gọi x, y lần lượt là số mol của Fe, Al
Fe + 2HCl ---> FeCL2 + H2
mol 1 2 1 1
mol x 2x x x
2 Al + 6HCl ---> 2AlCl3 + 3H2
mol 2 6 2 3
mol y 3y y 1.5y
nH2 =8.96/22.4=0.4 mol
Ta có hệ phương trình sau
56x+27y=11 => x=0.1
x+1.5y= 0.4 => y=0.2
mFe= 0.1*56=5.6g
% mFe =5.6*100/11= 50.9%
%mAl= 100%-50.9%=49.1%