

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời. 2Al + 2NaOH + 2H2O -> 2NaAlO2 + 3H2 0,2 => mAl = 27.0,2 = 5,4 (gam) => %mAl = 5,4 %. Gọi số mol của Fe và Cr trong hỗn hợp là x và y. Fe + 2HCl -> FeCl2 + H2 x x(mol) Cr + 2HCl -> CrCl2 + H2 y y Ta có các phương trình : x + y = 56x + 52y = 94,6 (2). Giải hệ hai phương trình (1) và (2) ta được x = 1,55 ; y = 0,15. => mFe = 56.1,55 = 86,8 gam ; %mFe = 86,8%. Và mCr = 52.0,15 = 7,8 (gam) ; %mCr = 7,8 %. Mg + HCl - MgCl2 + H2 Al + HCl - AlCl3 + H2 còn Cu đứng sau H nên không phản ứng với HCl. nCuO = \(\dfrac{16}{80}=0,2\) mol Pt: 2Cu + O2 --to--> 2CuO 0,2 mol<--------------0,2 mol .....Mg + 2HCl --> MgCl2 + H2 0,2 mol<-----------0,2 mol .....2Al + 6HCl --> 2AlCl3 + 3H2 ....MgCl2 + 2NaOH --> Mg(OH)2 + 2NaCl ...0,2 mol<---------------0,2 mol ....AlCl3 + 3NaOH --> Al(OH)3 + 3NaCl ....Al(OH)3 + NaOH --> NaAlO2 + 2H2O ..........................................(tan) ...Mg(OH)2 --to--> MgO + H2O 0,2 mol<------------ 0,2 mol nMgO = \(\dfrac{8}{40}=0,2\) mol mCu = 0,2 . 64 = 12,8 (g) mMg = 0,2 . 24 = 4,8 (g) mAl = mhh - mCu - mMg = 20 - 12,8 - 4,8 = 2,4 (g) % mCu = \(\dfrac{12,8}{20}.100\%=64\%\) % mMg = \(\dfrac{4,8}{20}.100\%=24\%\) % mAl = \(\dfrac{2,4}{20}.100\%=12\%\) Gọi số mol của Mg, Al ,Cu có trong hỗn hợp lần lượt là a, b, c (mol) (a,b,c>0) Gọi số mol K và Al trong hỗn hợp x, y 2K + 2H2O → KOH + H2 (1) x x (mol) 2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑ (2) y y (mol) Do x tan hết nên Al hết, KOH dư sau (2). Khi thêm HCl, ban đầu chưa có kết tủa vì: HCl + KOH → KCl + H2O (3) X – y x – y (mol) Khi HCl trung hòa hết KOH dư thì bắt đầu có kết tủa: KAlO2 + HCl + H2O → Al(OH)3 ↓ + KCl (4) Vậy để trung hòa KOH dư cần 100 ml dung dịch HCl 1M. Ta có: nHCl = nKOH dư sau phản ứng (2) = x – y = 0,1.1 = 0,1 (mol) (I) Mặt khác: 39x + 27 y = 10,5 (II) Từ (1) và (II) => x = 0,2; y = 0,1. % nK = %nAl = 100% - 66,67% = 33,33%. K + HOH --> KOH +1/2H2 Al + KOH + HOH --> KAlO2 +3/2H2 -Cho HCl vào bd kg có ket tua => KOH du HCl + KOH --> KCl + HOH -Sau đó có ket tua => KOH het => KAlO2 phan ung KAlO2 + HCl + HOH --> Al(OH)3 + KCl vì den 100ml dd HCl 1M co xuat hien ket tua nen => n(KAlO2) =n(HCl) = 0,1 => n(Al) = 0,1 => %Al = 25,71% => %K =74,29% Luu y: hoi hóa xem bai giai co dung hay co van de nao kg gop ý dum nha thanks C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3 CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3 C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑ Y(AgCl, Ag) + HNO3 --> ... Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O phương trình dạng toán tử : \(\widehat{H}\)\(\Psi\) = E\(\Psi\) Toán tử Laplace: \(\bigtriangledown\)2 = \(\frac{\partial^2}{\partial x^2}\)+ \(\frac{\partial^2}{\partial y^2}\)+\(\frac{\partial^2}{\partial z^2}\) thay vào từng bài cụ thể ta có : a.sin(x+y+z) \(\bigtriangledown\)2 f(x,y,z) = ( \(\frac{\partial^2}{\partial x^2}\)+ \(\frac{\partial^2}{\partial y^2}\)+\(\frac{\partial^2}{\partial z^2}\))sin(x+y+z) =\(\frac{\partial^2}{\partial x^2}\)sin(x+y+z) + \(\frac{\partial^2}{\partial y^2}\)sin(x+y+z) + \(\frac{\partial^2}{\partial z^2}\)sin(x+y+z) =\(\frac{\partial}{\partial x}\)cos(x+y+z) + \(\frac{\partial}{\partial y}\)cos(x+y+z) + \(\frac{\partial}{\partial z}\)cos(x+y+z) = -3.sin(x+y+z) \(\Rightarrow\) sin(x+y+z) là hàm riêng. với trị riêng bằng -3. b.cos(xy+yz+zx) \(\bigtriangledown\)2 f(x,y,z) = ( \(\frac{\partial^2}{\partial x^2}\)+ \(\frac{\partial^2}{\partial y^2}\)+\(\frac{\partial^2}{\partial z^2}\))cos(xy+yz+zx) =\(\frac{\partial^2}{\partial x^2}\)cos(xy+yz+zx) +\(\frac{\partial^2}{\partial y^2}\)cos(xy+yz+zx) + \(\frac{\partial^2}{\partial z^2}\)cos(xy+yz+zx) =\(\frac{\partial}{\partial x}\)(y+z).-sin(xy+yz+zx) + \(\frac{\partial}{\partial y}\)(x+z).-sin(xy+yz+zx) + \(\frac{\partial}{\partial z}\)(y+x).-sin(xy+yz+zx) =- ((y+z)2cos(xy+yz+zx) + (x+z)2cos(xy+yz+zx) + (y+x)2cos(xy+yz+zx)) =-((y+z)2+ (x+z)2 + (x+z)2).cos(xy+yz+zx) \(\Rightarrow\) cos(xy+yz+zx) không là hàm riêng của toán tử laplace. c.exp(x2+y2+z2)


= 1,7 (1)


2Mg + O2 --t*--> 2MgO (1)
...a............................a (mol)
4Al + 3O2 --t*--> 2Al2O3 (2)
...b............................b/2 (mol)
2Cu + O2 --t*--> 2CuO (3)
...c.............................c (mol)
Khi m (g) hỗn hợp 3 kim loại trên tác dụng với HCl dư => Cu không phản ứng với HCl
Mg + 2HCl ---> MgCl2 + H2 (4)
..a...................................a (mol)
2Al + 6HCl ---> 2AlCl3 + 3H2 (5)
..b....................................3b/2 (mol)
Theo đầu ta có 24a + 27b + 64c = m (I)
..........................40a + 51b + 80c = 1,72m (II)
.......................... a + 3b/2 + 0c = 0,952m/22,4 (III)
Vì m(g) là 1 đại lượng chưa biết và cả 3 pt trên đều chứa m ở vế phải nên ta có thể giả sử m=1 (g) (Khi thay
m=1 không ảnh hưởng đến % khối lượng các chất có tronh hỗn hợp)
Khi đó thay m=1 vào (I), (II) (III) ta được:
(I) <=> 24a + 27b + 64c = 1
(II) <=> 40a + 51b + 80c = 1,72
(III) <=> a + 3b/2 +0c=0,0425
Giải hệ phương trình 3 ẩn (cái này nên dùng bằng máy tính là nhanh nhất) trên ta được
a = 0,0125 (mol) => mMg = 0,3g => %Mg=0,3/1.100%=30%
b = 0,02 (mol) => mAl = 0,54g => %Al= 0,54/1.100%=54%
c = 0,0025 (mol) => mCu = 0,16g => %Cu=0,16/1.100%=16%

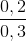 .100% = 66,67%;
.100% = 66,67%;

