Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nếu số lít SO2 =12.32 thì số mol sẽ là 0.55 nên Kl Cu =35.2(g).Không phù hợp yêu cầu của đề bài.

a)
$Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O$
$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
b) n Cu =a (mol) ; n Fe = b(mol)
=> 64a + 56b = 12(1)
n SO2 = a + 1,5b = 5,6/22,4 = 0,25(2)
(1)(2) suy ra a = b = 0,1
%m Cu = 0,1.64/12 .100% = 53,33%
%m Fe = 100% -53,33% = 46,67%
c)
n CuSO4 = a = 0,1(mol)
n Fe2(SO4)3 = 0,5a = 0,05(mol)
m muối = 0,1.160 + 0,05.400 = 36(gam)
d) n H2SO4 = 2n SO2 = 0,5(mol)
V H2SO4 = 0,5/2 = 0,25(lít)

Gọi số mol Cu, Fe là a, b (mol)
=> 64a + 56b = 17,6 (1)
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
b-------------------------------->1,5b
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
a--------------------------->a
=> a + 1,5b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,2 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,1.64}{17,6}.100\%=36,36\%\\\%m_{Fe}=\dfrac{0,2.56}{17,6}.100\%=63,64\%\end{matrix}\right.\)

Ta có: \(n_M=\dfrac{7}{M_M}\left(mol\right)\)
\(n_{SO_2}=0,1875\left(mol\right)\)
Giả sử: M có hóa trị cao nhất là a.
⇒ Số e cho là a.
Theo ĐLBT mol e, có: \(\dfrac{7a}{M_M}=0,1875.2\)
\(\Rightarrow M_M=\dfrac{56a}{3}\left(g/mol\right)\)
Với a = 1 ⇒ MM = 56/3 (loại)
a = 2 ⇒ MM = 112/3 (loại)
a = 3 ⇒ MM = 56 (nhận)
Vậy: M là Fe.
Bạn tham khảo nhé!

a)
nSO2=\(\dfrac{10,08}{22,4}\)= 0,45(mol)
2Al + 6H2SO4 --> Al2(SO4)3 + 6H2O +3SO2
x ---------------------------------------------> 3/2x
2Fe + 6H2SO4 --> Fe2(SO4)3 + 6H2O + 3SO2
y --------------------------------------------------> 3/2y
b) ta có hệ pt sau
\(\left\{{}\begin{matrix}27x+56y=11\\\dfrac{3}{2}x+\dfrac{3}{2}y=0,45\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
%mAl = \(\dfrac{0,2.27}{11}.100\)= 49%
%mFe=\(49-100\) =51%
c) m Al2(SO4)3= 0,1.342=34,2 g
mFe2(SO4)3=0,05.400=20 g

a) Gọi số mol của Al và Fe trong 13,8 gam hỗn hợp lần lượt là x và y
nH2 = 10,08:22.4= 0,45 mol
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
x ------------------------------------------>3/2x
Fe + H2SO4 → FeSO4 + H2
y ------------------------------------> y
Ta có hệ pt\(\left\{{}\begin{matrix}27x+56y=13,8\\\dfrac{3}{2}x+y=0,45\end{matrix}\right.\) => x = 0,2 và y = 0,15
=> mFe = 0,15.56 = 8,4 gam <=> %mFe = \(\dfrac{8,4}{13,8}\).100% = 60,87%
b)
X + O2 → Y
Bảo toàn khối lượng => mO2 = mY - mX = 5,76 gam <=> nO2 = 0,18 mol
Ta có sơ đồ: \(\left\{{}\begin{matrix}Fe\\Al\end{matrix}\right.\) + O2 → Y \(\underrightarrow{H_2SO_4đ,n}\) → Fe2(SO4)3 + Al2(SO4)3 + SO2 + H2O
Các quá trình oxi hóa - khử:
Fe0 → Fe+3 + 3e O20 + 4e → 2O-2
0,15 -> 0,45 0,18 --> 0,72
Al0 → Al+3 + 3e S+6 + 2e → S+4
0,2 -> 0,6 2x <- x
Áp dụng ĐLBT electron => 2x + 0,72 = 0,45 + 0,6
<=> x = 0,165
=>V SO2 đktc = 0,165.22,4 = 3,696 lít
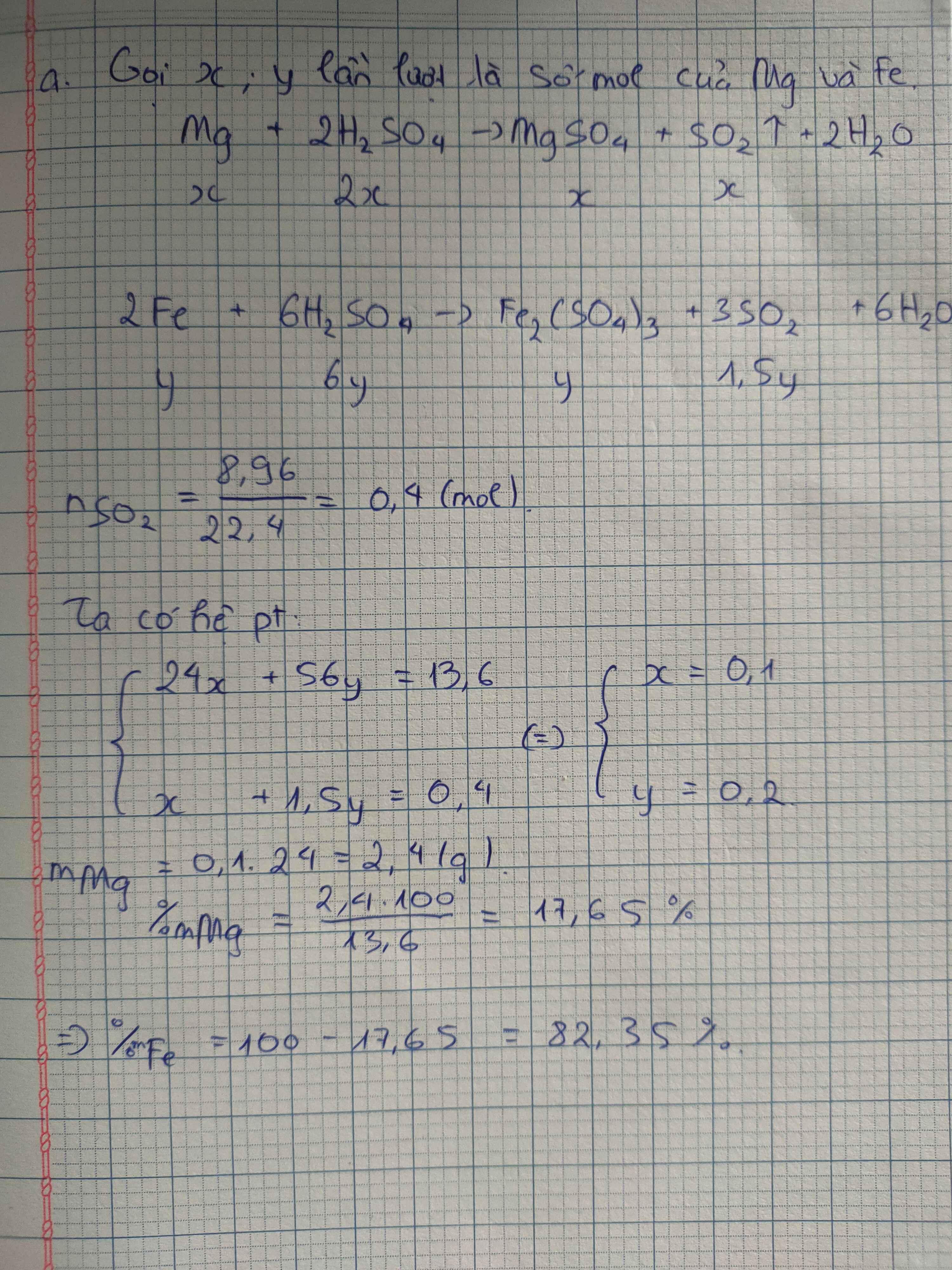




\(a) 2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O\\ 2Al+ 6H_2SO_4 \to Al_2(SO_4)_3 + 3SO_2 + 6H_2O\\ b) n_{Fe} = a(mol) ; n_{Al} = b(mol) \Rightarrow 56a + 27b = 11(1)\\ n_{SO_2} = 1,5a + 1,5b = \dfrac{10,08}{22,4} = 0,45(2)\\ (1)(2) \Rightarrow a = 0,1 ; b = 0,2\\ \%m_{Fe} = \dfrac{0,1.56}{11}.100\% = 50,91\%\\ \%m_{Al} = 100\%-50,91\% = 49,09\%\)
Giỏi thế bạn ơi iiu bạn nhìu
Bạn có thương mình giúp mình làm nốt câu dc ko ạ:
Câu 6:Cho 18,4 gam hỗn hợp gồm Cu và Fe tác dụng vớidung dịch H2SO4 đặc nóng dư thì thu được 7,84 lít khíSO2 (đktc, sản phẩm khử duy nhất) thoát ra.
1. Tính phần trăm khối lượng các kim loại trong hỗnhợp đầu.
2. Tính thể tích dung dịch NaOH 2M tối thiểu cần đểhấp thụ hết lượng SO2 thoát ra ở thí nghiệm trên.
Không cần phương trình nha:
Số mol của SO2: 10,08/22,4=0.45 (mol)
Gọi a và b là số mol của Fe và Al:
Bảo toàn khối lượng ta có:
56a + 27b = 11 (1)
Bảo toàn electron ta có:
Ai chưa biết:(Tổng số e nhường luôn bằng số e nhận)
3nFe + 3nAl = 2nSO2
=>3a + 3b = 2.0,45 (2)
Từ (1) và (2) => a=0,1 (mol) ; b=0,2 (mol)
=>%mFe=(0,1.56.100)/11=50,91%
%mAl=100-50,91=40,09%