Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Tính \(m\):
- Số mol khí:
\(n_{k h \overset{ˊ}{\imath}} = \frac{11 , 2}{22 , 4} = 0 , 5 \&\text{nbsp};\text{mol}\)
- Khối lượng Fe và Al theo tỉ lệ:
\(m_{A l} = 0 , 3 m , m_{F e} = 0 , 7 m\)
- Khối lượng rắn còn lại:
\(m_{r \overset{ˊ}{\overset{ }{a}} n} = 0 , 75 m\)
- Khối lượng kim loại phản ứng:
\(m_{p h ả n ứ n g} = m - 0 , 75 m = 0 , 25 m\)
- Giải hệ phương trình dựa vào phản ứng và số mol khí để tìm \(m\).
b) Tính thể tích dung dịch NaOH:
- Số mol kết tủa tính theo khối lượng 7,8 g.
- Tính số mol OH\(^{-}\) cần theo tỉ lệ phản ứng với Al và Fe trong dung dịch.
- Tính thể tích NaOH 2M:
\(V = \frac{n_{O H^{-}}}{2}\)

a,
Khi trộn hai cốc lại với nhau xảy ra phản ứng :
\(Na_2CO_3+2HCl-->2NaCl+H_2O+CO_2\)
Vì có khí CO2 thoát ra nên tổng khối lượng giảm
\(=>\) Sau một thời gian chờ hỗn hợp phản ứng hoàn toàn \(=>m_B< m_A\)
b, Cho từ từ cốc HCl vào cốc Na2CO3 xảy ra phản ứng :
\(Na_2CO_3+HCl-->NaCl+NaHCO_3\)
Nếu NaCO3 dư thì không khí có thoát ra . Để lâu ngoài không khí xảy ra phản ứng :
\(Na_2CO_3+CO_2+H_2O-->2NaHCO_3\)
Do hấp thụ CO2 ngoài không khí nên lúc đó khối lượng mB tăng lên
\(->m_B>m_A\)
Vậy .....................

Bài 1 : nBa(2+)=0,1.0,5+0,1.0,4=0,09 mol
nHCO3- = 0,1 mol --> n CO3(2-)=0,1 mol
-->nCO3(2-)>nBa(2+)
nBaCO3 = 0,09 mol
--->mBaCO3=17,73g
Bài 2: Mg + 2FeCl3 --> MgCl2 + 2FeCl2
Mg + FeCl2 --> MgCl2 + Fe
Nếu sau pư Mg dư thì m rắn = mMg dư +mFe = m Mg dư + 56x0.12 = mMg dư + 6.72 > 3.36g
Vậy chất rắn sau pư chỉ có Fe
n = 0.06 mol
nMg = 0.5n FeCl3 + nFe = 0.5x0.12 + 0.06 = 0.12mol
=> m = 2.88g

Sách giáo khoaa cần cải cách vấn đề này, chứ dạy học sinh theo sách mà đáp án lại ra theo thí nghiệm thì căn cứ ở đâu mà chấm? Hồi đó tỉnh em cũng bị cái này :v trong sgk bảo màu vàng :v nhưng thi ra lại là màu nâu đất :v mọi người đều nói là lấy sgk làm căn cứ :))) nhưng người ra đề lấy thực tế và học sinh đều bị trừ câu đó 0,25 đ (trừ mấy người làm sai ^_^). 0,25 đ :))) đủ khiến một vài ai đó rớt tốt nghiệp cấp II và tuyển sinh lớp 10 :v
nói tóm tác vấn đề của cô giáo đã nói :
| muối tạo bởi | bazơ mạnh | bazơ yếu |
| axit mạnh | không đổi màu quì tím | đổi màu quì tím sang màu đỏ |
| axit yếu | đổi màu quì tím sang màu xanh | trường hợp này thì chưa chắc được và độ pH của nó gần bằng 7 |

Câu 1 :
\(a.CH_4+Cl_2\underrightarrow{as,1:1}CH_3Cl+HCl\)
\(b.C_2H_4+H_2O\underrightarrow{^{H^+,t^0}}C_2H_5OH\)
\(c.CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
\(d.C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
\(e.CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(f.\left(RCOO\right)_3C_3H_5+3NaOH\rightarrow3RCOONa+C_3H_5\left(OH\right)_3\)
Câu 2 :
a) CTCT C2H2 và C2H6 :
\(CH\equiv CH\)
\(CH_3-CH_3\)
b) Nhận biết CH4, C2H4 :
Sục lần lượt các khí qua dung dịch Br2 dư :
- Mất màu : C2H4
- Không HT : CH4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
c)
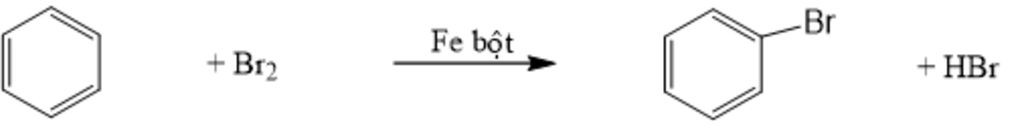
TN1 : Mất màu nâu đỏ Br2 và có khí HBr thoát ra.
 TN2 :
TN2 :
Dầu ăn không tan trong nước , nổi trên bề mặt
Câu 3 :
\(n_{CH_4}=a\left(mol\right),n_{C_2H_6}=b\left(mol\right)\)
\(n_X=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+b=0.2\left(1\right)\)
\(n_{CaCO_3}=\dfrac{30}{100}=0.3\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{^{t^0}}CO_2+2H_2O\)
\(C_2H_6+\dfrac{7}{2}O_2\underrightarrow{^{t^0}}2CO_2+3H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(..............0.3......0.3\)
\(n_{CO_2}=a+2b=0.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%V_{CH_4}=\%V_{C_2H_6}=\dfrac{0.1}{0.2}\cdot100\%=50\%\)
Câu 4 :
\(\text{ Trong 100 ml cồn 70 độ có 70 ml rượu etylic và 30 ml nước.}\)
\(V_{C_2H_5OH}=\dfrac{70}{100}\cdot50=35\left(ml\right)\)
\(n_{C_2H_5OH}=\dfrac{9.2}{46}=0.2\left(mol\right)\)
\(n_{CH_3COOH}=\dfrac{6}{60}=0.1\left(mol\right)\)
\(CH_3COOH+C_2H_5OH\underrightarrow{H^+,t^0}CH_3COOC_2H_5+H_2O\)
\(0.1.........................0.1....................0.1\)
\(H\%=\dfrac{5.28}{0.1\cdot88}\cdot100\%=60\%\)
