Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

số mol kẽm tham gia phản ứng là:\(n_{Zn}=\frac{m}{M}=\frac{6,5}{65}=0,1\left(mol\right)\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 (mol)
a, thể tích khí hiđro thu được là:\(V_{H_2}=n_{H_2}\times22,4=0,1\times22,4=2,24\left(l\right)\)
b,khối lượng HCl cần dùng là:\(m_{HCl}=n_{HCl}\times M=0,2\times65=13\left(g\right)\)

\(Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\\ a,\%m_{Fe}=\dfrac{0,02.56}{4,36}.100\approx25,688\%\\ \Rightarrow\%m_{Ag}\approx74,312\%\\ b,Ta.thấy:2,18=\dfrac{1}{2}.4,36\\ \Rightarrow m_{hh\left(câuB\right)}=\dfrac{1}{2}.m_{hh\left(câuA\right)}\\ n_{Fe}=\dfrac{0,02}{2}=0,01\left(mol\right)\\ n_{Ag}=\dfrac{2,18-0,01.56}{108}=0,015\left(mol\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ 2Ag+Cl_2\rightarrow\left(t^o\right)2AgCl\\ n_{Cl_2}=\dfrac{3}{2}.n_{Fe}+\dfrac{1}{2}.n_{Ag}=\dfrac{3}{2}.0,01+\dfrac{1}{2}.0,015=0,0225\left(mol\right)\\ \Rightarrow V_{Cl_2\left(đktc\right)}=0,0225.22,4=0,504\left(l\right)\)

a, PTHH: 2Mg + O2 ---to→ 2MgO
b, Theo ĐLBTKL ta có:
\(m_{Mg}+m_{O_2}=m_{MgO}\)
c, \(m_{Mg}+m_{O_2}=m_{MgO}\Leftrightarrow m_{O_2}=m_{MgO}-m_{Mg}=15-9=6\left(g\right)\)

a) Giả sử lấy lượng mỗi chất là a gam
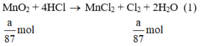
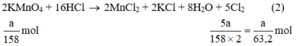
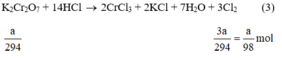
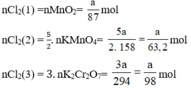
Ta có: 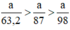
Lượng Cl2 điều chế được từ pt (2) nhiều nhất.
Vậy dùng KMnO4 điều chế được nhiều Cl2 hơn.
b) Nếu lấy số mol các chất bằng a mol
Theo (1) nCl2(1) = nMnO2 = a mol
Theo (2) nCl2(2) = 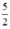 . nKMnO4 = 2,5a mol
. nKMnO4 = 2,5a mol
Theo (3) nCl2(3) = 3. nK2Cr2O7 = 3a mol
Ta có: 3a > 2,5a > a.
⇒ lượng Cl2 điều chế được từ pt (3) nhiều nhất.
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn.

sao chị ko đáp lại câu trả lời của em ở câu trước , chị ko biết hả ?



Fe2O3 + 3H2 --to--> 2Fe + 3H2O
Fe + 2HCl → FeCl2+ H2
2H2 + O2 --to---> 2H2O
Fe\(_2O_3\)+3CO\(\rightarrow\)2Fe+3CO\(_2\uparrow\)
Fe+H\(_2SO_4\)\(\rightarrow\)\(H_2\uparrow+FeSO_4\)
\(2H_2+O_2\rightarrow2H_2O\) Điều kiện:nhiệt độ
nZn = 0,2 mol
2Zn + O2 --to--> 2ZnO
0,2.....0,1...............0,2
⇒ mZnO = 0,2.81 = 16,2 (g)
⇒ Vkk = 0,1.22,4.5 = 11,2 (l)
2KMnO4 ---to--> K2MnO4 + MnO2 + O2
⇒ mKMnO4 = 0,2.158 = 31,6 (g)
nH2 = 0,1 mol
2H2 + O2 ---to--> 2H2O
Đặt tỉ lệ ta có
\(\dfrac{0,1}{2}\) < 0,1
⇒ O2 dư
⇒ mH2O = 0,1.18 = 18 (g)
phương trình 1 thiếu nhiệt độ
giúp mình viết PTPƯ với thanks
zòi mak
uk.bây giờ mới thấy hihi
mà câu 1 á có 2 câu trả lời minhg nên chọn cái nào đây
tùy bn
bạn ơi cho mình hỏi phản ứng 1 ,2 là phản ứng thế phải ko vậy
uh
uk