Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. biết \(M_{O_2}=2.16=32\left(đvC\right)\)
vậy \(M_X=\) \(32.5=160\left(đvC\right)\)
b. gọi CTHH của hợp chất là \(A_2O_3\)
ta có:
\(2A+3O=160\)
\(2A+3.16=160\)
\(2A+48=160\)
\(2A=160-48=112\)
\(A=\dfrac{112}{2}=56\left(đvC\right)\)
\(\Rightarrow A\) là sắt, kí hiệu là \(Fe\)
c. \(CTHH:Fe_2O_3\)

gOI HỢP CHẤT là \(XO_2\)
Theo bài: \(M_{XO_2}=32M_{H_2}=64\left(đvC\right)\)
Mà \(M_X+2M_O=64\Rightarrow M_X=32\left(đvC\right)\)
Vậy X là nguyên tố lưu huỳnh.KHHh:S

Gọi hợp chất là $XO_2$.
Phân tử hiđro là $H_2$ có phân tử khối:
$M_{H_2}=2$
Theo đề bài, hợp chất nặng hơn phân tử hiđro 32 lần, nên:
$M_{XO_2}=32\cdot2=64$
Ta có:
$M_{XO_2}=M_X+2\cdot16$
$64=M_X+32$
$M_X=32$
Nguyên tố có nguyên tử khối bằng $32$ là lưu huỳnh.
Tên nguyên tố: Lưu huỳnh
Kí hiệu hóa học: S

PTK của hợp chất = $32M_{H_2} = 32.2 = 64(đvC)$
Suy ra : X + 16.2 = 64 $\Rightarrow X = 32$
Vậy X là lưu huỳnh, KHHH : S
PTKhidro = 1.2 = 2
→ PTKh/c = 32.2 = 64
→ NTKX = 64 - 16.2 = 32
→ X là nguyên tố Lưu huỳnh. Kí hiệu là S

a. Gọi CTHH của oxit là: A2O3
Ta có: \(d_{\dfrac{A_2O_3}{O_2}}=\dfrac{M_{A_2O_3}}{M_{O_2}}=\dfrac{M_{A_2O_3}}{32}=5\left(lần\right)\)
=> \(M_{A_2O_3}=160\left(g\right)\)
b. Ta có: \(M_{A_2O_3}=M_A.2+16.3=160\left(g\right)\)
=> MA = 56(g)
=> A là sắt (Fe)
c. Vậy CTHH của X là: Fe2O3

Câu 2.
Gọi công thức của hợp chất là $XO_2$.
Phân tử hiđro là $H_2$ nên:
$M_{H_2}=2$
Hợp chất nặng hơn phân tử hiđro $32$ lần nên:
$M_{XO_2}=32\cdot2=64$
Ta có:
$M_{XO_2}=M_X+2\cdot16$
$64=M_X+32$
$M_X=32$
Nguyên tố có nguyên tử khối bằng $32$ là lưu huỳnh.
Kí hiệu hóa học: $S$
Câu 3.
Gọi số proton, electron, nơtron của nguyên tử $Y$ lần lượt là $p,e,n$.
Vì nguyên tử trung hòa điện nên:
$p=e$
Theo đề bài:
$p+e+n=52$
$\Rightarrow p+p+n=52$
$\Rightarrow 2p+n=52$ (1)
Trong hạt nhân, số hạt không mang điện là nơtron,
số hạt mang điện là proton.
Theo đề:
$n=p+1$ (2)
Thế (2) vào (1):
$2p+(p+1)=52$
$3p+1=52$
$3p=51$
$p=17$
Suy ra:
$e=p=17$
$n=p+1=18$
Vậy $p=17,\quad e=17,\quad n=18$

a, PTK của hợp chất là 32.4,4375 = 142 (g/mol)
b,Ta có: \(2M_P+5M_X=142\)
\(\Leftrightarrow2.31+5M_X=142\)
\(\Leftrightarrow5M_X=80\Leftrightarrow M_X=16\left(g/mol\right)\)
⇒ X là nguyên tố oxi (O)
a, PTK của hợp chất là 32.4,4375 = 142 (g/mol)
b,Ta có: 2MP+5MX=1422MP+5MX=142
⇔2.31+5MX=142⇔2.31+5MX=142
⇔5MX=80⇔MX=16(g/mol)⇔5MX=80⇔MX=16(g/mol)
⇒ X là nguyên tố oxi (O)

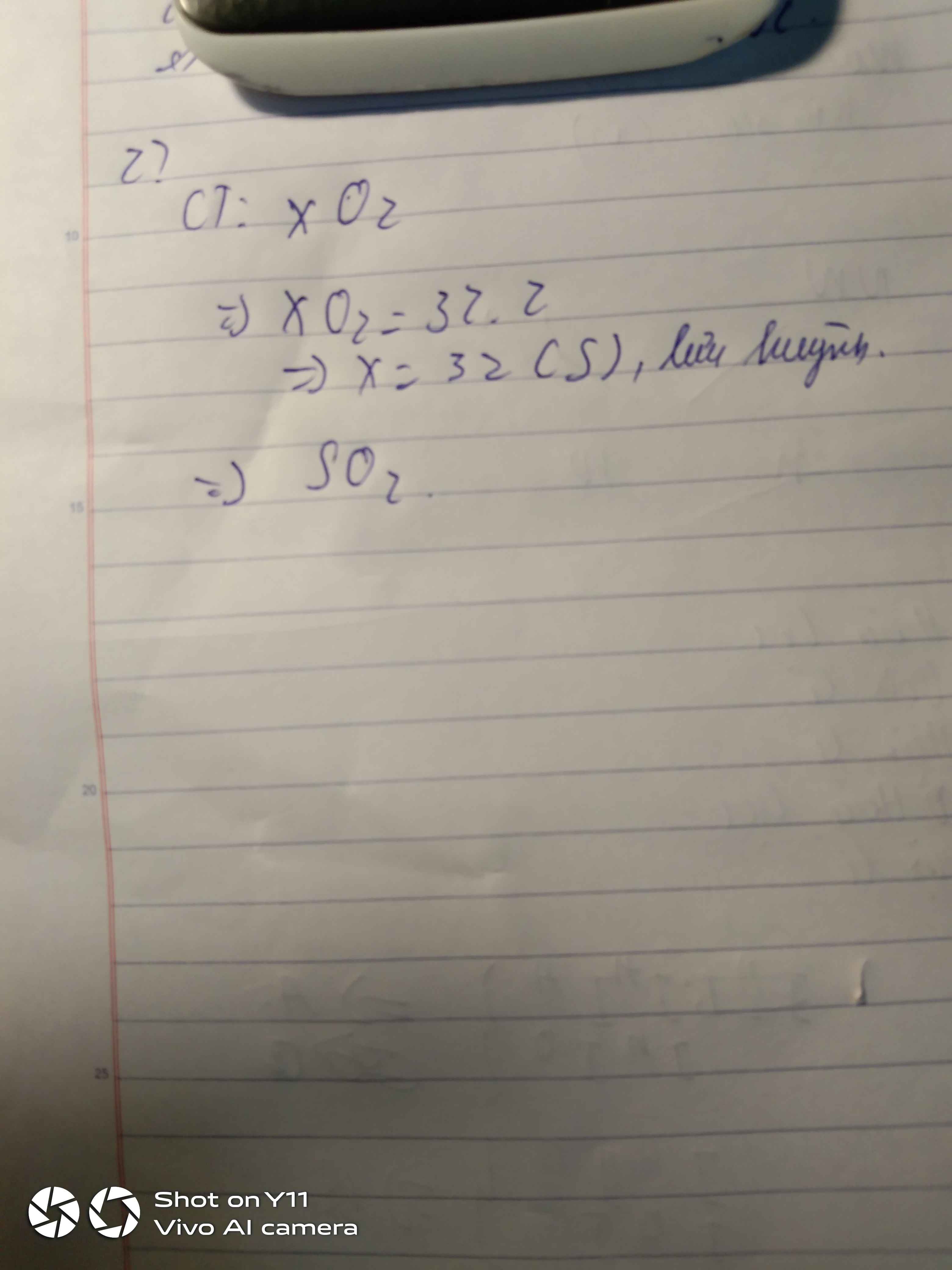
CTPT của A là : \(X_3O_4\)
\(M_A=116\cdot M_{H_2}=2\cdot116=232\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow3X+16\cdot4=232\)
\(\Rightarrow X=56\)
\(X:Fe\)
\(CTHH:Fe_3O_4\)
a. Gọi CTHH là: X3O4
Theo đề, ta có:
\(d_{\dfrac{X_3O_4}{H_2}}=\dfrac{M_{X_3O_4}}{2}=116\left(lần\right)\)
\(\Rightarrow PTK_{X_3O_4}=M_{X_3O_4}=232\left(g\right)\)
b. Ta có: \(M_{X_3O_4}=NTK_X.3+16.4=232\left(g\right)\)
\(\Rightarrow NTK_X=56\left(đvC\right)\)
Vậy X là sắt (Fe)
CTHH là Fe3O4
a. biết \(PTK_{H_2}=2.1=2\left(đvC\right)\)
vậy \(PTK_A=116.2=232\left(đvC\right)\)
b. gọi CTHH của A là \(X_3O_4\), ta có:
\(3X+4O=232\)
\(3X+4.16=232\)
\(3X+64=232\)
\(3X=232-64=168\)
\(X=\dfrac{168}{3}=56\left(đvC\right)\)
\(\Rightarrow X\) là sắt \(\left(Fe\right)\)
\(\Rightarrow CTHH:Fe_3O_4\) (Oxit sắt từ)
M là j v?
Khí hiệu tỉ khối d có được dùng với chất rắn không bạn ?
Thân ái mời bạn lật trang số 69, SGK Hóa Học 8, Bài 20 : Tỉ khối của chất khí nha.
Dạ, lúc đó em định sửa nhưng ko sửa được nên để vậy luôn